Objectifs d’apprentissage
À la fin de cette section, vous serez en mesure de :
- Décrire la matière et les éléments
- Décrire l’interrelation entre les protons, les neutrons et les électrons, et les façons dont les électrons peuvent être donnés ou partagés entre les atomes
À son niveau le plus fondamental, la vie est constituée de matière. La matière occupe l’espace et possède une masse. Toute matière est composée d’éléments, des substances qui ne peuvent pas être décomposées ou transformées chimiquement en d’autres substances. Chaque élément est constitué d’atomes, chacun ayant un nombre constant de protons et des propriétés uniques. Au total, 118 éléments ont été définis ; toutefois, seuls 92 sont présents à l’état naturel, et moins de 30 sont présents dans les cellules vivantes. Les 26 éléments restants sont instables et, par conséquent, n’existent pas pendant très longtemps ou sont théoriques et n’ont pas encore été détectés.
Chaque élément est désigné par son symbole chimique (comme H, N, O, C et Na), et possède des propriétés uniques. Ces propriétés uniques permettent aux éléments de se combiner et de se lier entre eux de manière spécifique.
Atomes
Un atome est le plus petit composant d’un élément qui conserve toutes les propriétés chimiques de cet élément. Par exemple, un atome d’hydrogène possède toutes les propriétés de l’élément hydrogène, comme le fait qu’il existe sous forme de gaz à température ambiante, et qu’il se lie à l’oxygène pour créer une molécule d’eau. Les atomes d’hydrogène ne peuvent pas être décomposés en quelque chose de plus petit tout en conservant les propriétés de l’hydrogène. Si un atome d’hydrogène était décomposé en particules subatomiques, il n’aurait plus les propriétés de l’hydrogène.
Au niveau le plus élémentaire, tous les organismes sont constitués d’une combinaison d’éléments. Ils contiennent des atomes qui se combinent entre eux pour former des molécules. Dans les organismes multicellulaires, comme les animaux, les molécules peuvent interagir pour former des cellules qui se combinent pour former des tissus, lesquels constituent les organes. Ces combinaisons continuent jusqu’à ce que des organismes multicellulaires entiers soient formés.

Figure 1. Les atomes sont constitués de protons et de neutrons situés dans le noyau, et d’électrons entourant le noyau.
Tous les atomes contiennent des protons, des électrons et des neutrons (figure 1). La seule exception est l’hydrogène (H), qui est constitué d’un proton et d’un électron. Un proton est une particule chargée positivement qui réside dans le noyau (le cœur de l’atome) d’un atome et a une masse de 1 et une charge de +1. Un électron est une particule chargée négativement qui se déplace dans l’espace autour du noyau. En d’autres termes, il réside à l’extérieur du noyau. Il a une masse négligeable et une charge de -1.
Les neutrons, comme les protons, résident dans le noyau d’un atome. Ils ont une masse de 1 et n’ont pas de charge. Les charges positives (protons) et négatives (électrons) s’équilibrent dans un atome neutre, qui a une charge nette nulle.
Parce que les protons et les neutrons ont chacun une masse de 1, la masse d’un atome est égale au nombre de protons et de neutrons de cet atome. Le nombre d’électrons n’entre pas en ligne de compte dans la masse globale, car leur masse est si petite.
Comme indiqué précédemment, chaque élément a ses propres propriétés uniques. Chacun contient un nombre différent de protons et de neutrons, ce qui lui donne son propre numéro atomique et son propre numéro de masse. Le numéro atomique d’un élément est égal au nombre de protons que cet élément contient. Le numéro de masse est le nombre de protons plus le nombre de neutrons de cet élément. Il est donc possible de déterminer le nombre de neutrons en soustrayant le numéro atomique du numéro de masse.
Ces nombres fournissent des informations sur les éléments et la façon dont ils vont réagir lorsqu’ils sont combinés. Les différents éléments ont des points de fusion et d’ébullition différents, et sont dans différents états (liquide, solide ou gaz) à température ambiante. Ils se combinent également de différentes manières. Certains forment des types de liaisons spécifiques, tandis que d’autres ne le font pas. La façon dont ils se combinent dépend du nombre d’électrons présents. En raison de ces caractéristiques, les éléments sont classés dans le tableau périodique des éléments, un tableau des éléments qui comprend le numéro atomique et la masse atomique relative de chaque élément. Le tableau périodique fournit également des informations clés sur les propriétés des éléments (figure 2), souvent indiquées par un code de couleurs. La disposition du tableau montre également comment les électrons de chaque élément sont organisés et fournit des détails importants sur la façon dont les atomes vont réagir les uns avec les autres pour former des molécules.
Les isotopes sont différentes formes d’un même élément qui ont le même nombre de protons, mais un nombre différent de neutrons. Certains éléments, comme le carbone, le potassium et l’uranium, ont des isotopes naturels. Le carbone 12, l’isotope le plus courant du carbone, contient six protons et six neutrons. Il a donc un numéro de masse de 12 (six protons et six neutrons) et un numéro atomique de 6 (ce qui en fait du carbone). Le carbone 14 contient six protons et huit neutrons. Il a donc un numéro de masse de 14 (six protons et huit neutrons) et un numéro atomique de 6, ce qui signifie qu’il s’agit toujours de l’élément carbone. Ces deux formes alternatives du carbone sont des isotopes. Certains isotopes sont instables et vont perdre des protons, d’autres particules subatomiques ou de l’énergie pour former des éléments plus stables. On les appelle isotopes radioactifs ou radioisotopes.
Art Connection

Figure 2. Disposé en colonnes et en lignes en fonction des caractéristiques des éléments, le tableau périodique fournit des informations clés sur les éléments et sur la façon dont ils pourraient interagir entre eux pour former des molécules. La plupart des tableaux périodiques fournissent une clé ou une légende aux informations qu’ils contiennent.
Combien de neutrons possèdent respectivement le (K) potassium-39 et le potassium-40 ?
L’évolution en action
Datation au carbone

Figure 3. L’âge des restes qui contiennent du carbone et qui ont moins de 50 000 ans environ, comme ce mammouth pygmée, peut être déterminé par la datation au carbone. (crédit : Bill Faulkner/NPS)
Le carbone 14 (14C) est un radio-isotope naturel qui est créé dans l’atmosphère par les rayons cosmiques. Il s’agit d’un processus continu, de sorte que davantage de 14C est toujours créé. Lorsqu’un organisme vivant se développe, le niveau relatif de 14C dans son corps est égal à la concentration de 14C dans l’atmosphère. Lorsqu’un organisme meurt, il n’ingère plus de 14C, de sorte que le rapport diminue. Le 14C se désintègre en 14N par un processus appelé désintégration bêta ; il dégage de l’énergie dans ce lent processus.
Après environ 5 730 ans, seule la moitié de la concentration initiale de 14C aura été convertie en 14N. Le temps nécessaire pour que la moitié de la concentration initiale d’un isotope se désintègre en sa forme la plus stable est appelé sa demi-vie. Comme la demi-vie du 14C est longue, on l’utilise pour déterminer l’âge d’anciens objets vivants, comme les fossiles. En utilisant le rapport entre la concentration de 14C trouvée dans un objet et la quantité de 14C détectée dans l’atmosphère, on peut déterminer la quantité d’isotope qui ne s’est pas encore désintégrée. Sur la base de cette quantité, l’âge du fossile peut être calculé à environ 50 000 ans (figure 3). Les isotopes ayant une demi-vie plus longue, comme le potassium 40, sont utilisés pour calculer l’âge des fossiles plus anciens. Grâce à la datation au carbone, les scientifiques peuvent reconstituer l’écologie et la biogéographie des organismes vivant au cours des 50 000 dernières années.
Concept en action
Cette simulation vous en apprend davantage sur les atomes et les isotopes, et sur la façon dont vous pouvez distinguer un isotope d’un autre.
Les liaisons chimiques
La façon dont les éléments interagissent les uns avec les autres dépend de la façon dont leurs électrons sont disposés et du nombre d’ouvertures pour les électrons qui existent dans la région la plus extérieure où les électrons sont présents dans un atome. Les électrons existent à des niveaux d’énergie qui forment des coquilles autour du noyau. La coquille la plus proche peut contenir jusqu’à deux électrons. La coquille la plus proche du noyau est toujours remplie en premier, avant que toute autre coquille puisse être remplie. L’hydrogène a un électron ; par conséquent, il n’a qu’une seule place occupée dans la coquille la plus basse. L’hélium a deux électrons ; il peut donc remplir complètement la coquille la plus basse avec ses deux électrons. Si vous regardez le tableau périodique, vous verrez que l’hydrogène et l’hélium sont les deux seuls éléments de la première rangée. Cela s’explique par le fait qu’ils n’ont que des électrons dans leur première coquille. L’hydrogène et l’hélium sont les deux seuls éléments qui ont la coquille la plus basse et aucune autre coquille.
Les deuxième et troisième niveaux d’énergie peuvent contenir jusqu’à huit électrons. Les huit électrons sont disposés en quatre paires et une position dans chaque paire est remplie par un électron avant que toute paire ne soit complétée.
En regardant à nouveau le tableau périodique (figure 2), vous remarquerez qu’il y a sept rangées. Ces rangées correspondent au nombre de coquilles que possèdent les éléments de cette rangée. Les éléments d’une rangée donnée ont un nombre croissant d’électrons au fur et à mesure que les colonnes vont de gauche à droite. Bien que chaque élément ait le même nombre de coquilles, toutes les coquilles ne sont pas complètement remplies d’électrons. Si vous regardez la deuxième rangée du tableau périodique, vous trouverez le lithium (Li), le béryllium (Be), le bore (B), le carbone (C), l’azote (N), l’oxygène (O), le fluor (F) et le néon (Ne). Tous ces éléments ont des électrons qui n’occupent que les première et deuxième coquilles. Le lithium n’a qu’un seul électron dans sa coquille la plus externe, le béryllium en a deux, le bore en a trois, et ainsi de suite, jusqu’à ce que la coquille entière soit remplie de huit électrons, comme c’est le cas pour le néon.
Tous les éléments n’ont pas assez d’électrons pour remplir leur coquille la plus externe, mais un atome est le plus stable lorsque toutes les positions d’électrons dans la coquille la plus externe sont remplies. En raison de ces vacances dans les coquilles les plus externes, nous assistons à la formation de liaisons chimiques, ou d’interactions entre deux ou plusieurs éléments identiques ou différents, qui aboutissent à la formation de molécules. Pour atteindre une plus grande stabilité, les atomes auront tendance à remplir complètement leurs coquilles externes et se lieront à d’autres éléments pour atteindre cet objectif en partageant des électrons, en acceptant des électrons d’un autre atome ou en donnant des électrons à un autre atome. Comme les coquilles extérieures des éléments de faible numéro atomique (jusqu’au calcium, dont le numéro atomique est 20) peuvent contenir huit électrons, on parle de la règle de l’octuor. Un élément peut donner, accepter ou partager des électrons avec d’autres éléments pour remplir sa coquille externe et satisfaire à la règle de l’octuor.

Figure 4. Les éléments ont tendance à remplir leurs coquilles externes avec des électrons. Pour ce faire, ils peuvent soit donner ou accepter des électrons d’autres éléments.
Lorsqu’un atome ne contient pas un nombre égal de protons et d’électrons, il est appelé un ion. Comme le nombre d’électrons n’est pas égal au nombre de protons, chaque ion a une charge nette. Les ions positifs sont formés en perdant des électrons et sont appelés cations. Les ions négatifs sont formés en gagnant des électrons et sont appelés anions. Les noms anioniques élémentaires sont modifiés pour se terminer par -ide.
Par exemple, le sodium n’a qu’un électron dans sa coquille la plus externe. Il faut moins d’énergie au sodium pour donner cet électron que pour accepter sept électrons supplémentaires pour remplir la coquille extérieure. Si le sodium perd un électron, il a maintenant 11 protons et seulement 10 électrons, ce qui lui laisse une charge globale de +1. On l’appelle maintenant un ion sodium.
L’atome de chlore a sept électrons dans sa coquille externe. Encore une fois, il est plus efficace du point de vue énergétique pour le chlore de gagner un électron que d’en perdre sept. Par conséquent, il a tendance à gagner un électron pour créer un ion avec 17 protons et 18 électrons, ce qui lui donne une charge négative nette (-1). On l’appelle maintenant un ion chlorure. Ce mouvement des électrons d’un élément à l’autre est appelé transfert d’électrons. Comme l’illustre la figure 4, un atome de sodium (Na) ne possède qu’un seul électron dans sa coquille externe, alors qu’un atome de chlore (Cl) possède sept électrons dans sa coquille externe. Un atome de sodium donnera son électron pour vider sa coquille, et un atome de chlore acceptera cet électron pour remplir sa coquille, devenant ainsi du chlorure. Les deux ions satisfont maintenant à la règle de l’octuor et ont des coquilles extérieures complètes. Comme le nombre d’électrons n’est plus égal au nombre de protons, chacun est maintenant un ion et a une charge de +1 (sodium) ou de -1 (chlorure).
Les liaisons ioniques
Il existe quatre types de liaisons ou d’interactions : les liaisons ioniques, covalentes, les liaisons hydrogène et les interactions de van der Waals. Les liaisons ioniques et covalentes sont des interactions fortes qui nécessitent un apport d’énergie plus important pour se rompre. Lorsqu’un élément donne un électron de son enveloppe extérieure, comme dans l’exemple de l’atome de sodium ci-dessus, un ion positif est formé. L’élément qui accepte l’électron est maintenant chargé négativement. Comme les charges positives et négatives s’attirent, ces ions restent ensemble et forment une liaison ionique, ou une liaison entre ions. Les éléments se lient entre eux, l’électron d’un élément restant majoritairement dans l’autre élément. Lorsque les ions Na+ et Cl- se combinent pour produire NaCl, un électron d’un atome de sodium reste avec les sept autres de l’atome de chlore, et les ions sodium et chlorure s’attirent mutuellement dans un réseau d’ions avec une charge nette nulle.
Liens covalents
Un autre type de liaison chimique forte entre deux ou plusieurs atomes est une liaison covalente. Ces liaisons se forment lorsqu’un électron est partagé entre deux éléments et constituent la forme la plus forte et la plus courante de liaison chimique dans les organismes vivants. Les liaisons covalentes se forment entre les éléments qui composent les molécules biologiques de nos cellules. Contrairement aux liaisons ioniques, les liaisons covalentes ne se dissocient pas dans l’eau.
Les atomes d’hydrogène et d’oxygène qui se combinent pour former les molécules d’eau sont liés entre eux par des liaisons covalentes. L’électron de l’atome d’hydrogène partage son temps entre l’enveloppe externe de l’atome d’hydrogène et l’enveloppe externe incomplète de l’atome d’oxygène. Pour remplir complètement l’enveloppe externe d’un atome d’oxygène, deux électrons provenant de deux atomes d’hydrogène sont nécessaires, d’où l’indice « 2 » dans H2O. Les électrons sont partagés entre les atomes, partageant leur temps entre eux pour « remplir » l’enveloppe extérieure de chacun. Ce partage constitue un état d’énergie plus faible pour tous les atomes concernés que s’ils existaient sans que leurs coquilles externes soient remplies.
Il existe deux types de liaisons covalentes : polaires et non polaires. Les liaisons covalentes non polaires se forment entre deux atomes d’un même élément ou entre des éléments différents qui partagent les électrons de manière égale. Par exemple, un atome d’oxygène peut se lier à un autre atome d’oxygène pour remplir leurs coquilles externes. Cette association est non polaire car les électrons seront répartis de manière égale entre chaque atome d’oxygène. Deux liaisons covalentes se forment entre les deux atomes d’oxygène car l’oxygène a besoin de deux électrons partagés pour remplir sa coquille extérieure. Les atomes d’azote formeront trois liaisons covalentes (également appelées triples covalentes) entre deux atomes d’azote car chaque atome d’azote a besoin de trois électrons pour remplir sa coquille la plus externe. Un autre exemple de liaison covalente non polaire se trouve dans la molécule de méthane (CH4). L’atome de carbone possède quatre électrons dans sa coquille la plus externe et a besoin de quatre autres pour la remplir. Il obtient ces quatre électrons de quatre atomes d’hydrogène, chaque atome en fournissant un. Ces éléments partagent tous les électrons de manière égale, créant ainsi quatre liaisons covalentes non polaires (figure 5).
Dans une liaison covalente polaire, les électrons partagés par les atomes passent plus de temps plus près d’un noyau que de l’autre. En raison de la répartition inégale des électrons entre les différents noyaux, une charge légèrement positive (δ+) ou légèrement négative (δ-) se développe. Les liaisons covalentes entre les atomes d’hydrogène et d’oxygène dans l’eau sont des liaisons covalentes polaires. Les électrons partagés passent plus de temps près du noyau d’oxygène, lui conférant une petite charge négative, qu’ils n’en passent près des noyaux d’hydrogène, conférant à ces molécules une petite charge positive.

Figure 5. La molécule d’eau (à gauche) représente une liaison polaire avec une charge légèrement positive sur les atomes d’hydrogène et une charge légèrement négative sur l’oxygène. Le méthane (au milieu) et l’oxygène (à droite) sont des exemples de liaisons non polaires.
Les liaisons hydrogène
Les liaisons ioniques et covalentes sont des liaisons fortes dont la rupture nécessite une énergie considérable. Cependant, toutes les liaisons entre éléments ne sont pas des liaisons ioniques ou covalentes. Des liaisons plus faibles peuvent également se former. Ce sont des attractions qui se produisent entre des charges positives et négatives et dont la rupture ne nécessite pas beaucoup d’énergie. Deux liaisons faibles fréquentes sont les liaisons hydrogène et les interactions de Van der Waals. Ces liaisons donnent naissance aux propriétés uniques de l’eau et aux structures uniques de l’ADN et des protéines.
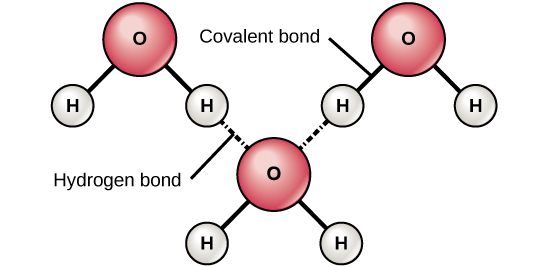
Figure 6. Les liaisons hydrogène se forment entre les charges légèrement positives (δ+) et légèrement négatives (δ-) des molécules covalentes polaires, comme l’eau.
Lorsque des liaisons covalentes polaires contenant un atome d’hydrogène se forment, l’atome d’hydrogène dans cette liaison a une charge légèrement positive. Cela est dû au fait que l’électron partagé est tiré plus fortement vers l’autre élément et loin du noyau d’hydrogène. Comme l’atome d’hydrogène est légèrement positif (δ+), il sera attiré par les charges partielles négatives voisines (δ-). Lorsque cela se produit, une faible interaction se produit entre la charge δ+ de l’atome d’hydrogène d’une molécule et la charge δ- de l’autre molécule. Cette interaction est appelée une liaison hydrogène. Ce type de liaison est courant ; par exemple, la nature liquide de l’eau est causée par les liaisons hydrogène entre les molécules d’eau (figure 6). Les liaisons hydrogène confèrent à l’eau les propriétés uniques qui permettent la vie. Sans les liaisons hydrogène, l’eau serait un gaz plutôt qu’un liquide à température ambiante.
Les liaisons hydrogène peuvent se former entre différentes molécules et elles ne doivent pas toujours inclure une molécule d’eau. Les atomes d’hydrogène dans les liaisons polaires au sein de n’importe quelle molécule peuvent former des liaisons avec d’autres molécules adjacentes. Par exemple, les liaisons hydrogène maintiennent ensemble deux longs brins d’ADN pour donner à la molécule d’ADN sa structure caractéristique à double brin. Les liaisons hydrogène sont également responsables d’une partie de la structure tridimensionnelle des protéines.
interactions de van der Waals
Comme les liaisons hydrogène, les interactions de van der Waals sont de faibles attractions ou interactions entre molécules. Elles se produisent entre des atomes polaires, liés de manière covalente, dans différentes molécules. Certaines de ces attractions faibles sont causées par des charges partielles temporaires formées lorsque les électrons se déplacent autour d’un noyau. Ces interactions faibles entre les molécules sont importantes dans les systèmes biologiques.
Résumé de la section
La matière est tout ce qui occupe l’espace et possède une masse. Elle est constituée d’atomes de différents éléments. Les 92 éléments présents à l’état naturel ont tous des qualités uniques qui leur permettent de se combiner de diverses manières pour créer des composés ou des molécules. Les atomes, qui sont constitués de protons, de neutrons et d’électrons, sont les plus petites unités d’un élément qui conservent toutes les propriétés de cet élément. Les électrons peuvent être donnés ou partagés entre les atomes pour créer des liaisons, notamment des liaisons ioniques, covalentes et hydrogène, ainsi que des interactions de van der Waals.
Exercices d’autocontrôle supplémentaires
1. Regardez la figure 2 : combien de neutrons ont respectivement le (K) potassium-39 et le potassium-40 ?
2. Pourquoi les liaisons hydrogène et les interactions de van der Waals sont-elles nécessaires aux cellules ?
Réponses
1. Le potassium-39 possède vingt neutrons. Le potassium-40 a vingt et un neutrons.
2. Les liaisons hydrogène et les interactions de van der Waals forment des associations faibles entre différentes molécules. Elles fournissent la structure et la forme nécessaires aux protéines et à l’ADN à l’intérieur des cellules pour qu’ils fonctionnent correctement. Les liaisons hydrogène donnent également à l’eau ses propriétés uniques, qui sont nécessaires à la vie.
.