N2O (dikväveoxid) är en kväveoxid och kallas skrattgas. I den här handledningen kommer vi att lära oss följande om lustgas.
- Hur man ritar Lewisstrukturen för N2O
- Rita resonansstrukturer efter Lewisstrukturen
- Oxidationstal för kväve- och syreatomer.
Om du redan känner till lewisstrukturen för N2O kan du hoppa över den första delen av denna handledning och gå direkt till lewisstrukturen.
N2O:s lewisstruktur
Det finns flera steg att följa för att rita N2O:s lewisstruktur. Alla dessa steg förklaras i detalj i den här handledningen och en nybörjare kan lära sig grunderna för att rita lewisstrukturen.
Antal elektroner i valensskalet
Först bör vi veta hur många elektroner i valensskalet hos syre- och kväveatomerna som kommer att tillföras för att bilda molekylen.
Antal elektroner i kväveatomens valensskal = 5
Antal kväveatomer i N2O-molekylen = 2
Antal elektroner som ges av kväveatomerna = 5*2 = 10
Antal elektroner i syreatomens valensskal = 6
Total elektroner som ges av alla. atomer = 10 + 6 = 16
Antal totala elektroner som stöter bort paren (summan av σ + π + lone par i valansskalet) = 16/2 = 8
Centrumatom i N2O
Stuellt sett har kväveatomen störst möjlighet att vara centrumatom än syreatomen eftersom kväve kan uppvisa en högre valans än syre.
Så är en av kväveatomerna placerad som centrumatom och andra atomer är placerade runt den. Nu kan vi föreställa oss en skiss för N2O och den är figurerad nedan.
Laddningar på atomer
När en molekyl ritas ska vi vara noga med att alltid minimera laddningarna på atomerna eftersom när atomernas laddningar är låga är stabiliteten hos den molekylen stor.
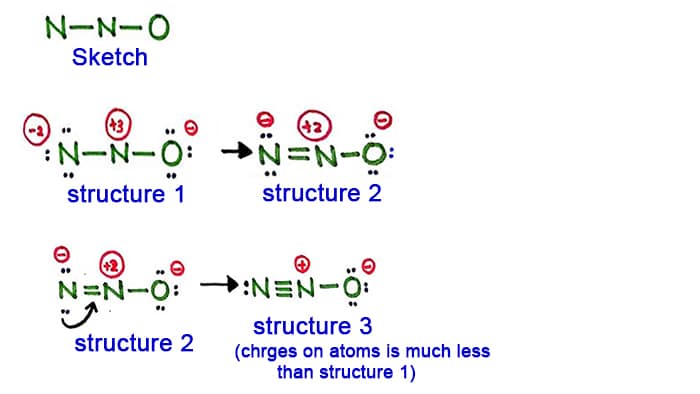
Struktur 1
Se struktur 1, det finns positiva och laddningar på varje atom i N2O-molekylen. Så denna struktur verkar inte vara en stabil struktur. Därför bör vi försöka rita en annan struktur genom att ändra struktur 1.
Skapa en ny bindning genom att omvandla ett ensamt par i kväveatomen i sidan (inte i den centrala kväveatomen).
Struktur 2
Ett ensamt par i kväveatomen (vänster sida) orsakas nu till att bilda en bindning mellan kväveatomer. Nu finns det alltså en dubbelbindning mellan kväveatomerna. Därmed minskar tätheten av laddningar på atomerna.
Men, som ni ser, finns det fortfarande laddningar på atomerna. Så låt oss prova en annan struktur för N2O för att sänka laddningarna om det är möjligt.
Struktur 3
Ett annat långt par i kväveatomen (vänster sida) orsakas nu att bilda en bindning mellan kväveatomer. Nu finns det alltså en trippelbindning mellan kväveatomer.
I denna struktur minskar dessutom laddningarna på atomerna ytterligare. Nu har den centrala kväveatomen endast +1 laddning och syreatomen har -1 laddning.
Struktur 3 är den bästa (mest stabila) strukturen vi kan rita för N2O. Dess centrumatom innehåller, runt den,
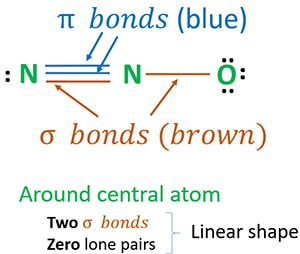
- två sigma (σ)-bindningar
- noll ensamma par
Form av N2O-molekylen runt centrumatomen
N2O-molekylen innehåller två kväveatomer och en syreatom. Först bör vi försöka rita den mest stabila Lewisstrukturen av N2O för att bestämma N2O-molekylens form.
Antalet ensamstående par och antalet σ-bindningar runt centrumatomen är viktigt för att hitta formen på en molekyl.
På grund av två sigma-bindningar och noll ensamma par runt centrumatomen (kväve) är N2O-molekylens form linjär.
Vi kan rita N2O-resonansstrukturer för att identifiera den mest stabila strukturen hos N2O. Oxidationstal för kväve i N2O bestäms utifrån de mest stabila strukturerna. Slutligen bygger vi upp N2O-molekylens form.
N2O-resonansstrukturer
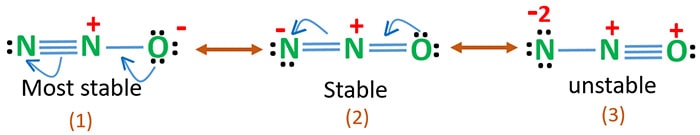
Syrets elektronegativitet är högre än kväve. Detta innebär att en negativ laddning på en syreatom är stabilare än en negativ laddning på en kväveatom. Annars kan vi säga att syre gillar elektroner mer än kväve.
Struktur 3 är den mest instabila resonansen hos N2O eftersom det finns en positiv laddning på syreatomen.
Struktur 2 har en viss stabilitet.
Struktur 1 är den mest stabila resonansen eftersom syret innehar den negativa laddningen.
Oxidationstillstånd, nummer för N2O
Vi kan beräkna oxidationstillstånd för N2O för den mest stabila resonansstrukturen.
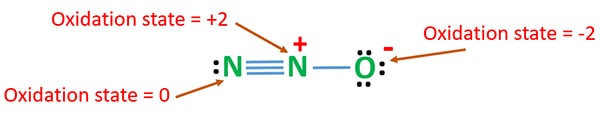
Oxidationstillstånd för N2O
Oxidationsnummer för kväve i N2O är +1. Men i den verkliga situationen befinner sig en kväveatom i oxidationstalet +2 och den andra kväveatomen i oxidationstalet 0. Oxidationstalet för syre är -2.
Oxidationstal från ekvation
Vi vet att i de flesta fall är syrets oxidationstal -2. Det finns två kväveatomer i N2O. Ta kväveoxidationstalet x. N2O-molekylens totala laddning är 0.
En del av oxidationstalen för varje grundämne i molekylen bör vara lika med noll.