Termodynamika jest gałęzią fizyki, która zajmuje się energią i pracą systemu.Termodynamika zajmuje się odpowiedzią systemu w dużej skali, którą możemy obserwować i mierzyć w eksperymentach.Jako aerodynamicy, jesteśmy najbardziej zainteresowani termodynamiką systemów napędowych i przepływów z dużymi prędkościami.Aby zrozumieć jak działa system napędowy, musimy przestudiować podstawy termodynamiki gazów.
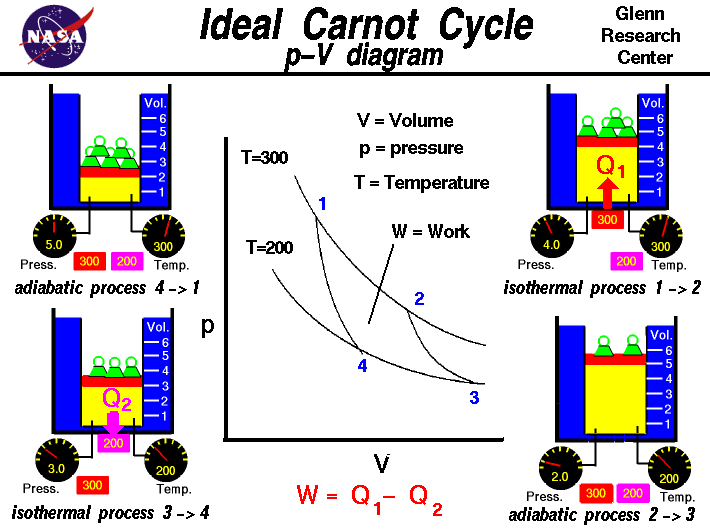
Gazy mają różne właściwości, które możemy obserwować za pomocą naszych zmysłów, w tym ciśnienie gazu p, temperaturę T, masę i objętość V, która zawiera gaz.Uważna, naukowa obserwacja pozwoliła ustalić, że te zmienne są powiązane ze sobą, a wartości tych właściwości określają stan gazu.Proces termodynamiczny, taki jak podgrzewanie lub sprężanie gazu, zmienia wartości zmiennych stanu w sposób, który jest opisany przez prawa termodynamiki. Praca wykonywana przez gaz i ciepło przekazywane gazowi zależą od stanu początkowego i końcowego gazu oraz od procesu użytego do zmiany stanu. Możliwe jest przeprowadzenie serii procesów, w których stan zmienia się podczas każdego procesu, ale gaz ostatecznie powraca do stanu początkowego. Taka seria procesów nazywana jest cyklem i stanowi podstawę do zrozumienia działania silników. Cykl Carnota jest jednym z podstawowych cykli termodynamicznych i został opisany na tej stronie internetowej. Użyjemy diagramu ap-V do przedstawienia różnych procesów w cyklu Carnota. Cykl rozpoczyna się od gazu, oznaczonego na rysunku kolorem żółtym, który jest zamknięty w cylindrze oznaczonym kolorem niebieskim. Objętość cylindra jest zmieniana przez poruszający się czerwony tłok, a ciśnienie jest zmieniane przez umieszczanie na tłoku ciężarków. Mamy dwa źródła ciepła; czerwone o nominalnej temperaturze 300 stopni, a fioletowe o temperaturze 200 stopni. Początkowo gaz znajduje się w stanie 1 przy wysokiej temperaturze, wysokim ciśnieniu i małej objętości.
- Pierwszym procesem wykonywanym na gazie jest rozprężanie izotermiczne. Źródło ciepła o temperaturze 300 stopni wchodzi w kontakt z cylindrem, a masa jest usuwana, co powoduje obniżenie ciśnienia w gazie. Temperatura pozostaje stała, ale objętość wzrasta. Podczas procesu przechodzenia od stanu 1 do stanu 2 ciepło jest przekazywane ze źródła do gazu w celu utrzymania temperatury. Zwrócimy uwagę na przekazywanie ciepła przez Q1 do gazu.
- Drugim procesem zachodzącym w gazie jest rozprężanie adiabatyczne. Podczas procesu adiabatycznego do gazu nie jest przekazywane ciepło. Masa jest usuwana, co powoduje obniżenie ciśnienia w gazie. Temperatura maleje, a objętość rośnie, ponieważ gaz rozszerza się, aby wypełnić objętość. Podczas procesu od stanu 2 do stanu 3 ciepło nie jest przekazywane.
- Trzecim procesem wykonywanym na gazie jest kompresja izotermiczna. Źródło ciepła o temperaturze 200 stopni wchodzi w kontakt z cylindrem i dodawany jest ciężar, co powoduje wzrost ciśnienia w gazie. Temperatura pozostaje stała, ale objętość maleje. Podczas procesu od stanu 3 do stanu 4 ciepło jest przekazywane z gazu do źródła ciepła, aby utrzymać temperaturę. Zwrócimy uwagę na oddawanie ciepła przez Q2 od gazu.
- Czwartym procesem wykonywanym na gazie jest sprężanie adiabatyczne. Dodawana jest masa, która podnosi ciśnienie w gazie. Temperatura wzrasta, a objętość maleje, ponieważ gaz jest sprężany. Podczas procesu od stanu 4 do stanu 1 nie jest przekazywane ciepło.
Po zakończeniu czwartego procesu stan gazu powrócił do stanu początkowego, a cykl można powtarzać dowolną ilość razy. W trakcie cyklu gaz wykonał pracę W, a ilość pracy jest równa powierzchni wyznaczonej przez krzywe procesu.Z pierwszego prawa termodynamiki wynika, że ilość wykonanej pracy jest równa ciepłu netto przekazanemu w trakcie procesu:
W = Q1 – Q2
Cykl Carnota działa jak silnik, zamieniając ciepło przekazane gazowi w trakcie procesów na pracę użyteczną. Podobny Cykl Braytona wyjaśnia, jak działa silnik turbinowy, a Cykl Otta wyjaśnia, jak działa silnik spalinowy.
Działania:
Zwiedzanie z przewodnikiem
Nawigacja..
![]()
Strona główna Przewodnika dla początkujących