Thermodynamica is een tak van de natuurkunde die zich bezighoudt met de energie en arbeid van een systeem.Thermodynamica houdt zich bezig met de grootschalige reactie van een systeem die we kunnen waarnemen en meten in experimenten.Als aërodynamici zijn we het meest geïnteresseerd in de thermodynamica van voortstuwingssystemen en stromingen met hoge snelheid.Om te begrijpen hoe een voortstuwingssysteem werkt, moeten we de basisthermodynamica van gassen bestuderen.
Gassen hebben verschillende eigenschappen die we met onze zintuigen kunnen waarnemen, waaronder de gasdruk p, de temperatuur T, de massa en het volume V dat het gas bevat.Zorgvuldige, wetenschappelijke observatie heeft vastgesteld dat deze variabelen met elkaar in verband staan, en de waarden van deze eigenschappen bepalen de toestand van het gas.Een thermodynamisch proces, zoals het verhitten of samendrukken van het gas, verandert de waarden van de toestandsvariabelen op een wijze die wordt beschreven door de wetten van de thermodynamica. De door een gas verrichte arbeid en de aan een gas overgedragen warmte hangen af van de begin- en eindtoestand van het gas en van het proces dat wordt toegepast om de toestand te wijzigen.
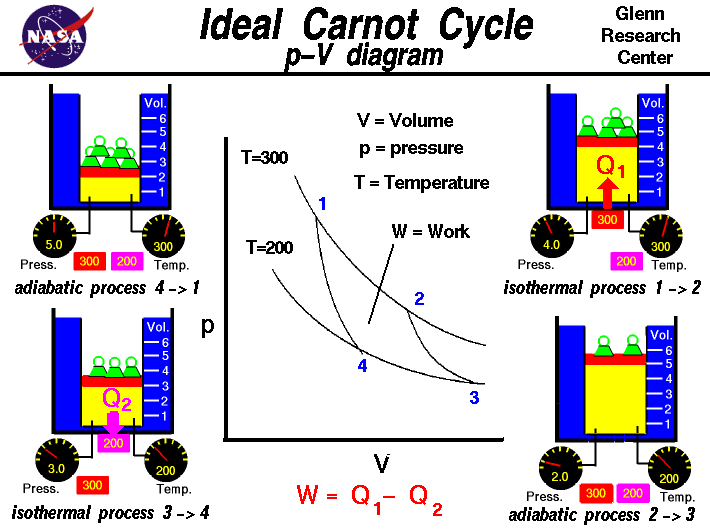
Het is mogelijk een reeks processen uit te voeren, waarbij de toestand tijdens elk proces wordt gewijzigd, maar het gas uiteindelijk terugkeert naar zijn oorspronkelijke toestand. Een dergelijke reeks processen wordt een cyclus genoemd en vormt de basis voor het begrip van motoren. De Carnot-cyclus is een van de fundamentele thermodynamische cycli en wordt op deze webpagina beschreven. We zullen gebruik maken van een V-diagram om de verschillende processen in de Carnot-cyclus in kaart te brengen. De cyclus begint met een gas, geel gekleurd op de figuur, dat is opgesloten in een cilinder, blauw gekleurd. Het volume van de cilinder wordt veranderd door een bewegende rode zuiger, en de druk wordt veranderd door gewichten op de zuiger te plaatsen. We hebben twee warmtebronnen: de rode is nominaal 300 graden en de paarse is 200 graden. Aanvankelijk is het gas in toestand 1 bij hoge temperatuur, hoge druk en laag volume. De 300 graden warmtebron wordt in contact gebracht met de cilinder, en het gewicht wordt verwijderd, waardoor de druk in het gas daalt. De temperatuur blijft constant, maar het volume neemt toe. Tijdens het proces van toestand 1 naar toestand 2 wordt warmte overgedragen van de bron naar het gas om de temperatuur te handhaven. We zullen de warmteoverdracht door Q1 naar het gas noteren.
Aan het eind van het vierde proces is de toestand van het gas teruggekeerd naar de oorspronkelijke toestand en kan de cyclus zo vaak als men wil worden herhaald. Tijdens de cyclus heeft het gas arbeid W geproduceerd, en de hoeveelheid arbeid is gelijk aan het oppervlak dat door de proceskrommen wordt omsloten.Volgens de eerste wet van de thermodynamica is de hoeveelheid geproduceerde arbeid gelijk aan de nettowarmte die tijdens het proces is overgedragen:
W = Q1 – Q2
De Carnot-cyclus heeft gefunctioneerd als een motor, waarbij de warmte die tijdens de processen aan het gas is overgedragen, is omgezet in nuttige arbeid. Een soortgelijke Brayton-cyclus laat zien hoe een gasturbinemotor werkt, en een Otto-cyclus laat zien hoe een verbrandingsmotor werkt.
Activiteiten:
Rondleidingen
Navigatie..
![]()
Beginner’s Guide Home Page