Die Thermodynamik ist ein Teilgebiet der Physik, das sich mit der Energie und der Arbeit eines Systems befasst.Die Thermodynamik befasst sich mit dem großräumigen Verhalten eines Systems, das wir in Experimenten beobachten und messen können.Als Aerodynamiker sind wir am meisten an der Thermodynamik von Antriebssystemen und Hochgeschwindigkeitsströmungen interessiert.Um zu verstehen, wie ein Antriebssystem funktioniert, müssen wir die grundlegende Thermodynamik von Gasen studieren.
Gase haben verschiedene Eigenschaften, die wir mit unseren Sinnen beobachten können, einschließlich des Gasdrucks p, der Temperatur T, der Masse und des Volumens V, in dem sich das Gas befindet.Durch sorgfältige wissenschaftliche Beobachtung wurde festgestellt, dass diese Variablen miteinander in Beziehung stehen, und die Werte dieser Eigenschaften bestimmen den Zustand des Gases.Ein thermodynamischer Prozess, wie das Erhitzen oder Komprimieren des Gases, ändert die Werte der Zustandsvariablen auf eine Weise, die durch die Gesetze der Thermodynamik beschrieben wird. Die von einem Gas verrichtete Arbeit und die auf ein Gas übertragene Wärme hängen vom Anfangs- und Endzustand des Gases und von dem Prozess ab, der zur Änderung des Zustands verwendet wird.
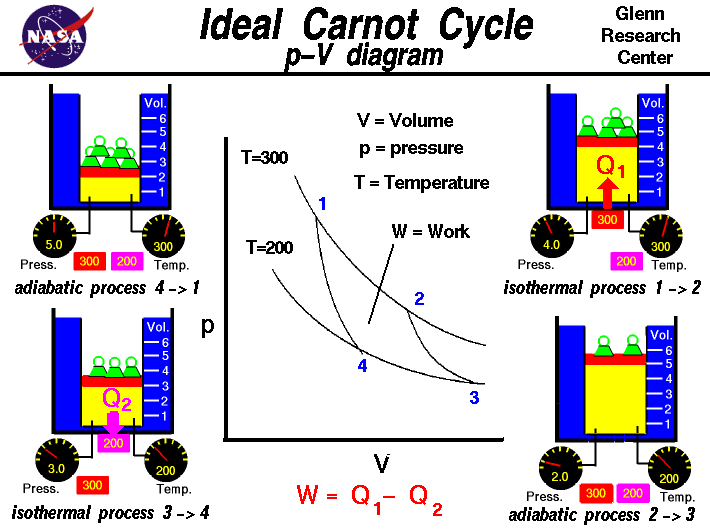
Es ist möglich, eine Reihe von Prozessen durchzuführen, bei denen der Zustand während jedes Prozesses geändert wird, das Gas aber schließlich in seinen ursprünglichen Zustand zurückkehrt. Eine solche Reihe von Prozessen wird als Zyklus bezeichnet und bildet die Grundlage für das Verständnis von Kraftwerken. Der Carnot-Zyklus ist einer der grundlegenden thermodynamischen Zyklen und wird auf dieser Webseite beschrieben. Wir werden ein V-Diagramm verwenden, um die verschiedenen Prozesse des Carnot-Kreislaufs darzustellen. Der Zyklus beginnt mit einem Gas, das in der Abbildung gelb gefärbt ist und sich in einem blau gefärbten Zylinder befindet. Das Volumen des Zylinders wird durch einen sich bewegenden roten Kolben verändert, und der Druck wird durch das Anbringen von Gewichten auf dem Kolben verändert. Wir haben zwei Wärmequellen; die rote hat eine Nenntemperatur von 300 Grad, die violette eine von 200 Grad. Zu Beginn befindet sich das Gas im Zustand 1 mit hoher Temperatur, hohem Druck und geringem Volumen.
- Der erste Prozess, der mit dem Gas durchgeführt wird, ist eine isothermische Expansion. Die 300-Grad-Wärmequelle wird mit dem Zylinder in Kontakt gebracht, und das Gewicht wird entfernt, wodurch der Druck im Gas sinkt. Die Temperatur bleibt konstant, aber das Volumen nimmt zu. Während des Übergangs von Zustand 1 zu Zustand 2 wird Wärme von der Quelle auf das Gas übertragen, um die Temperatur aufrechtzuerhalten. Wir notieren die Wärmeübertragung durch Q1 in das Gas.
- Der zweite Prozess, der auf das Gas einwirkt, ist eine adiabatische Expansion. Während eines adiabatischen Prozesses wird keine Wärme auf das Gas übertragen. Es wird Gewicht entzogen, wodurch der Druck im Gas sinkt. Die Temperatur sinkt und das Volumen nimmt zu, da sich das Gas ausdehnt, um das Volumen zu füllen. Beim Übergang von Zustand 2 zu Zustand 3 wird keine Wärme übertragen.
- Der dritte Prozess, der mit dem Gas durchgeführt wird, ist eine isothermische Kompression. Die 200-Grad-Wärmequelle wird mit dem Zylinder in Kontakt gebracht, und es wird ein Gewicht hinzugefügt, wodurch sich der Druck im Gas erhöht. Die Temperatur bleibt konstant, aber das Volumen nimmt ab. Während des Übergangs von Zustand 3 zu Zustand 4 wird Wärme vom Gas auf die Wärmequelle übertragen, um die Temperatur aufrechtzuerhalten. Wir notieren die Wärmeübertragung durch Q2 weg vom Gas.
- Der vierte Prozess, der an dem Gas durchgeführt wird, ist eine adiabatische Kompression. Es wird ein Gewicht hinzugefügt, wodurch sich der Druck im Gas erhöht. Die Temperatur steigt und das Volumen nimmt ab, während das Gas komprimiert wird. Während des Prozesses von Zustand 4 zu Zustand 1 wird keine Wärme übertragen.
Am Ende des vierten Prozesses ist der Zustand des Gases wieder in den ursprünglichen Zustand zurückgekehrt und der Zyklus kann beliebig oft wiederholt werden. Nach dem ersten Hauptsatz der Thermodynamik ist die erzeugte Arbeit gleich der während des Prozesses übertragenen Nettowärme:
W = Q1 – Q2
Der Carnot-Kreisprozess hat die Funktion eines Motors, der die während der Prozesse auf das Gas übertragene Wärme in nützliche Arbeit umwandelt. Ein ähnlicherBrayton-Zykluserklärt, wie einTurbinenmotor funktioniert, und einOtto-Zykluserklärt, wie ein Verbrennungsmotor funktioniert.
Aktivitäten:
Führungen
Navigation..
![]()
Anfängerhandbuch Startseite