Ecco il problema della copertura delle “ammine” in Org 2: non c’è narrazione.
A differenza della maggior parte dei capitoli, non inizia con una serie di concetti e poi costruisce una serie di esempi a cui si possono applicare quei concetti.
No. Un tipico capitolo sulle ammine in un libro di testo introduttivo è essenzialmente solo un miscuglio di argomenti apparentemente casuali messi insieme che non si adattano a nessun altro. L’unico filo conduttore è che contengono azoto in qualche modo.
Caso emblematico: il post di oggi sulle ammine a caso riguarda i riarrangiamenti di Hofmann e Curtius.
Che cosa spinge a farlo, vi chiederete? Non c’è una buona risposta. La maggior parte dei corsi li copre ad un certo punto, e devono essere inseriti da qualche parte. Quindi, che diavolo. Perché non ora?
Tabella del contenuto
- I riarrangiamenti di Hofmann e Curtius
- Il meccanismo dei riarrangiamenti di Hofmann e Curtius, Parte prima – Impostazione del riarrangiamento
- Parte seconda: Il passo chiave del riarrangiamento nei riarrangiamenti di Hofmann e Curtius
- Parte terza: Formazione dell’isocianato
- Mettendo insieme i passi
- Il destino dell’isocianato: Formazione di carbammati, ammine e uree
- Sommario: I riarrangiamenti di Hofmann e Curtius
- Note
- (Avanzate) Riferimenti e ulteriori letture
- I riarrangiamenti di Hofmann e Curtius
- Il meccanismo dei riarrangiamenti di Hofmann e Curtius, parte 1: Impostazione del riarrangiamento
- Parte 1: Preludio
- 3. Il passo chiave del riarrangiamento in Hofmann e Curtius
- Formazione dell’isocianato
- Mettere insieme i passi
- Il destino dell’isocianato
- Sommario: I riarrangiamenti di Hofmann e Curtius
- Note
- (Avanzato) Riferimenti e ulteriori letture
I riarrangiamenti di Hofmann e Curtius
I riarrangiamenti di Hofmann e Curtius sono due esempi di un’intera famiglia di reazioni di riarrangiamento che condividono un passo meccanico comune.
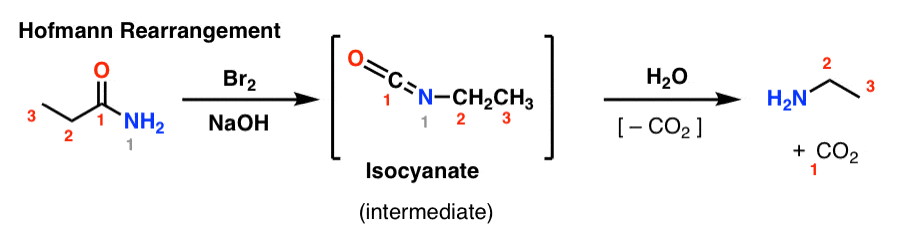
Nel riarrangiamento di Hofmann, un’ammide è trattata con bromo e base (solitamente NaOH o KOH). Al riscaldamento, si forma un isocianato intermedio, che non viene isolato. In presenza di acqua, l’isocianato perde biossido di carbonio (“decarbossilato”) per dare un’ammina.
Il legame chiave che si forma nel Hofmann è il legame C2-N. Notate come il gruppo carbonile (C1) viene perso, formando anidride carbonica (CO2). (nota: questa non è una numerazione IUPAC, solo una numerazione per facilitare la discussione)
Nel riarrangiamento Curtius, un azide acilica è riscaldata, e si forma un isocianato. Nel Curtius, l’isocianato può essere isolato, ma di solito viene ulteriormente trasformato in altre specie come un carbammato, un’urea, o (tramite decarbossilazione, come in Hofmann) in un’ammina (più avanti).
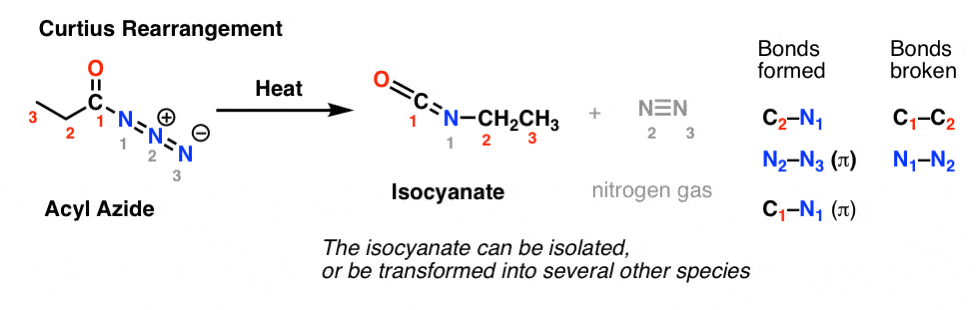
L’osservazione chiave da notare in entrambi i casi è che il legame C1-C2 si è rotto, e si è formato un nuovo legame C2-N.
La domanda è COME?
Il meccanismo dei riarrangiamenti di Hofmann e Curtius, parte 1: Impostazione del riarrangiamento
Ci sono quattro parti importanti nel meccanismo dei riarrangiamenti di Curtius e Hofmann, e noi le attraverseremo tutte.
- Preludio (semplice)
- Il passo chiave della migrazione (difficile, ma meno difficile se ti rendi conto di averne visto una variante in Org 1!)
- Formazione dell’isocianato (semplice)
4. Epilogo: Trasformazioni dell’isocianato
Parte 1: Preludio
- Il riarrangiamento di Hofmann avviene con un’ammide.
- Il riarrangiamento di Curtius avviene con un azide acilica.
Entrambi sono convenientemente preparati da alogenuri acilici attraverso una reazione di addizione-eliminazione. Se ora stai coprendo le ammine, allora le reazioni carboniliche sono probabilmente un territorio familiare. Gli alogenuri acilici possono essere preparati da acidi carbossilici usando un reagente come il cloruro di tionile (SOCl2) o il pentacloruro di fosforo (PCl5).
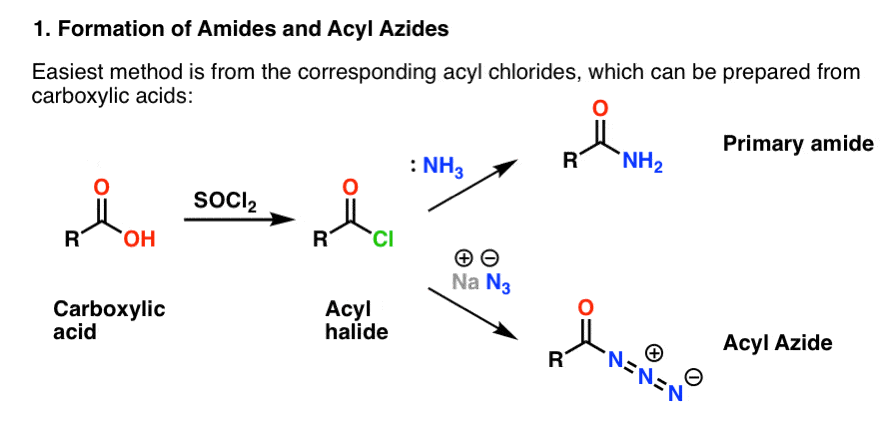
Impostazione di Hofmann
Nel riarrangiamento di Hofmann, l’ammide è trattata con bromo (Br2) e una base come NaOH. Questo provoca la rottura di N-H e la formazione di N-Br, con conseguente installazione di un buon gruppo lasciante sull’azoto. Chiamiamo questo una “N-bromoammide”.
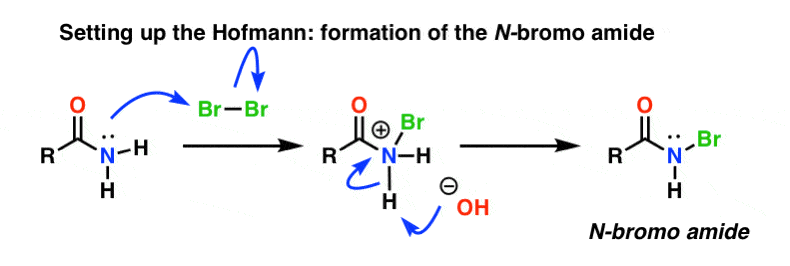
Il Curtius non ha bisogno di “allestimento”, poiché l’azide acilica ha già uno splendido gruppo di partenza incorporato: N2. Questo è il motivo per cui le azidi organiche dovrebbero essere trattate con cura, dato che un trattamento approssimativo può portare a esplosioni.
3. Il passo chiave del riarrangiamento in Hofmann e Curtius
Ora si va al sodo.
Il passo chiave nei riarrangiamenti di Hofmann e Curtius è la migrazione di un atomo di carbonio per spostare un gruppo lasciante su un azoto adiacente.
Questo richiede due frecce curve da disegnare, che sono mostrate nella struttura all’estrema sinistra (sotto).
- Nella prima freccia curva, il legame C-C si rompe, e si forma un nuovo legame C-N.
- Nella seconda freccia curva, il legame N-LG (gruppo lasciante) si rompe.
Tuttavia, non è sempre facile passare direttamente dalla struttura all’estrema sinistra a quella all’estrema destra (che è disegnata in modo carino e ordinato!).
Ogni anno, agli esami, si perdono inutilmente punti per gli studenti che azzeccano le frecce curve ma finiscono per disegnare la struttura sbagliata! Ecco perché incoraggio gli studenti a disegnare prima una “versione brutta”, che sembra una merda ma almeno ha tutti i legami al posto giusto. C’è sempre tempo per ridisegnarla e renderla bella più tardi.
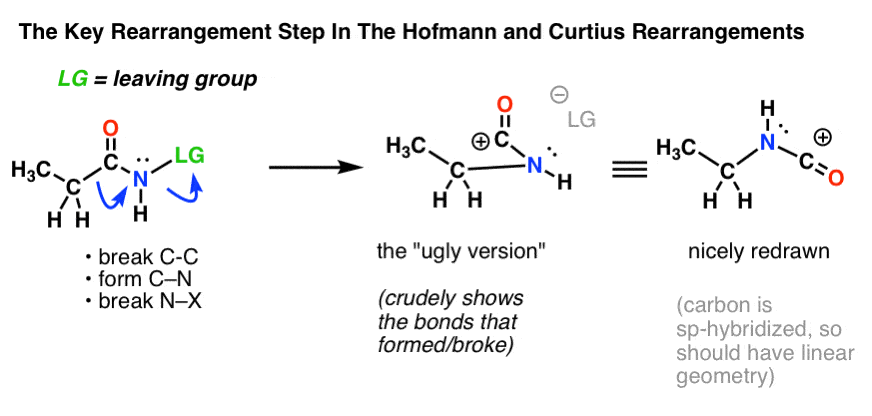
All’inizio questo riarrangiamento probabilmente sembra… strano. Ma in realtà è una reazione che hai già visto prima! (ma in forma mascherata).
Qualcuno ricorda il meccanismo per il passo di “ossidazione” nell’idroborazione-ossidazione?
E’ praticamente la stessa cosa!
Ecco un aggiornamento:
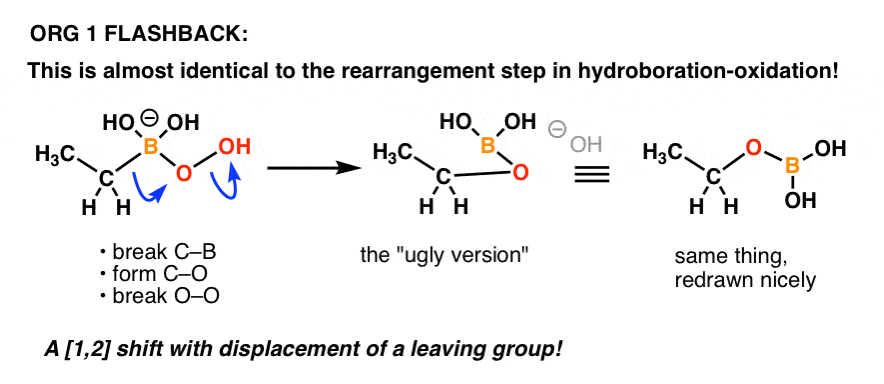
Un altro esempio di come le cose imparate in una parte precedente della chimica organica possono tornare in una parte successiva del corso!
Visitiamo il passo specifico di riarrangiamento nei riarrangiamenti di Hofmann e Curtius con esempi concreti.
Ecco il passo chiave di Hofmann, dove il riscaldamento porta alla rottura di C-C, alla formazione di C-N, e alla rottura di N-Br.
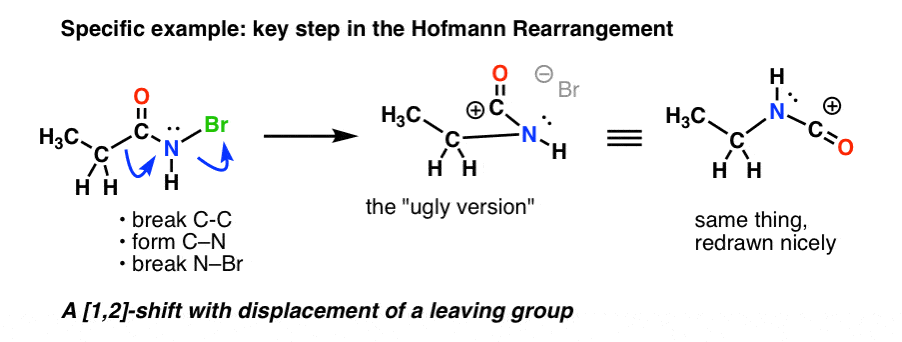
Se seguite tutte le frecce, dovreste ritrovarvi con un carbocation dall’aspetto strano (sopra a destra) di cui ci occuperemo tra un minuto.
Nel Curtius, il riscaldamento dell’azide acilica provoca il riarrangiamento. Il gruppo lasciante è l’azoto gassoso (N2).
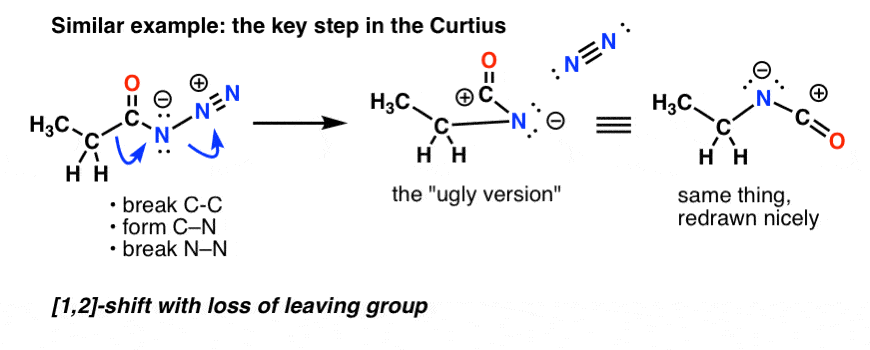
(Una sottile differenza tra il Curtius e l’Hofmann è che non c’è idrogeno attaccato a N nel Curtius, così ci ritroviamo con una carica negativa sull’azoto nella specie riarrangiata.)
Formazione dell’isocianato
Il prossimo passo è passare dalla nostra specie riarrangiata all’isocianato. Per chiunque sia abituato a disegnare forme di risonanza, questo non dovrebbe essere troppo difficile.
(Come discuteremo in seguito, gli studi hanno determinato che la formazione dell’isocianato avviene contemporaneamente alla migrazione. Ma per i nostri scopi didattici, penso che sia utile trattare questa fase in modo isolato. Possiamo mettere tutto insieme in un minuto).
Come forse ricorderete da molto tempo in Org 1, una forma di risonanza con ottetti completi è superiore a una senza (ripasso veloce). Il nostro strano prodotto del riarrangiamento ha un carbocation adiacente a un azoto che contiene una coppia solitaria. Quindi il primo passo è quello di disegnare la formazione di un nuovo legame pi greco C-N. Questa è essenzialmente solo una forma di risonanza.
Il riarrangiamento di Hofmann avviene in presenza di base. Quindi, dopo aver disegnato la forma di risonanza, il passo successivo è la deprotonazione del legame N-H dando l’isocianato neutro.
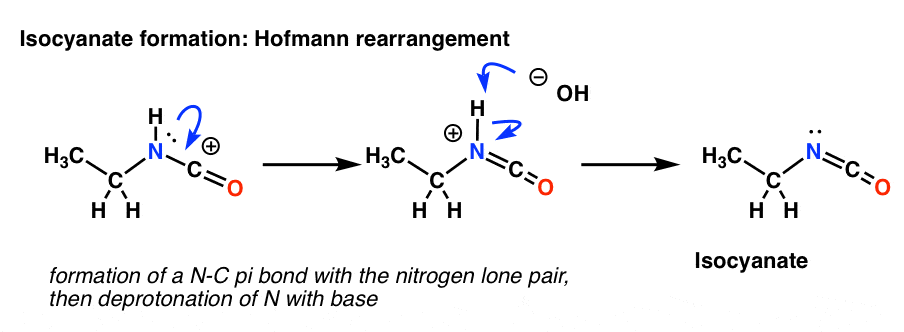
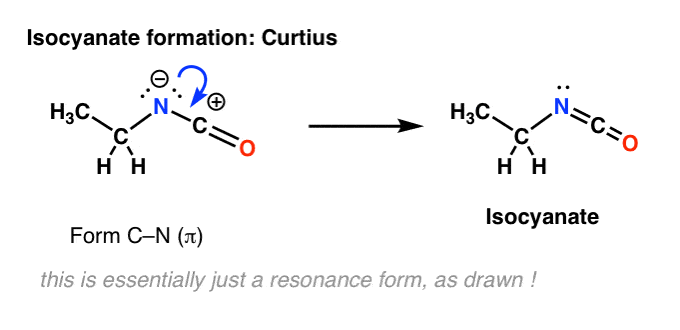
Non c’è idrogeno sull’azoto nel Curtius. Quindi la formazione dell’isocianato si ottiene semplicemente con la donazione di una coppia solitaria dall’azoto al carbocatione. Puoi semplicemente guardarlo come se disegnasse una forma di risonanza.
Mettere insieme i passi
Gli studi sul meccanismo dei riarrangiamenti di Hofmann e Curtius hanno determinato che questi due passi non avvengono in sequenza; in realtà avvengono nello stesso momento! (come facciamo a saperlo? vedi nota 1)
Ovvero, la migrazione avviene contemporaneamente alla formazione dell’isocianato.
Dobbiamo ridisegnare i meccanismi di Hofmann e Curtius per riflettere ciò, incorporando entrambi i passaggi.
Ecco il meccanismo di Hofmann (notare che l’evento di deprotonazione è in realtà separato).
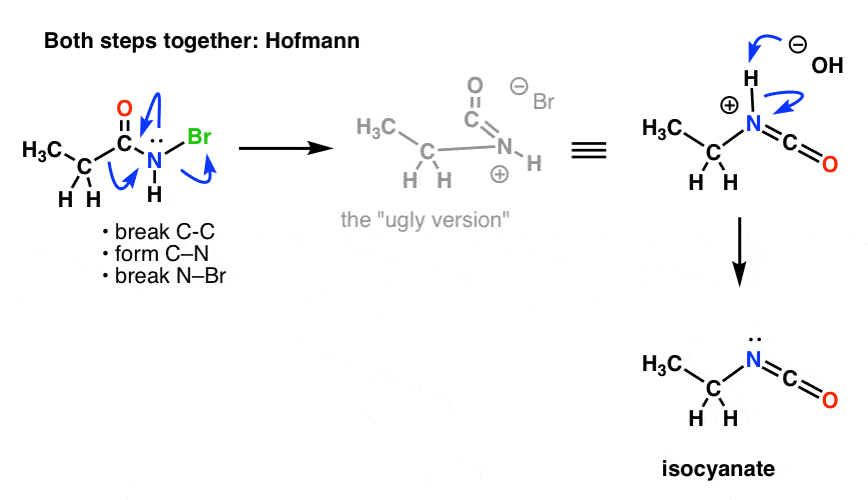
E il Curtius:
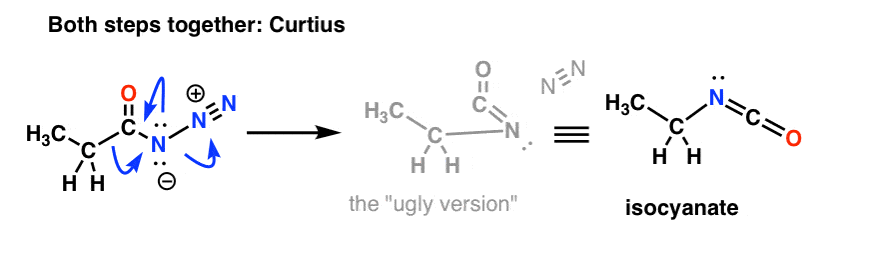
Il destino dell’isocianato
Entrambi Hofmann e Curtius danno origine a un isocianato. Probabilmente non avete mai incontrato gli isocianati prima d’ora. A prima vista, sono specie dall’aspetto piuttosto strano, ma la loro chimica non è così diversa da quella di altre specie carboniliche come esteri, ammidi e alogenuri acilici.
La struttura dell’isocianato assomiglia molto a quella del biossido di carbonio, CO2. Il carbonio è pi-legato a due atomi fortemente elettronegativi. Questo rende il carbonio un eccellente elettrofilo.
Aggiungendo vari nucleofili, gli isocianati possono essere trasformati in altre specie utili.
– Aggiungendo un alcol si forma un carbammato
– Aggiungendo un’ammina si ottiene un’urea
– Aggiungendo acqua si ottiene un acido carbamico, che è instabile. Gli acidi carbammici perdono rapidamente l’anidride carbonica per dare un’ammina.
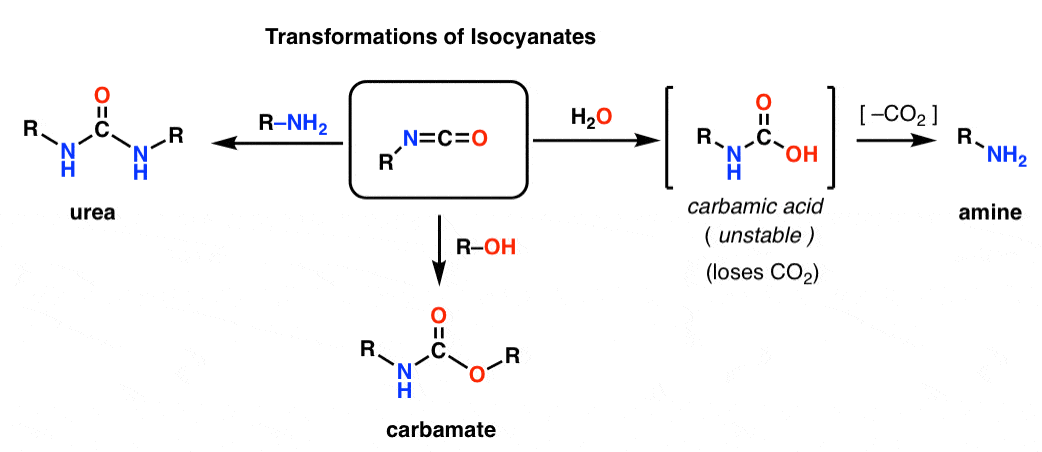
In particolare, la via della decarbossilazione presenta un modo ingegnoso per fare ammine. Abbiamo imparato tonnellate di modi per fare acidi carbossilici, ma non troppi modi per fare ammine (oltre alla sostituzione nucleofila e all’aminazione riduttiva). L’Hofmann è un buon trucco da avere nella tasca posteriore in situazioni in cui nessuna di queste situazioni potrebbe applicarsi – come fare aniline sostituite, per esempio.
Meccanismi? OK, bene. Vedi l’argomento bonus 1.
Sommario: I riarrangiamenti di Hofmann e Curtius
Il meccanismo di questi riarrangiamenti è complicato a prima vista, ma è reso considerevolmente più facile una volta che ti rendi conto che hai già visto una variante della reazione di migrazione (ad es.Cioè nell’idroboro-ossidazione).
Consiglio vivamente di disegnare prima la versione brutta, perché ti aiuterà a concentrarti sul vedere i legami che si formano e si rompono, prima di provare a ridisegnarla in una struttura esteticamente più attraente. Questo vale anche per i riarrangiamenti di Beckmann e Wolff, che hanno un passo simile.(vedi sotto)
Note
Oggetto 1: Isocianati
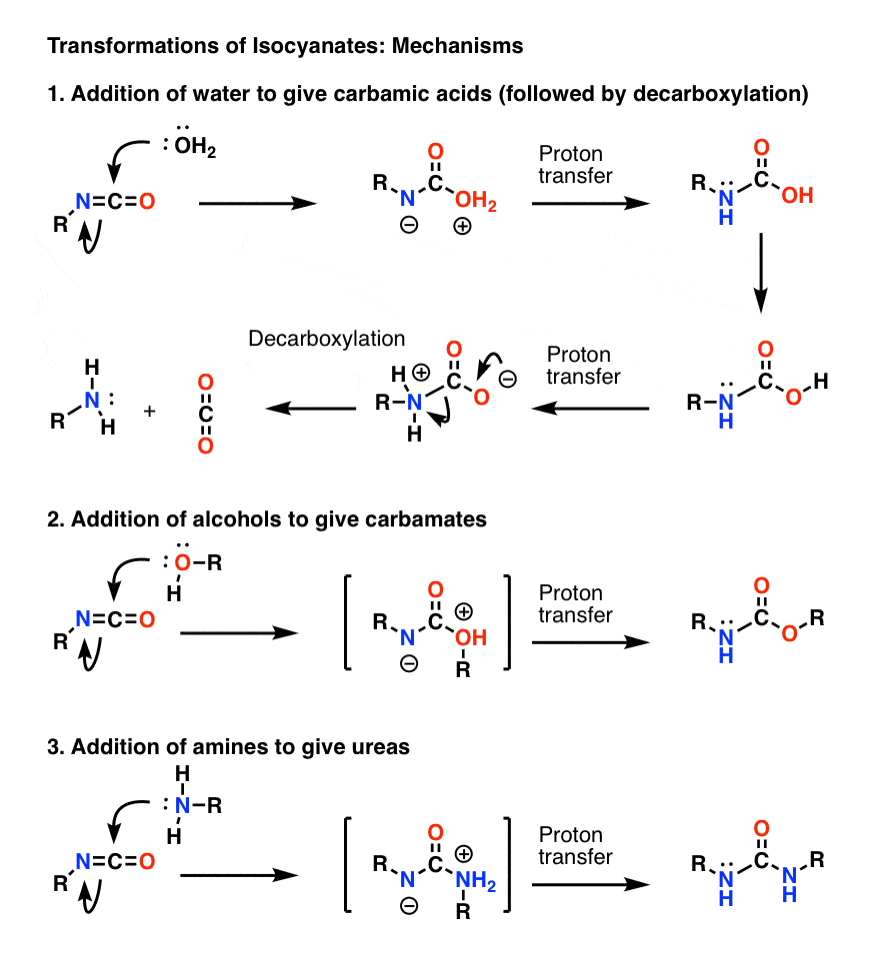
Il meccanismo più importante degli isocianati è l’aggiunta elettrofila (cioè l’aggiunta di un nucleofilo al carbonio centrale, elettrofilo). Nel meccanismo qui sotto ho mostrato il nucleofilo che si aggiunge al carbonio in modo da formare un anione sull’azoto, anche se questa non è probabilmente la migliore forma di risonanza (l’ossigeno è migliore a stabilizzare la carica negativa rispetto all’azoto). Il trasferimento di protoni dall’ossigeno all’azoto dà come risultato una specie neutra. (Ho usato la bacchetta magica del trasferimento di protoni qui, perché è più veloce).
Nota che il passo di decarbossilazione in 1) non ha bisogno di essere preceduto dalla deportazione dell’ossigeno, anche se sicuramente deve verificarsi in modo che l’azoto sia protonato durante il passo (non si vuole formare uno ione ammide fortemente basico, per esempio).
Bonus Topic 2: I riarrangiamenti Beckmann, Wolff, e altri condividono un passo simile
Ma aspetta, c’è di più!
C’è un 1,2-shift con perdita di un gruppo di partenza nel riarrangiamento Beckmann. Il passo chiave è essenzialmente lo stesso che abbiamo visto nel riarrangiamento di Hofmann e Curtius.
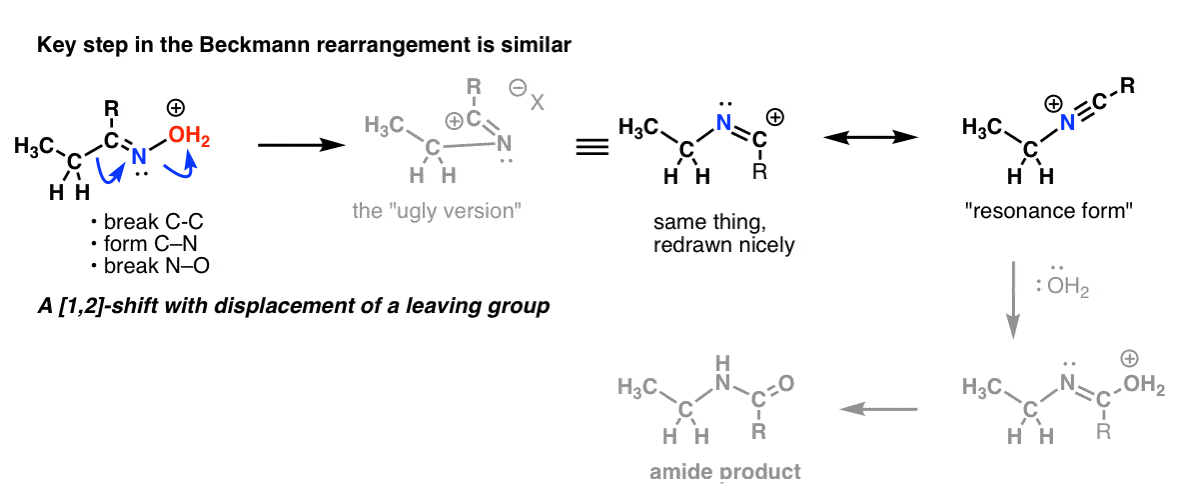
E nel riarrangiamento di Wolff, che è comunemente trattato, potresti anche riconoscere lo stesso passo chiave.
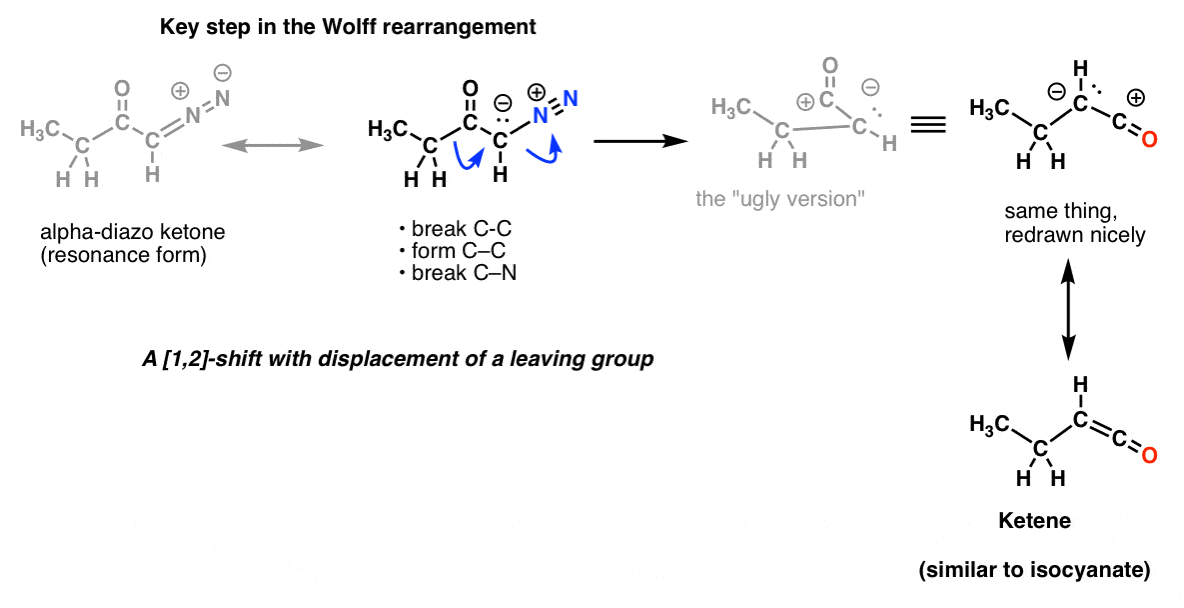
E non è tutto! C’è una reazione chiamata riarrangiamento di Schmidt, che è come il Curtius, ma deriva dall’aggiunta di HN3 a un cloruro di acile (o acido carbossilico). E ce n’è un’altra chiamata riarrangiamento di Lossen che avviene con gli acidi idrossiamici. Nessun premio per chi indovina il passo chiave di questi due processi. E non abbiamo nemmeno menzionato il Baeyer-Villiger, che non coinvolge l’azoto, ma è più o meno lo stesso tipo di processo.
Quando ho imparato il passo di idroborazione-ossidazione in Org 1, molte lune fa, certamente non mi aspettavo che avrei visto lo stesso schema di reazione ripetersi in così tante forme diverse.
La linea di fondo è che ci sono un sacco di reazioni che vanno con nomi diversi che procedono attraverso lo stesso processo meccanico. Questo evidenzia l’importanza di imparare i modelli chiave nella chimica organica, perché di sicuro si ripetono molto.
Nota finale. Concertato, non separato?
Se il Curtius fosse graduale, la perdita di azoto porterebbe a un nitrene. I nitruri subiscono una serie di reazioni interessanti, come l’inserimento in legami C-H (!). Quindi si può progettare un esperimento per testare questo: se si prova il seguente riarrangiamento di Curtius, si potrebbe cercare la prova della formazione di un anello a cinque membri.
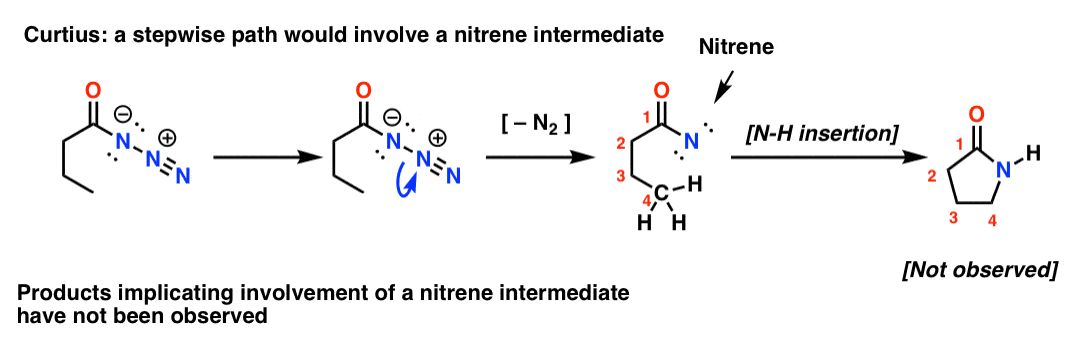
L’assenza di tali prodotti, insieme ad altre prove, indica un meccanismo concertato.
(Avanzato) Riferimenti e ulteriori letture
- Ueber die Einwirkung des Broms in alkalischer Lösung auf Amide
W. Hofmann
Chem. Ber. 1881, 14, 2725-2736
DOI: 10.1002/cber.188101402242
L’articolo originale di A. W. Hofmann (che fu un chimico molto produttivo e il suo nome è attribuito a molte altre trasformazioni) sulla degradazione delle ammidi in ammine primarie. - Un riarrangiamento di Hofmann modificato mite ed efficiente
Xicai Huang, Mehran Seid, and Jeffrey W. Keillor
The Journal of Organic Chemistry 1997, 62 (21), 7495-7496
DOI:10.1021/jo9708553
Questo è un riarrangiamento di Hofmann modificato effettuato in metanolo – in questo caso, l’acido carbammico intermedio può reagire con il solvente metanolo per produrre carbammati di metile in buona resa. - FORMAZIONE DI CARBAMATO DI METILE VIA REAZIONI MODIFICATE DI HOFMANN: METHYL N-(p-METHOXYPHENYL)CARBAMATE
Jeffrey W. Keillor and Xicai Huang
Org. Synth. 2002, 78, 234
DOI: 10.15227/orgsyn.078.0234
Una procedura affidabile e testata indipendentemente per il riarrangiamento di Hofmann modificato nel Rif. #2. - La reazione di Hofmann
Wallis, Everett L.; Lane, John F.
Org. React. 1946, 3, 267-306
DOI: 10.1002/0471264180.or003.07
Una vecchia ma completa (per il suo tempo) recensione sulla reazione di Hofmann (la reazione da ammide ad ammina, da non confondere con le sue altre reazioni). - Note – Un riesame dei limiti della reazione di Hofmann
Ernest Magnien e Richard Baltzly
The Journal of Organic Chemistry 1958, 23 (12), 2029-2032
DOI:10.1021/jo01106a630
Questo è un interessante articolo in cui gli autori hanno tentato di estendere la portata del riarrangiamento di Hofmann oltre quanto descritto nell’articolo originale regolando attentamente le condizioni di reazione. - 20. Hydrazide und Azide organischer Säuren
Curtius, T. I. Abhandlung.
Journal Für Praktische Chemie, 50(1), 275-294. (1894).
DOI:1002/prac.18940500125 - Ueber Stickstoffwasserstoffsäure (Azoimid) N3H.
Curtius, T.
Berichte Der Deutschen Chemischen Gesellschaft, 23(2), 3023-3033.(1890).
DOI:1002/cber.189002302232
Primi articoli di Theodore Curtius che descrivono la reattività di irazidi aciliche e azidi aciliche. - La reazione di Curtius
Smith, P. A. S.
Org. React. 1946, 3, 336
DOI: 10.1002/0471264180.or003.09
Una vecchia ma completa revisione della reazione di Curtius, che include la storia della scoperta di questo riarrangiamento, la portata del substrato, i limiti, il confronto con altre reazioni simili e le procedure sperimentali. - ISOCIANATO DI UNDECILE
F. H. Allen e Alan Bell
Org. Synth. 1944, 24, 94
DOI: 10.15227/orgsyn.024.0094
Una procedura vecchia ma riproducibile e testata per sintetizzare isocianati attraverso il riarrangiamento di Curtius. - Una sintesi totale senza gruppi protettivi di (±)-Dievodiamina
William P. Unsworth, Christiana Kitsiou, e Richard J. K. Taylor
Lettere organiche 2013 15 (13), 3302-3305
DOI:1021/ol4013469
Il primo passo di questa sintesi totale utilizza un riarrangiamento di Curtius per effettuare una ciclizzazione intramolecolare dell’acido carbossilico sostituito dall’indolo. - Metodi e reazioni sintetiche. 121. Preparazione catalizzata da ioduro di zinco di aroyl azidi da cloruri di aroyl e trimetilsilile azide
K. Surya Prakash, Pradeep S. Iyer, Massoud Arvanaghi, and George A. Olah
The Journal of Organic Chemistry 1983 48 (19), 3358-3359
DOI: 10.1021/jo00167a051
Una procedura conveniente per la preparazione di aril azidi aromatiche dal premio Nobel Prof. George A. Olah. Questi possono poi essere usati per i riarrangiamenti di Curtius.