Abstract
Complicazioni come la perdita anastomotica (AL) dopo le procedure colorettali sono associate a una significativa morbilità. La AL subclinica può essere fuorviante a causa del comportamento clinico e quindi pone un dilemma diagnostico. A volte le indagini radiologiche sono un complemento, ma possono essere una deviazione nella progressione diagnostica. Presentiamo un caso di AL subclinica in cui la mancata diagnosi ha portato a esiti sfavorevoli. Nei pazienti suscettibili, i risultati diagnostici devono essere interpretati con cautela sullo sfondo dello scenario clinico. I chirurghi e i radiologi devono essere ben familiarizzati con le diverse presentazioni di complicazioni postoperatorie dopo la chirurgia gastrointestinale inferiore e le loro manifestazioni sull’imaging.
Parole chiave
perdita anastomotica, perdita subclinica, clistere di contrasto
Introduzione
Le procedure colon-rettali comprendono una parte importante della chirurgia generale. Nonostante tutti i progressi e la tecnica chirurgica precisa, le complicazioni, tra cui la perdita anastomotica (AL), causano una significativa morbilità e mortalità. Una perdita locale o confinata si presenta senza sintomi allarmanti, quindi chiamata perdita anastomotica subclinica. La tomografia computerizzata (TC) dell’addome è diventata il metodo di scelta nella valutazione delle complicazioni post-chirurgiche. Mentre la sua superiorità in questi casi non è dimostrata, gli errori umani nella refertazione che portano a risultati inferiori agli standard non sono rari. L’affidamento sull’imaging come strumento diagnostico per sostituire il giudizio clinico (a causa dell’impatto medico-legale), è diventato un problema di preoccupazione.
Presentazione del caso
Un uomo di 82 anni è stato ammesso all’unità medica per letargia insolita. Aveva una resezione anteriore assistita laparoscopica con una ileostomia di copertura per un adenocarcinoma rettale medio sei settimane fa. L’anastomosi è stata eseguita con una cucitrice circolare da 30 mm. Durante la presentazione attuale, ha lamentato un aumento della produzione dello stoma e una stanchezza insolita. L’esame fisico era irrilevante. Gli esami ematologici di routine hanno mostrato un elevato rapporto urea/creatinina e anomalie degli elettroliti. La gestione delle anomalie di volume e degli elettroliti è stata avviata.
In seguito la produzione dallo stoma è diminuita gradualmente e il paziente ha iniziato a lamentare dolore addominale e vomito. Il team chirurgico è stato coinvolto a questo punto della cura. Le radiografie addominali hanno dimostrato anse dilatate dell’intestino tenue e livelli multipli di liquido d’aria. La TAC dell’addome ha mostrato anse intestinali dilatate. L’anastomosi colorettale è stata riportata intatta senza segni di perdite. La diagnosi differenziale era un’ostruzione intestinale adesiva o un ileo secondario ad anomalie elettrolitiche. La decompressione nasogastrica e la rianimazione dei fluidi sono iniziate. Anticipando un recupero ritardato a causa delle aderenze e del precedente intervento chirurgico, è stata avviata la nutrizione parenterale. Inizialmente le caratteristiche ostruttive migliorarono dopo 48 ore con il ritorno della funzione dello stoma.
Tuttavia, alla reintroduzione di fluidi orali chiari, il paziente sviluppò un dolore ricorrente e vomito biliare. Il contrasto idrosolubile è stato somministrato attraverso il tubo nasogastrico (NGT) per ottenere risultati diagnostici e terapeutici. Lo studio ha segnalato un’ostruzione dell’intestino tenue prossimale al sito dell’ileostomia e il radiologo ha consigliato una somministrazione di contrasto attraverso l’ileostomia per conferma. Un catetere di Foley è stato inserito attraverso lo stoma e il paziente è stato inviato al dipartimento di imaging per una scansione ripetuta. Inaspettatamente il referto suggeriva stravasi di contrasto nella cavità peritoneale e nel pneumoperitoneo. Una perforazione al sito dell’ileostomia, forse dovuta al catetere, è stata suggerita come possibile causa.
Considerando la perforazione dell’ileostomia, è stata presa la decisione di una laparotomia di emergenza. Poiché era la sesta settimana dalla procedura primaria, è stato eseguito un clistere con contrasto idrosolubile per controllare l’integrità anastomotica prima di una possibile resezione o inversione dell’ileostomia, se necessario. È stato riportato come anastomosi colorettale intatta con buona distensione rettale. Pooling di contrasto libero nella pelvi è stato assunto come fuoriuscita dalla perforazione ileostomia a istanza precedente (Figura 1 freccia).
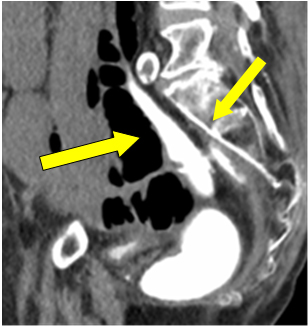
Figura 1: extravasazione di contrasto nella pelvi.
Un re-look midline laparotomia è stata eseguita. Sorprendentemente non è stata visualizzata alcuna perforazione macroscopica. I risultati includevano una moderata quantità di fluidi emosi con poche aderenze fibrinose senza alcuna banda ostruttiva. Il calibro normale, le piccole anse intestinali aderenti sono state notate giù nella pelvi. Queste non sono state disturbate dal chirurgo operante (nessuna perdita anastomotica sull’imaging). L’adesiolisi dell’intestino tenue rimanente è stata fatta e l’ileostomia è stata invertita.
Il paziente è stato trasferito all’unità di alta dipendenza ed è stato osservato attentamente. È rimasto stabile fino al quinto giorno postoperatorio quando è diventato delirante e ha sviluppato una rapida fibrillazione atriale. La ferita della laparotomia è stata notata come deiscente. Data la complessa storia chirurgica, è stato necessario ripetere la scansione CT per la tabella di marcia. Essa ha mostrato un ampio pneumoperitoneo e circa 200 ml di raccolta di rinforzo del bordo nella grondaia paracolica sinistra. Il paziente è stato nuovamente portato in sala operatoria d’urgenza dove è stata eseguita una riesplorazione. All’apertura dell’addome, era presente una peritonite fecolosa con un grande difetto nell’anastomosi colorettale nascosto da piccole aderenze intestinali al sito. L’anastomosi è stata tolta e creato uno stoma sigmoideo finale con chiusura del moncone rettale.
Il paziente ha avuto una convalescenza lenta ed è stato trasferito in una struttura di riabilitazione. Alla fine è stato dimesso a casa dopo aver trascorso 14 giorni in cura transitoria.
Discussione
AL rimane la principale causa di morbilità e mortalità nella chirurgia colorettale. Se non è prontamente identificata e trattata in modo appropriato, il tasso di mortalità può raggiungere il 50%. Uno stoma defunzionante può non garantire l’integrità dell’anastomosi gastrointestinale inferiore.
In letteratura sono stati descritti diversi termini e gradi anastomotici. La gestione clinica dipende dalla sede anatomica, dal grado di perdita e dalla gravità dei sintomi. Le caratteristiche subliniche delle perdite confinate spesso portano a confusione nella diagnosi. L’alto indice di sospetto e la diagnosi precoce sono la chiave per una pronta gestione clinica. In caso contrario, si avrà un deterioramento clinico e un ulteriore onere per l’economia del sistema sanitario.
La TAC è l’indagine più facilmente disponibile per le complicazioni intestinali postoperatorie. Alcune caratteristiche radiologiche di perdita come l’aria peri anastomotica, il fluido o la combinazione di entrambi possono essere raramente presenti. Tuttavia la sua efficacia diagnostica in AL intestinale inferiore non è ben stabilita. L’imaging può essere confuso da interpretare a causa dei cambiamenti post-operatori e di altri fattori confondenti come il pneumoperitoneo residuo, la cicatrizzazione o l’incaglio infiammatorio dei tessuti molli pre sacrali. La dimensione e l’estensione della perdita è un altro fattore importante da tenere a mente.
Il clistere di contrasto non solo dimostra il tasso e l’estensione della perdita, ma aiuta anche nella diagnosi di fenomeni come le raccolte pre sacrali. Il suo ruolo come studio di routine prima dell’inversione dello stoma divergente è ancora discutibile soprattutto in pazienti clinicamente insospettabili. Tuttavia, alcuni studi hanno dimostrato la superiorità del clistere con contrasto idrosolubile nel rilevamento di perdite nelle anastomosi distali in cui entrambe le modalità sono utilizzate.
Vari studi hanno anche riportato tassi falsi negativi del 35%-49% per l’imaging radiologico di sospette perdite anastomotiche.
In situazioni difficili, ci si dovrebbe affidare al giudizio clinico piuttosto che essere diretti dalla sola diagnostica per immagini, poiché una scansione negativa non è una risposta definitiva se il sospetto clinico non viene adeguatamente affrontato.
In questo scenario l’ostruzione intestinale era una falsa pista (probabile ileo in corso dovuto a sepsi subclinica). Durante la prima esplorazione, nessuna perdita macroscopica è stata trovata nell’ileostomia. L’istologia del campione resecato non ha mostrato alcun danno alla mucosa. Tuttavia, una lacerazione sierosa era suggestiva del catetere che attraversa un tratto subseroso prima di entrare nel peritoneo. L’analisi retrospettiva delle immagini è stata condotta con il dipartimento di radiologia. In uno dei film, la punta del catetere è stata trovata passare attraverso il piano sottocutaneo (Figura 2). Questo spiega il contrasto libero nella cavità peritoneale, piuttosto che l’effettiva perforazione del luminare dell’ileostomia. L’ipotesi sull’origine del contrasto ha contribuito all’enigma della diagnosi.
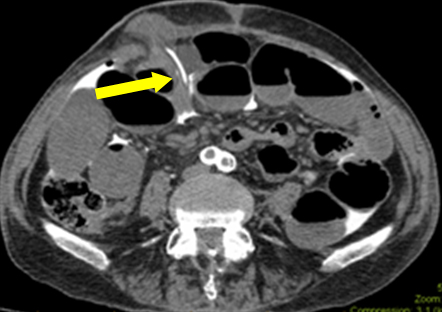
Figura 2: Immagine assiale che mostra la punta del catetere che entra dal piano sottocutaneo nella cavità peritoneale
Anche se banale, ma la perdita di contrasto e il pooling vicino al sito anastomotico sul clistere era un risultato significativo. Sfortunatamente è stato attribuito alla parte di stravasi precedenti attraverso la perforazione dello stoma.
Il paziente era stato operato di recente per un tumore maligno e a causa della cattiva alimentazione e dell’ostruzione intestinale in corso, la guarigione dell’anastomosi era già compromessa. Questo si aggiunge alla suscettibilità di perdite che rafforza ancora una volta la necessità di un alto indice di sospetto in questa situazione clinica.
A causa della precedente resezione anteriore bassa, le piccole anse intestinali erano aderenti nella pelvi confinando l’AL inizialmente minore, quindi mancavano le caratteristiche cliniche classiche. Una volta che l’ileostomia è stata invertita e la diversione fecale non era più presente per proteggere l’integrità anastomotica, la dimensione della perdita è progredita e ha portato al deterioramento con peritonite e deiscenza addominale.
Gli errori diagnostici possono verificarsi in qualsiasi campo della medicina. La cautela deve essere esercitata nell’interpretare i risultati degli studi sullo sfondo dell’acume clinico. Possiamo ridurre tali incidenze con il controllo di routine delle scansioni prima delle procedure e anche la banca dei casi futuri può essere stabilita da un regolare feedback costruttivo per l’imaging che differisce dai risultati operativi.
I pazienti con malattia neoplastica, associati ad altre co-morbidità e a uno stato nutrizionale compromesso, sono altamente suscettibili di una guarigione compromessa di un’anastomosi intestinale. Questi dovrebbero essere considerati vulnerabili per l’anastomosi subclinica soprattutto quando i segni classici di perdita sono assenti. La radiologia postoperatoria dovrebbe essere interpretata con cautela in questo caso e l’intervento chirurgico può servire a una migliore modalità diagnostica e quindi anche terapeutica.
Inoltre, l’apprendimento della radiologia chirurgica è di fondamentale importanza per i chirurghi e un feedback regolare ai radiologi può aiutare a identificare nuove presentazioni di complicazioni postoperatorie dopo la chirurgia colorettale.
- Trencheva K, Morrissey KP, Wells M, Mancuso CA, Lee SW, et al. (2013) Identificazione di importanti predittori di perdite anastomotiche dopo resezione del colon e del retto: studio prospettico su 616 pazienti. Ann Surg 257: 108-113.
- Lim M, Akhtar S, Sasapu K, Harris K, Burke D, et al. (2006) perdite cliniche e subcliniche dopo anastomosi colorettali basse: uno studio clinico e radiologico. Dis Colon Rectum 49: 1611-1619.
- Bruce J, Krukowski ZH, Al-Khairy G, Russell EM, Park KG (2001) Revisione sistematica della definizione e misurazione delle perdite anastomotiche dopo chirurgia gastrointestinale. Br J surg 88: 1157-1168.
- Guillem JG, Cohen AM (1999) Current issues in colorectal cancer surgery. Semin Oncol 26: 505-513.
- Leester B, Asztalos I, Polnyib C (2002) Complicanze settiche dopo resezione rettale anteriore bassa – lo stoma divergente è ancora giustificato? Acta Chir Iugosl 49: 67-71.
- Power N, Atri M, Ryan S, Haddad R, Smith A (2007) Valutazione CT della perdita intestinale anastomotica. Clin Radiol 62: 37-42.
- Nicksa GA, Dring RV, Johnson KH, Sardella WV, Vignati PV, et al. (2007) perdite anastomotiche: qual è il miglior studio di diagnostica per immagini? Dis Colon Rectum 50: 197-203.
- Kalady MF, Mantyh CR, Petrofski J, Ludwig KA (2008) Routine contrast imaging delle anastomosi pelviche basse prima della chiusura dell’ileostomia defunzionante: è necessario? J Gastrointest Surg 12: 1227-1231.
- Khair G, Alhamarneh O, Avery J, Cast J, Gunn J, et al. (2007) Uso di routine del clistere di gastrograffina prima dell’inversione di una ileostomia ad anello. Dig Surg 24: 338-341.
- Akyol AM, McGregor JR, Galloway DJ, George WD (1992) Radiologia di contrasto postoperatoria precoce nella valutazione dell’integrità anastomotica colorettale. Int J Colorectal Dis 7: 141-143.
- Goligher JC, Graham NG, De Dombal FT (1970) Deiscenza anastomotica dopo resezione anteriore del retto e del sigmoide. Br J Surg 57: 109-118.
- Haynes IG, Goldman M, Silverman SH, Alexander-Williams J, Keighley MR (1986) Il clistere di contrasto idrosolubile dopo l’anastomosi del colon. Br J Surg 69: 714-717.
- Khoury W, Ben-Yehuda A, Ben-Haim M, Klausner JM, Szold O (2009) Tomografia computerizzata addominale per la diagnosi di perdite post-operatorie del tratto gastrointestinale inferiore. J Gastrointest Surg 13: 1454-1458.
- Doeksen A, Tanis PJ, Wüst AF, Vrouenraets BC, van Lanschot JJ, et al. (2008) Valutazione radiologica delle anastomosi colorettali. Int J Colorectal Dis 23: 863-868.