Contexte
Le cuivre est l’un des éléments chimiques de base. À l’état presque pur, le cuivre est un métal rouge-orange connu pour sa grande conductivité thermique et électrique. Il est couramment utilisé pour fabriquer une grande variété de produits, notamment des fils électriques, des casseroles et des poêles, des tuyaux et des tubes, des radiateurs automobiles et bien d’autres. Le cuivre est également utilisé comme pigment et agent de conservation pour le papier, la peinture, les textiles et le bois. Il est combiné au zinc pour produire du laiton et à l’étain pour produire du bronze.
Le cuivre a été utilisé pour la première fois il y a 10 000 ans déjà. Un pendentif en cuivre datant d’environ 8700 avant J.-C. a été trouvé dans ce qui est aujourd’hui le nord de l’Irak. Il existe des preuves que vers 6400 avant J.-C., le cuivre était fondu et coulé en objets dans la région connue aujourd’hui sous le nom de Turquie. Vers 4 500 avant J.-C., cette technologie était également pratiquée en Égypte. La plupart du cuivre utilisé avant 4000 avant J.-C. provenait de la découverte aléatoire d’affleurements isolés de cuivre natif ou de météorites qui avaient heurté la Terre. La première mention de l’extraction systématique du minerai de cuivre remonte à environ 3800 avant J.-C., lorsqu’une référence égyptienne décrit des opérations minières dans la péninsule du Sinaï.
Vers 3000 av. J.-C. , de grands dépôts de minerai de cuivre ont été découverts sur l’île de Chypre, dans la mer Méditerranée. Lorsque les Romains ont conquis Chypre, ils ont donné au métal le nom latin aes cyprium, qui a souvent été raccourci en cyprium. Plus tard, ce nom a été corrompu en cuprum, d’où le mot anglais copper et le symbole chimique Cu sont dérivés.
En Amérique du Sud, des objets en cuivre étaient produits le long de la côte nord du Pérou dès 500 av. J.-C., et le développement de la métallurgie du cuivre était bien avancé au moment où l’empire inca est tombé aux mains des soldats espagnols conquérants dans les années 1500.
Aux États-Unis, la première mine de cuivre a été ouverte à Branby, dans le Connecticut, en 1705, suivie d’une autre à Lancaster, en Pennsylvanie, en 1732. Malgré cette production précoce, la plupart du cuivre utilisé aux États-Unis était importé du Chili jusqu’en 1844, lorsque l’exploitation de grands gisements de minerai de cuivre à haute teneur a commencé autour du lac Supérieur. Le développement de techniques de traitement plus efficaces à la fin des années 1800 a permis l’exploitation de minerais de cuivre à plus faible teneur à partir d’énormes mines à ciel ouvert dans l’ouest des États-Unis.
Aujourd’hui, les États-Unis et le Chili sont les deux premiers pays producteurs de cuivre au monde, suivis par la Russie, le Canada et la Chine.
Matières premières
Le cuivre pur est rarement trouvé dans la nature, mais il est généralement combiné avec d’autres produits chimiques sous forme de minerais de cuivre. Il existe environ 15 minerais de cuivre exploités commercialement dans 40 pays du monde. Les plus courants sont les minerais sulfurés, dans lesquels le cuivre est chimiquement lié au soufre. D’autres sont connus sous le nom de minerais d’oxyde, de minerais de carbonate ou de minerais mixtes, selon les produits chimiques présents. De nombreux minerais de cuivre contiennent également des quantités importantes d’or, d’argent, de nickel et d’autres métaux précieux, ainsi que de grandes quantités de matériaux commercialement inutiles. La plupart des minerais de cuivre exploités aux États-Unis ne contiennent qu’environ 1,2 à 1,6 % de cuivre en poids.
Le minerai sulfuré le plus courant est la chalcopyrite, CuFeS 2 , également appelée pyrite de cuivre ou minerai de cuivre jaune. La chalcocite, Cu 2 S, est un autre minerai sulfuré.
La cuprite, ou minerai de cuivre rouge, Cu 2 O, est un minerai d’oxyde. La malachite, ou minerai de cuivre vert, Cu(OH) 2 -CuCO 3 , est un important minerai de carbonate, tout comme l’azurite, ou carbonate de cuivre bleu, Cu(OH) 2 -2CuCO 3 .
D’autres minerais comprennent la tennantite, la boronite, la chrysocolle et l’atacamite.
En plus des minerais eux-mêmes, plusieurs autres produits chimiques sont souvent utilisés pour traiter et raffiner le cuivre. Il s’agit notamment de l’acide sulfurique, de l’oxygène, du fer, de la silice et de divers composés organiques, selon le procédé utilisé.
Le processus de fabrication
Le processus d’extraction du cuivre à partir du minerai de cuivre varie en fonction du type de minerai et de la pureté souhaitée du produit final. Chaque procédé comprend plusieurs étapes au cours desquelles les matières indésirables sont éliminées physiquement ou chimiquement, et la concentration de cuivre est progressivement augmentée. Certaines de ces étapes sont réalisées sur le site même de la mine, tandis que d’autres peuvent être réalisées dans des installations distinctes.
Voici les étapes utilisées pour traiter les minerais sulfurés que l’on trouve couramment dans l’ouest des États-Unis.
Exploitation minière
- 1 La plupart des minerais sulfurés sont extraits d’immenses mines à ciel ouvert par forage et dynamitage à l’aide d’explosifs. Dans ce type d’exploitation, le matériau situé au-dessus du minerai, appelé les morts-terrains, est d’abord enlevé pour exposer le gisement de minerai enfoui. Cela produit une mine à ciel ouvert qui peut atteindre un kilomètre ou plus de large. Une route permettant l’accès des équipements descend en spirale les pentes intérieures de la fosse.
- 2 Le minerai exposé est ramassé par de grandes pelles mécaniques capables de charger 500-900 pieds cubes (15-25 mètres cubes) en une seule bouchée. Le minerai est chargé dans des camions bennes géants, appelés haul trucks, et est transporté vers le haut et hors de la fosse.
Concentration
Le minerai de cuivre contient généralement une grande quantité de saleté, d’argile et une variété de minéraux non cuprifères. La première étape consiste à éliminer une partie de ces déchets. Ce processus s’appelle la concentration et se fait généralement par la méthode de flottation.
- 3 Le minerai est broyé dans une série de concasseurs à cône. Un concasseur à cône est constitué d’un cône de broyage intérieur qui tourne sur un axe vertical excentrique à l’intérieur d’un cône extérieur fixe. Lorsque le minerai est introduit dans la partie supérieure du concasseur, il est pressé entre les deux cônes et brisé en plus petits morceaux.
- 4 Le minerai concassé est ensuite broyé encore plus petit par une série de broyeurs. D’abord, il est mélangé à de l’eau et placé dans un broyeur à barres, qui consiste en un grand récipient cylindrique rempli de nombreuses petites longueurs de barres d’acier. Lorsque le cylindre tourne sur son axe horizontal, les tiges d’acier tombent et brisent le minerai en morceaux d’environ 3 mm de diamètre. Le mélange de minerai et d’eau est ensuite fragmenté dans deux broyeurs à boulets, qui ressemblent à un broyeur à barres, à l’exception des boules d’acier utilisées à la place des barres. La boue de minerai finement broyé qui sort du dernier broyeur à boulets contient des particules d’environ 0,01 in (0,25 mm) de diamètre.
- 5 La boue est mélangée à divers réactifs chimiques, qui enrobent les particules de cuivre. Un liquide, appelé moussant, est également ajouté. L’huile de pin ou l’alcool à longue chaîne sont souvent utilisés comme moussants. Ce mélange est pompé dans des réservoirs rectangulaires, appelés cellules de flottation, où de l’air est injecté dans la boue par le fond des réservoirs. Les réactifs chimiques font que les particules de cuivre s’accrochent aux bulles lorsqu’elles remontent à la surface. Le moussant forme une épaisse couche de bulles, qui déborde des cuves et est recueillie dans des auges. On laisse les bulles se condenser et l’eau est évacuée. Le mélange obtenu, appelé concentré de cuivre, contient environ 25 à 35 % de cuivre, ainsi que divers sulfures de cuivre et de fer, et de plus petites concentrations d’or, d’argent et d’autres matériaux. Les matériaux restants dans le réservoir sont appelés gangue ou résidus. Ils sont pompés dans des bassins de décantation et on les laisse sécher.
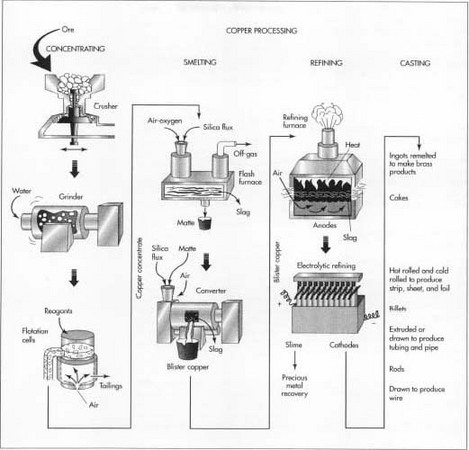
Fusion
Une fois que les déchets ont été physiquement retirés du minerai, le concentré de cuivre restant doit subir plusieurs réactions chimiques pour éliminer le fer et le soufre. Ce processus s’appelle la fusion et implique traditionnellement deux fours, comme décrit ci-dessous. Certaines usines modernes utilisent un seul four, qui combine les deux opérations.
- 6 Le concentré de cuivre est introduit dans un four avec un matériau de silice, appelé flux. La plupart des fonderies de cuivre utilisent des fours flash enrichis en oxygène dans lesquels de l’air préchauffé et enrichi en oxygène est forcé dans le four pour brûler avec le fioul. Le concentré de cuivre et le fondant fondent et s’accumulent au fond du four. Une grande partie du fer contenu dans le concentré se combine chimiquement avec le fondant pour former un laitier, qui est écrémé à la surface du matériau fondu. Une grande partie du soufre contenu dans le concentré se combine avec l’oxygène pour former du dioxyde de soufre, qui est évacué du four sous forme de gaz et est traité dans une usine d’acide pour produire de l’acide sulfurique. Le matériau fondu restant dans le fond du four est appelé la matte. Elle est un mélange de sulfures de cuivre et de sulfures de fer et contient environ 60% de cuivre en poids.
- 7 La matte fondue est extraite du four et versée dans un second four appelé convertisseur. Un flux de silice supplémentaire est ajouté et de l’oxygène est soufflé à travers le matériau fondu. Les réactions chimiques dans le convertisseur sont similaires à celles du four à explosion. Le flux de silice réagit avec le fer restant pour former un laitier, et l’oxygène réagit avec le soufre restant pour former du dioxyde de soufre. Les scories peuvent être réintroduites dans le four éclair pour servir de fondant, et le dioxyde de soufre est traité dans l’usine d’acide. Une fois les scories retirées, une dernière injection d’oxygène élimine tout le soufre sauf une trace. Le matériau fondu résultant est appelé le blister et contient environ 99% de cuivre en poids.
Affinage
Même si le blister de cuivre est un cuivre pur à 99%, il contient encore des niveaux assez élevés de soufre, d’oxygène et d’autres impuretés pour entraver un affinage ultérieur. Pour éliminer ou ajuster les niveaux de ces matériaux, le cuivre blister est d’abord raffiné au feu avant d’être envoyé au processus final d’électro-affinage.
- 8 Le cuivre blister est chauffé dans un four d’affinage, qui est similaire à un convertisseur décrit ci-dessus. De l’air est soufflé dans le blister fondu pour oxyder certaines impuretés. Un flux de carbonate de sodium peut être ajouté pour éliminer les traces d’arsenic et d’antimoine. Un échantillon du matériau fondu est prélevé et un opérateur expérimenté détermine quand les impuretés ont atteint un niveau acceptable. Le cuivre fondu, qui est pur à environ 99,5 %, est ensuite versé dans des moules pour former de grandes anodes électriques, qui servent de bornes positives pour le processus d’électro-affinage.
- 9 Chaque anode de cuivre est placée dans un réservoir individuel, ou cellule, fait de béton polymère. Il peut y avoir jusqu’à 1 250 réservoirs en fonctionnement à un moment donné. Une feuille de cuivre est placée à l’extrémité opposée du réservoir pour servir de cathode, ou borne négative. Les réservoirs sont remplis d’une solution acide de sulfate de cuivre, qui agit comme un conducteur électrique entre l’anode et la cathode. Lorsqu’on fait passer un courant électrique dans chaque réservoir, le cuivre se détache de l’anode et se dépose sur la cathode. La plupart des impuretés restantes tombent de la solution de sulfate de cuivre et forment une boue au fond du réservoir. Après environ 9 à 15 jours, le courant est coupé et les cathodes sont retirées. Les cathodes pèsent maintenant environ 300 lb (136 kg) et sont constituées de cuivre pur à 99,95-99,99 %.
- 10 La boue qui s’accumule au fond de la cuve contient de l’or, de l’argent, du sélénium et du tellure. Elle est collectée et traitée pour récupérer ces métaux précieux.
Coulée
- 11 Après le raffinage, les cathodes de cuivre sont fondues et coulées en lingots, galettes, billettes ou barres selon l’application finale. Les lingots sont des briques rectangulaires ou trapézoïdales, qui sont refondues avec d’autres métaux pour fabriquer des produits en laiton et en bronze. Les gâteaux sont des plaques rectangulaires d’une épaisseur d’environ 20 cm et d’une longueur pouvant atteindre 8,5 m. Ils sont laminés pour fabriquer des plaques de cuivre. Elles sont laminées pour fabriquer des plaques, des bandes, des feuilles et des produits en feuille de cuivre. Les billettes sont des billes cylindriques d’environ 20 cm de diamètre et de plusieurs mètres de long. Elles sont extrudées ou étirées pour fabriquer des tubes et des tuyaux en cuivre. Les tiges ont une section transversale ronde d’environ 1,3 cm (0,5 po) de diamètre. Elles sont généralement coulées en très grandes longueurs, qui sont enroulées. Ce matériau enroulé est ensuite étiré davantage pour fabriquer du fil de cuivre.
Contrôle de la qualité
Parce que les applications électriques exigent un très faible niveau d’impuretés, le cuivre est l’un des rares métaux communs qui sont raffinés à presque 100% de pureté. Le processus décrit ci-dessus a été prouvé pour produire du cuivre de très haute pureté. Pour garantir cette pureté, des échantillons sont analysés à différentes étapes afin de déterminer si un ajustement du procédé est nécessaire.
Sous-produits/déchets
La récupération de l’acide sulfurique à partir du processus de fusion du cuivre fournit non seulement un sous-produit rentable, mais réduit également de manière significative la pollution atmosphérique causée par l’échappement du four. L’or, l’argent et d’autres métaux précieux sont également des sous-produits importants.
Les déchets comprennent les morts-terrains de l’exploitation minière, les résidus de l’opération de concentration et les scories de l’opération de fusion. Ces déchets peuvent contenir des concentrations importantes d’arsenic, de plomb et d’autres produits chimiques, qui constituent un danger potentiel pour la santé des populations environnantes. Aux États-Unis, l’Agence de protection de l’environnement (EPA) réglemente le stockage de ces déchets et l’assainissement de la zone une fois que les opérations d’extraction et de traitement ont cessé. Le simple volume des matériaux concernés – dans certains cas, des milliards de tonnes de déchets – rend cette tâche formidable, mais elle présente également des opportunités potentiellement rentables pour récupérer les matériaux utilisables contenus dans ces déchets.
L’avenir
La demande de cuivre devrait rester élevée, en particulier dans les industries électriques et électroniques. Les tendances actuelles du traitement du cuivre vont vers des méthodes et des équipements qui utilisent moins d’énergie et produisent moins de pollution atmosphérique et de déchets solides. Aux États-Unis, il s’agit d’une mission difficile en raison des contrôles environnementaux stricts et des minerais de cuivre à très faible concentration qui sont disponibles. Dans certains cas, les coûts de production peuvent augmenter de manière significative.
Une tendance encourageante est l’utilisation accrue de cuivre recyclé. Actuellement, plus de la moitié du cuivre produit aux Etats-Unis provient de cuivre recyclé. Cinquante-cinq pour cent du cuivre recyclé provient d’opérations d’usinage du cuivre, comme le formage par vis, et 45 % provient de la récupération de produits en cuivre usagés, comme les fils électriques et les radiateurs automobiles. Le pourcentage de cuivre recyclé devrait augmenter à mesure que les coûts de traitement du cuivre neuf augmentent.
Où en savoir plus
Livres
Brady, George S., Henry R. Clauser, et John A. Vaccari. Manuel des matériaux. McGraw-Hill, 1997.
Heiserman, David L. Exploration des éléments chimiques et de leurs composés. TAB Books, 1992.
Hombostel, Caleb. Les matériaux de construction. John Wiley and Sons, Inc, 1991.
Kroschwitz, Jacqueline I. et Mary Howe-Grant, ed. Encyclopédie de la technologie chimique. John Wiley and Sons, Inc. 1993.
Stwertka, Albert. Guide des éléments. Oxford University Press, 1996.
Périodiques
Baum, Dan et Margaret L. Knox. « Nous voulons que les gens qui ont un problème avec les déchets miniers pensent à Butte ». Smithsonian (novembre 1992) : 46-52, 54-57.
Shimada, Izumi et John F. Merkel. « Métallurgie des alliages de cuivre dans le Pérou ancien ». Scientific American (juillet 1991) : 80-86.
Autre
http://www.copper.org .
http://www.intercorr.com/periodic/29.htm .
http://innovations.copper.org/innovations.html .
– Chris Cavette