Termes clés
- anaérobie : Sans oxygène ; notamment d’un environnement ou d’un organisme.
- réduction : Réaction dans laquelle des électrons sont gagnés et la valence est réduite ; souvent par l’élimination de l’oxygène ou l’ajout d’hydrogène.
- Respiration anaérobie : réactions et processus métaboliques qui ont lieu dans les cellules des organismes qui utilisent des accepteurs d’électrons autres que l’oxygène
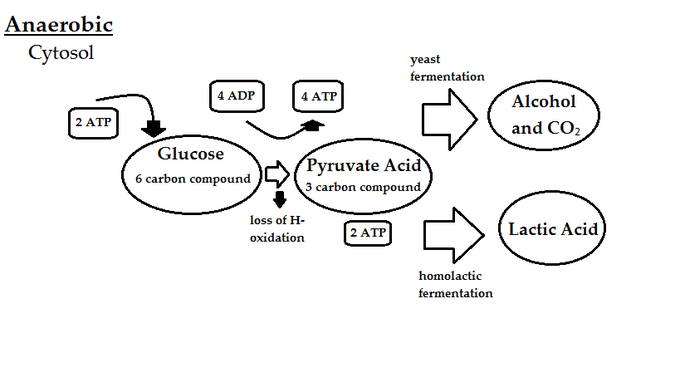
La respiration anaérobie est la formation d’ATP sans oxygène. Cette méthode intègre toujours la chaîne de transport d’électrons respiratoire, mais sans utiliser l’oxygène comme accepteur d’électrons terminal. À la place, des molécules telles que le sulfate (SO42-), le nitrate (NO3-) ou le soufre (S) sont utilisées comme accepteurs d’électrons. Ces molécules ont un potentiel de réduction plus faible que l’oxygène ; ainsi, moins d’énergie est formée par molécule de glucose dans des conditions anaérobies par rapport aux conditions aérobies.
Plusieurs types d’accepteurs d’électrons peuvent être utilisés pour la respiration anaérobie. La dénitrification est l’utilisation du nitrate (NO3-) comme accepteur terminal d’électrons. Le nitrate, comme l’oxygène, a un potentiel de réduction élevé. Ce processus est très répandu et utilisé par de nombreux membres des protéobactéries. De nombreuses bactéries dénitrifiantes peuvent également utiliser le fer ferrique (Fe3+) et différents accepteurs d’électrons organiques.
La réduction du sulfate utilise le sulfate (SO2-4) comme accepteur d’électrons, produisant du sulfure d’hydrogène (H2S) comme produit final métabolique. La réduction du sulfate est un processus relativement pauvre en énergie, et est utilisé par de nombreuses bactéries Gram négatif trouvées dans les δ-Proteobacteria. Elle est également utilisée par des organismes Gram positifs apparentés à Desulfotomaculum ou à l’archée Archaeoglobus.
La réduction des sulfates nécessite l’utilisation de donneurs d’électrons, tels que les composés carbonés lactate et pyruvate (réducteurs organotrophes), ou l’hydrogène gazeux (réducteurs lithotrophes). Certaines bactéries sulfato-réductrices autotrophes inhabituelles, telles que Desulfotignum phosphitoxidans, peuvent utiliser le phosphite (HPO3-) comme donneur d’électrons. D’autres, comme certaines espèces de Desulfovibrio, sont capables de disproportionner le soufre (scinder un composé en un donneur d’électrons et un accepteur d’électrons) en utilisant le soufre élémentaire (S0), le sulfite (SO3-2) et le thiosulfate (S2O32-) pour produire à la fois du sulfure d’hydrogène (H2S) et du sulfate (SO2-).
L’acétogenèse est un type de métabolisme microbien qui utilise l’hydrogène (H2) comme donneur d’électrons et le dioxyde de carbone (CO2) comme accepteur d’électrons pour produire de l’acétate, les mêmes donneurs et accepteurs d’électrons utilisés dans la méthanogenèse.
Le fer ferrique (Fe3+) est un accepteur d’électrons terminal anaérobie très répandu, utilisé par les organismes autotrophes et hétérotrophes. Le flux d’électrons dans ces organismes est similaire à ceux du transport d’électrons, se terminant en oxygène ou en nitrate, sauf que dans les organismes réducteurs de fer ferrique, l’enzyme finale de ce système est une réductase du fer ferrique. Comme certaines bactéries réductrices du fer ferrique (par exemple G. metallireducens) peuvent utiliser des hydrocarbures toxiques (par exemple le toluène) comme source de carbone, il y a un intérêt significatif à utiliser ces organismes comme agents de biorestauration dans les aquifères contaminés par le fer ferrique.
Les autres accepteurs d’électrons inorganiques comprennent la réduction de l’ion manganique (Mn4+) en manganeux (Mn2+), du sélénate (SeO42-) en sélénite (SeO32-) en sélénium (Se), Arsenate (AsO43-) en arsénite (AsO33-), et Uranyle (UO22+) en dioxyde d’uranium (UO2)
Les composés organiques peuvent également être utilisés comme accepteurs d’électrons dans la respiration anaérobie. Il s’agit notamment de la réduction du fumarate en succinate, du N-oxyde de triméthylamine (TMAO) en triméthylamine (TMA), et du sulfoxyde de diméthyle (DMSO) en sulfure de diméthyle (DMS).