Org 2での「アミン」の扱いについてですが、物語がありません。
ほとんどの章とは異なり、一連の概念から始まり、その概念を適用できる一連の例へと積み上げていくわけではありません。入門教科書の典型的なアミンの章は、基本的に、他のどこにも当てはまらない、一見ランダムに見えるトピックを寄せ集めたものに過ぎません。
例として、今日のランダムなアミン投稿は、Hofmann と Curtius の転位についてです。 良い答えはありません。 ほとんどのコースでいつか取り上げられるし、どこかに組み込まれているはずです。 だから、いったい何なのでしょう。
目次
- The Hofmann and Curtius Rearrangements
- HofmannとCurtiusの転位のメカニズム、パート1 – 転位の設定
- パート2:HofmannとCurtius転位における重要な転位ステップ
- パート3:転位が起こる前に、転位が起こるまで
- 転位が起こった後、その転位が起こるまで
- ステップをまとめる
- イソシアン酸の運命。 カルバメート、アミン、および尿素の生成
- まとめ:Hofmann および Curtius 転位
- 注
- (上級)参考文献とさらなる読み物
。 イソシアン酸の生成
The Hofmann and Curtius Rearrangements
ホフマン転位とカーティウス転位の二つは、共通の機構上の手順を持つ転位反応全体のファミリーの例である。
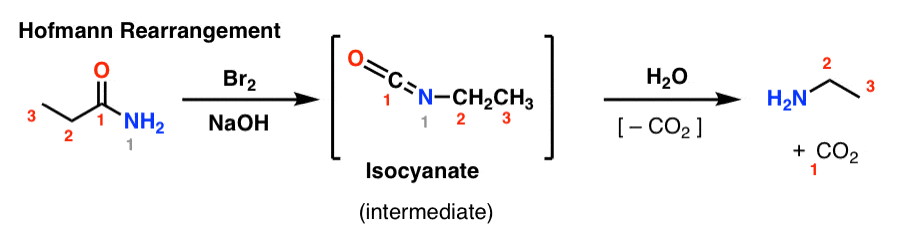
ホフマン転位では、アミドを臭素と塩基(通常NaOHまたはKOH)で処理する。 加熱すると、中間体イソシアネートが生成するが、これは単離されない。 水の存在下で、イソシアネートは二酸化炭素を失い(「脱炭酸」)、アミンを生成する。
ホフマンで形成される重要な結合は、C2-N結合である。 カルボニル基(C1)が失われ、二酸化炭素(CO2)が形成されることに注目。 (注:これはIUPAC番号ではなく、議論を容易にするための番号です)
Curtius転位では、アシルアジドが加熱され、イソシアネートが形成されます。 Curtius では、イソシアネートを単離することができますが、通常はさらにカルバメート、尿素、または (Hofmann のように脱炭酸を介して) アミンなどの他の種に変換されます (これらについては後で説明します)。
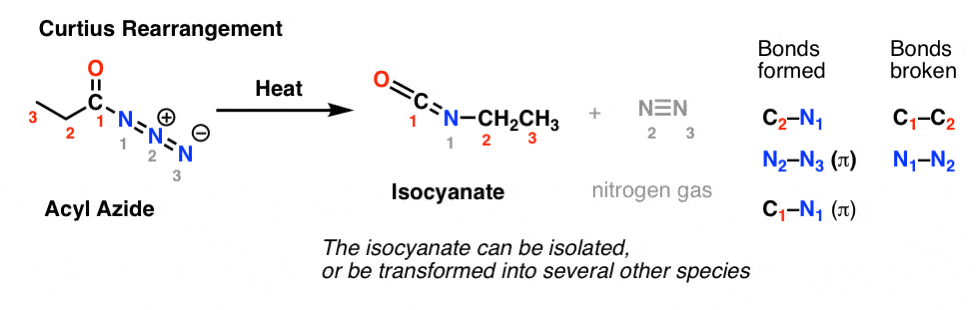
どちらの場合も注意すべき点は、C1-C2 結合は壊れて、新しい C2-N 結合ができている、という点です。
The Mechanism of the Hofmann and Curtius Rearrangements, Part 1: Setting Up The Rearrangement
Curtius転位とHofmann転位のメカニズムには4つの重要な部分があり、それらをすべて見ていきます。
- 前奏(簡単)
- The key migration step (tricky, but if you realize a variant of it in Org 1 !)(難しいが、それのオーガナイザーで見たことがあるのならそれほど難しくもない。
- イソシアネートの生成(簡単)
4.エピローグ。 イソシアン酸の変換
Part1: 前奏曲
- Hofmann転位はアミドで起こる。
- Curtius転位はアシルアジドで起こる。
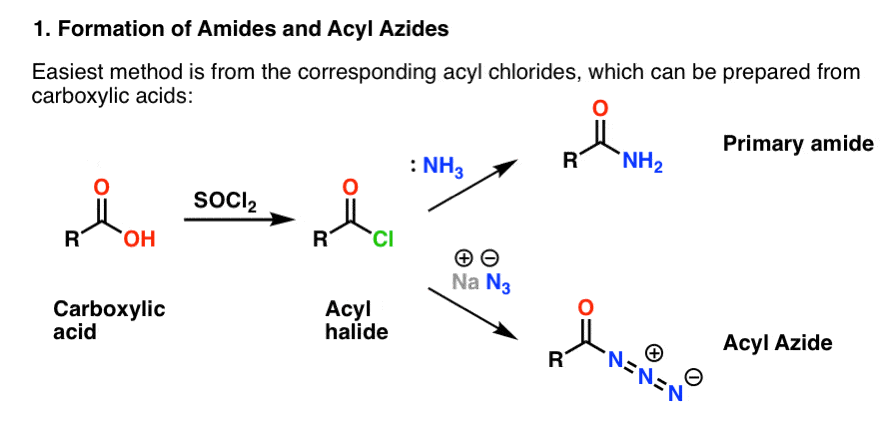
どちらもハロゲン化アシルから付加脱離反応によって簡便に調製される。 今、アミンを取り上げているのであれば、カルボニル反応は馴染みのある分野であろう。 ハロゲン化アシルは、塩化チオニル(SOCl2)や五塩化リン(PCl5)などの試薬を用いてカルボン酸から調製することができる。
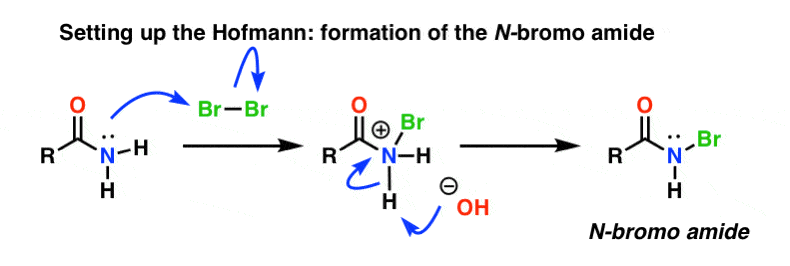
ホフマンの設定
ホフマン転位は、アミドを臭素(Br2)とNaOHなどの塩基で処理する。 この結果、N-Hが切断されN-Brが生成し、窒素に良好な脱離基が設置される。 これを「N-ブロモアミド」と呼んでいます。
アシルアジドにはすでに立派な脱離基が組み込まれているので、Curtiusは「設定」する必要がないのです。 N2. このため、有機アジドは乱暴に扱うと爆発することがあり、注意が必要です。
3. HofmannとCurtiusにおける重要な転位ステップ
さて、本題に入ります。
HofmannとCurtiusの転位で重要なステップは、炭素原子が移動して、隣接する窒素上の脱離基を置換することです。
これには2つの曲線矢印を描く必要がありますが、これは左端の構造(下)に示されているものです。
- 最初の曲がった矢印では、C-C結合が切れ、新しいC-N結合が形成されます。
- 2番目の曲がった矢印では、N-LG(脱離基)結合が切れます。
しかし、左端の構造から右端の構造(きれいに整然と描かれている!)に直接行くのは必ずしも簡単ではありません。
毎年試験で、曲線矢印は正しいが間違った構造を描いてしまった学生によって、無数の点が不必要に失われています!
は、2番目の曲線矢印で、N-LG(離脱基)結合が壊れています。 だから私は学生たちに、まず「醜いバージョン」を描くように勧めています。それは見た目はひどいものですが、少なくともすべての結合が正しい位置にあるものなのです。 6437>
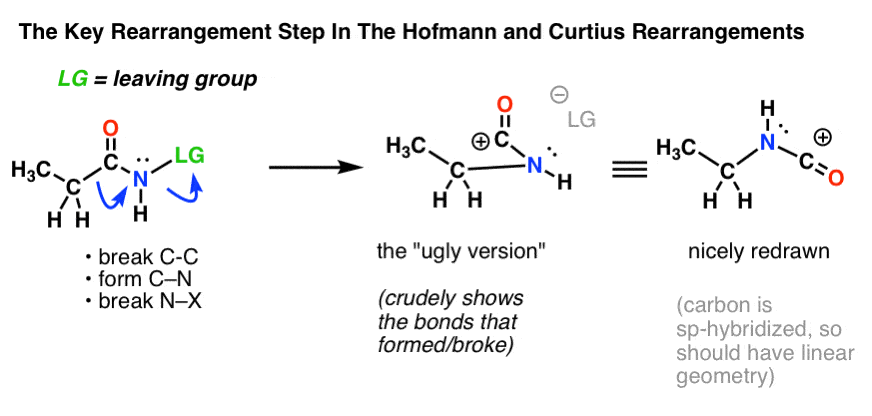
最初はこの転位はおそらく…奇妙に見えるでしょう。 しかし、それは実はあなたが以前に見たことのある反応なのです! (
Hydroboration-oxidation の “oxidation” のステップのメカニズムを覚えている人はいますか?
それは基本的に同じことです!
ここで復習です。
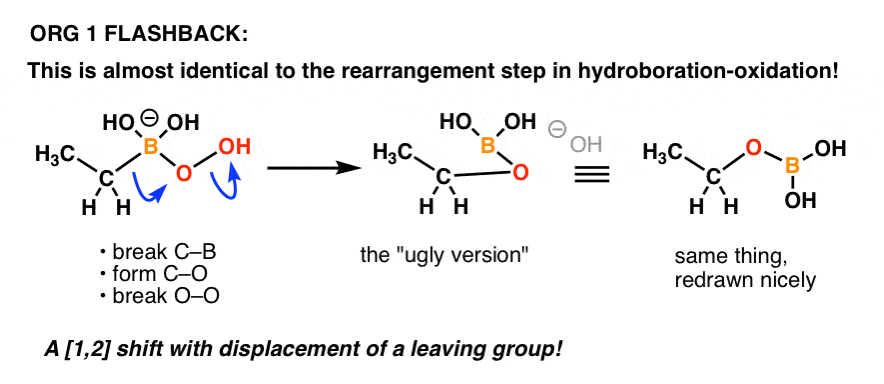
有機化学の以前のパートで学んだことが、後のパートでどのように戻ってくるかのもう1つの例です!
ここで、Hofmann転位とCurtius転位の具体的な転位ステップを具体例で見てみましょう。
ここで、Hofmannの重要なステップは、加熱によって、C-Cの切断、C-Nの形成、N-Brの切断が起こるところです。
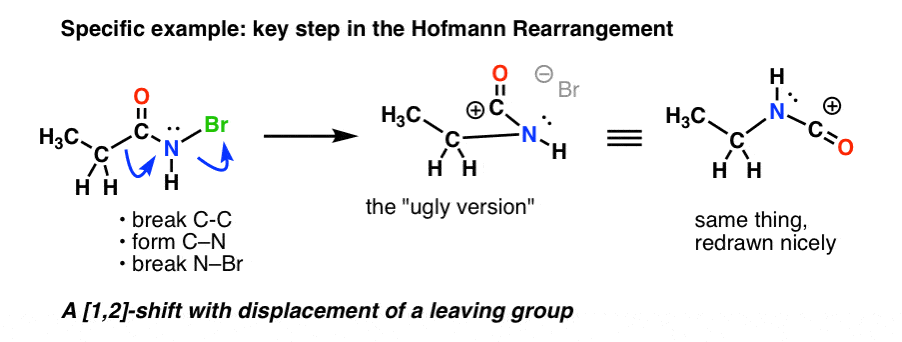
すべての矢印に従うと、奇妙な形のカルボカチオン(右上)に行き着きますが、これはすぐに扱います。
Curtiusでは、アシルアジドを加熱すると、転位が起こります。
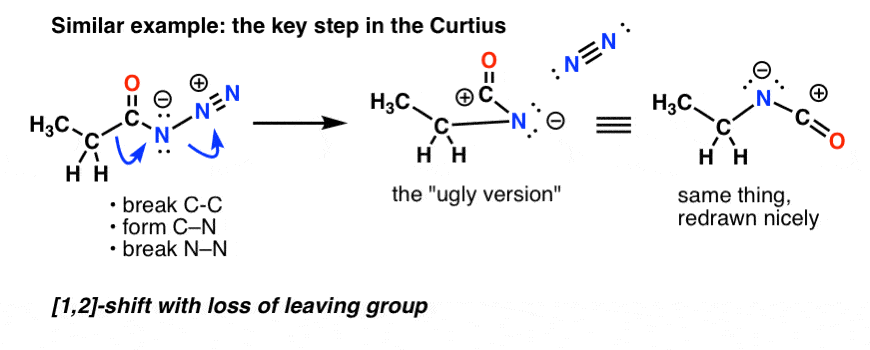
(CurtiusとHofmannの微妙な違いは、CurtiusではNに水素が結合していないため、転位した種の窒素に負の電荷が生じることです)
Isocyanate
次のステップは、転位種からISOCになることです。 共鳴形を描くのに慣れている人なら、これはそれほど難しくないはずです。
(後述しますが、イソシアネートの生成は移動と同時に起こることが研究で分かっています。 しかし、私たちの教育目的では、このステップを切り離して扱うことが役立つと思います。 すぐにまとめることができます)。
Org 1のところで思い出したかもしれませんが、完全なオクテットを持つ共鳴形態は持たない形態よりも優れています(クイックレビュー)。 私たちが転位で得た奇妙な形の生成物には、孤立対を含む窒素に隣接したカルボカチオンがあります。 そこで、まず最初に、新しいC-Nπ結合の形成を描きます。 これは本質的には単なる共鳴形です。
Hofmann転位は塩基の存在下で起こります。 共鳴形を描いた後、次のステップはN-H結合の脱プロトン化で、中性のイソシアネートを与えます。
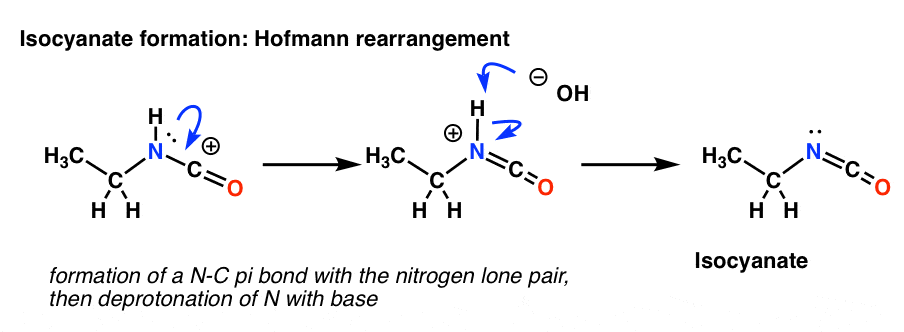
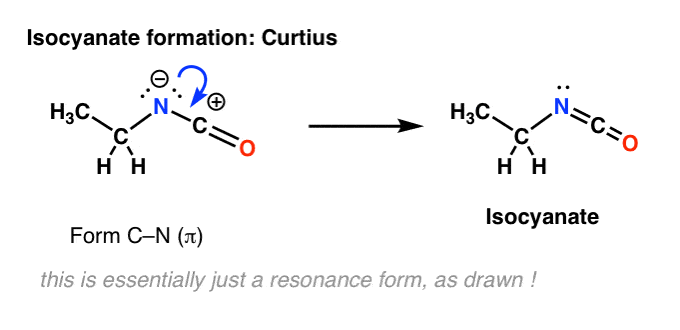
Curtiusでは窒素上に水素はありません。 したがって、イソシアネートの生成は、単に窒素からカルボカチオンへのローンペアの供与によって達成される。
Putting The Steps Together
Hofmann 転位と Curtius 転位の機構の研究では、これらの 2 つのステップが順次起こるのではなく、実際には同時に起こることを決定しました!
Hofmann 転位と Curtius 転位の機構では、2 つのステップが同時に起こっていることを決定しました。 (つまり、イソシアネートの形成と同時にマイグレーションが起こるのです(なぜこのことがわかるのでしょうか?
それを反映させるために、HofmannとCurtiusのメカニズムを描き直して、両方のステップを組み込む必要があります。
ここにHofmannを示します(実際には脱プロトン化イベントは別であることに注意してください)。
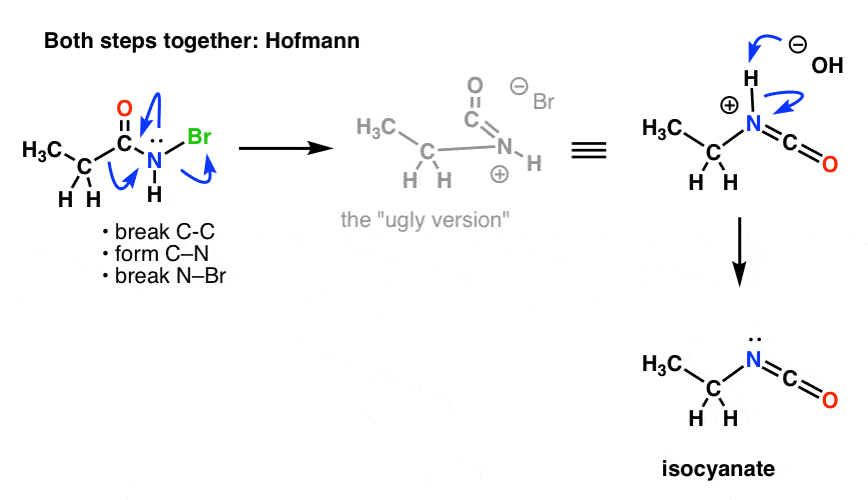
Curtius:
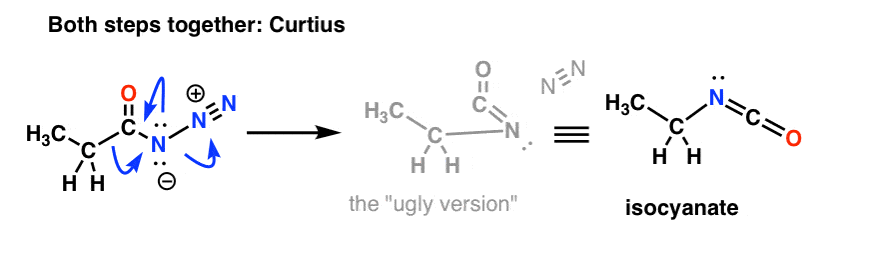
The Fate Of The Isocyanate
Hofmann と Curtius はともにイソシアネートを生成させるものである。 イソシアン酸塩に出会ったことはないだろうか。 一見すると、かなり奇妙な種ですが、その化学的性質は、エステル、アミド、ハロゲン化アシルなどの他のカルボニル種とそれほど変わりません。 炭素は2つの強い電気陰性原子にπ結合している。 これは、炭素を優れた親電子性にします。
さまざまな求核剤を加えることによって、イソシアネートは他の有用な種に変換されます。
– アルコールを加えると、カルバミン酸が生成します
– アミンを加えると、尿素になります
– 水を加えるとカルバミン酸になり、これは不安定になります。 カルバミン酸はすぐに二酸化炭素を失い、アミンになる
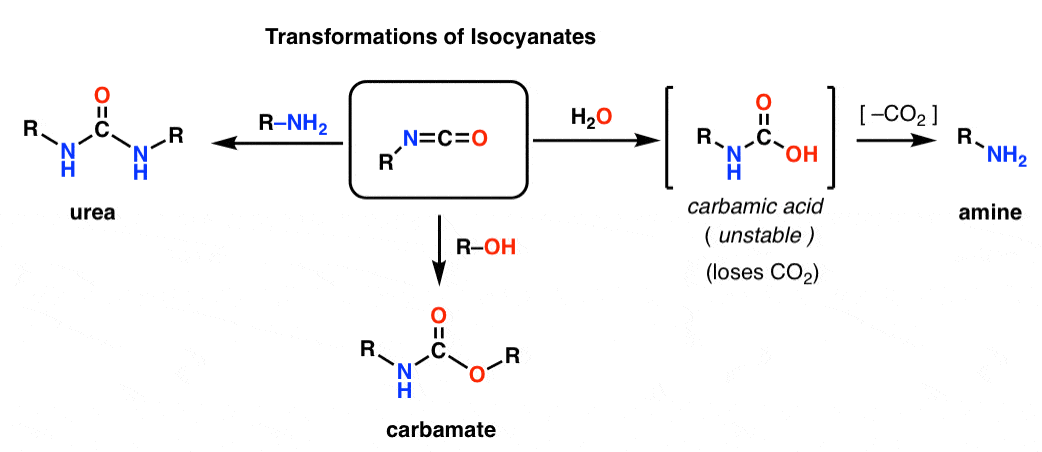
特に、脱炭酸経路はアミンを作るための巧妙な方法を提示している。 カルボン酸の作り方はたくさん習いましたが、アミンの作り方は(求核置換と還元的アミノ化以外では)あまり多くありません。 ホフマンは、そのどちらも当てはまらないような状況、たとえば置換アニリンを作るような状況で、後ろ盾として持っておくと便利なトリックです
メカニズム? OK、結構です。 ボーナストピック 1 を参照してください。
Summary: The Hofmann and Curtius Rearrangements
これらの転位のメカニズムは一見厄介ですが、以前に移行反応の変種を見たことがあることに気づけばかなり楽になります (i.) 。
私は、より美しく魅力的な構造に描き直す前に、結合の形成と切断を見ることに集中できるように、醜いバージョンを最初に描くことを強くお勧めします。 これは、ベックマン転位とウォルフ転位についても同様です。 下図では、窒素にアニオンを形成するように求核剤を炭素に付加していますが、これは最良の共鳴形態ではありません(酸素は窒素よりも負電荷を安定化させるのに優れています)。 酸素から窒素へのプロトン移動により、中性種が生成する。 (I used the Magic Wand of Proton Transfer here, because it’s faster).
Note that the decarboxylation step in 1) does not be priored by deportation of the oxygen, although it definitely needs to occur such that nitrogen is protonated during the step (you want to form a strongly basic amide ion, for instance).Now to have been priored by deportation of the oxygen, not have been priored to the one.
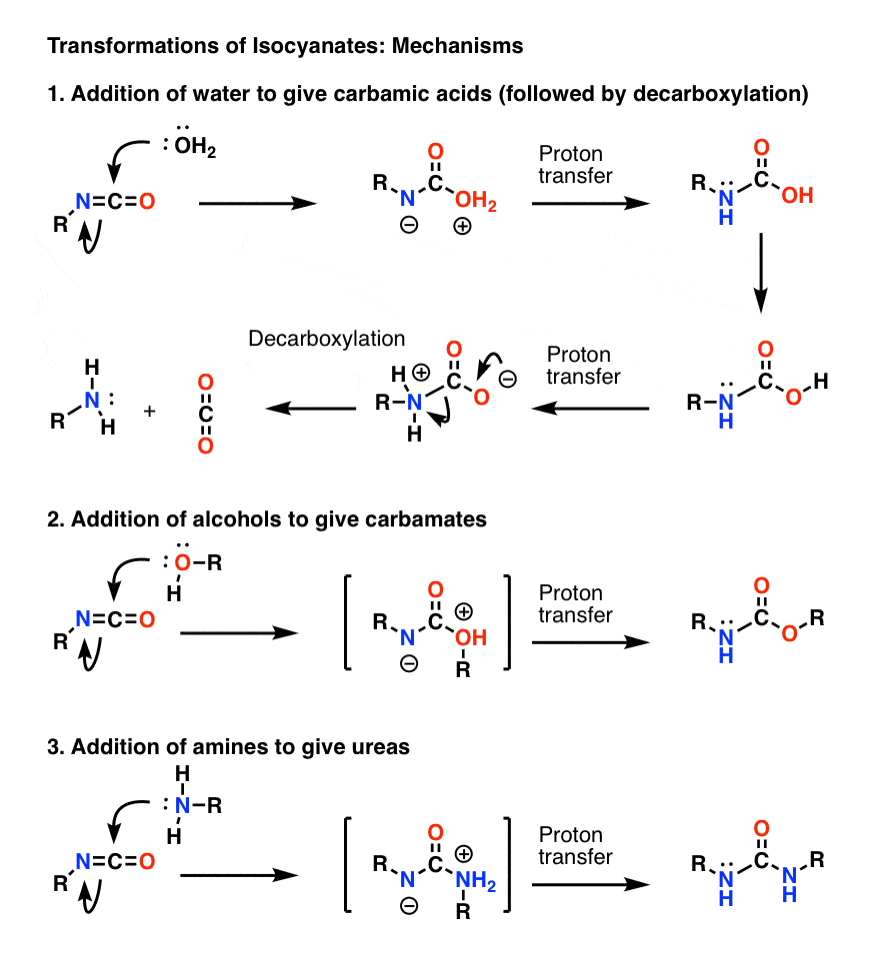
ボーナストピック2:ベックマン、ウォルフ、その他の転位は同じようなステップを共有している
でも、待って、もっとある!
ベックマン転位では脱離基を失って1,2シフトがあるのです。
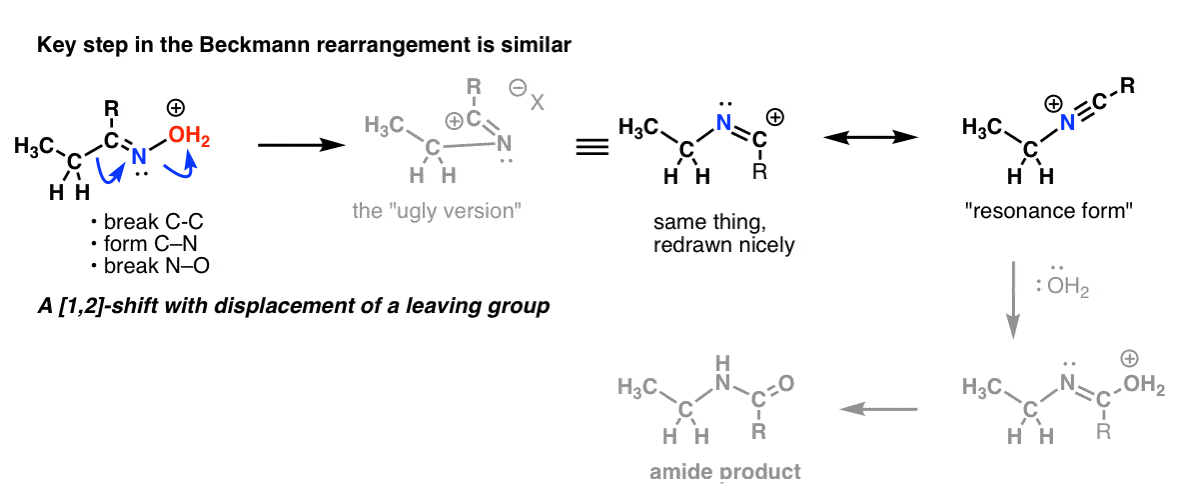
そして、よく取り上げられるWolff転位でも、同じキーステップを認識できるかもしれません。 Curtius と同じように、塩化アシル(またはカルボン酸)に HN3 を加えることで起こる Schmidt 転位と呼ばれる反応があるのです。 また、ヒドロキシアミック酸で起こるロッセン転位と呼ばれる反応もある。 この2つのプロセスの鍵となるステップを当てても、賞はありません。
Org 1のヒドロホウ素化-酸化のステップを学んだとき、私はまさか同じ反応パターンがこれほど多くの異なる形で繰り返されるとは思っていませんでした。 このことは、有機化学における重要なパターンを学ぶことの重要性を浮き彫りにしています。なぜなら、それらは確かによく繰り返されるからです。
Curtius が段階的であれば、窒素の喪失はニトリンをもたらすでしょう。 ニトレンはC-H結合への挿入(!)など、興味深い反応を多数起こします。 そこで、これをテストするために実験を計画することができます。次の Curtius 転位を試すと、5 員環の形成の証拠を探すことができます。
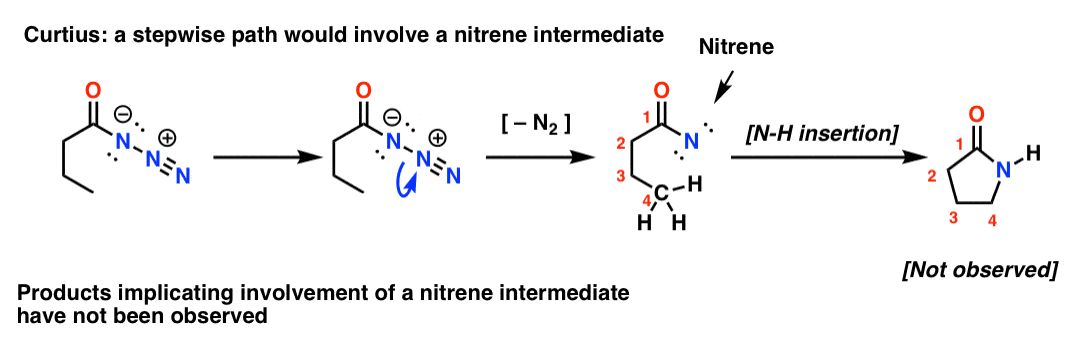
そのような生成物がないことは、他の証拠とともに、協調的メカニズムを指摘しています。
(詳細)文献および参考文献
- Ueber die Einwirkung des Brom in alkalischer Lösung a Amide
W. Hofmann
Chem. Ber. 1881, 14, 2725-2736
DOI: 10.1002/cber.188101402242
A. W. Hofmann(彼は非常に生産的な化学者で、他にも多くの変換に彼の名前があります)によるアミドから一級アミンへの分解に関するオリジナル論文。 - A Mild and Efficient Modified Hofmann Rearrangement
Xicai Huang, Mehran Seid, and Jeffrey W. Keillor
The Journal of Organic Chemistry 1997, 62 (21), 7495-7496
DOI:10.Hofmann Mold and Efficient Mild Hofmann Rearrangementは、一級アミンの分解に関するオリジナルな論文。1021/jo9708553
これはメタノール中で実施された修正ホフマン転位である-この場合、中間カルバミン酸はメタノール溶媒と反応し、良い収率でメチルカルバメートを生成できる - METHYL CARBAMATE FORMATION VIA MODIFIED HOFMANN REARRANGEMENT REACTIONS: メチル N-(p-METHOXYPHENYL)CARBAMATE
Jeffrey W. Keillor and Xicai Huang
Org. Synth. 2002, 78, 234
DOI: 10.15227/orgsyn.078.0234
Ref#2 の修正 Hofmann Rearrangement の信頼できる、独自にテストした手順。 - The Hofmann Reaction
Wallis, Everett L.; Lane, John F.
Org.No. React. 1946, 3, 267-306
DOI: 10.1002/0471264180.or003.07
Hofmann反応(アミド→アミン反応、彼の他の反応と混同しないように)についての古いが当時としては包括的なレビューです。 - Note – A Re-examination of the Limitations of the Hofmann Reaction
Ernest Magnien and Richard Baltzly
The Journal of Organic Chemistry 1958, 23 (12), 2029-2032
DOI:10.XXXXXXXX.XXXXXX.XXXX.XXXX.XXXX.XXXX.XXXX.1021/jo01106a630
著者らが反応条件を慎重に調整することにより、ホフマン転位の範囲を原著論文に記載されたものよりも広げようとした興味深い論文です - 20. ヒドラジドとアジド 有機セイレーン
Curtius, T. I. Abhandlung.
Journal Für Praktische Chemie, 50(1), 275-294. (1894).
DOI:1002/prac.18940500125 - Ueber Stickstoffwasserstoffsäure (Azoimid) N3H.
Curtius, T.
Berichte Der Deutschen Chemischen Gesellschaft, 23(2), 3023-3033.(1890).
DOI:1002/cber.189002302232
Theodore Curtiusによるアシルヒラジドとアシルアジドの反応性を述べた最初の論文 - The Curtius Reaction
Smith,P. A. S.
Org.B.S.,P. A.S.
The Curtius Reaction
The Curtius Reaction
Smith,P. A. S.
Org.B.S.,P. A.S.
The Curtius Reaction
DOI:1002/cber.1890023032DOI: 10.1002/0471264180.or003.09
この転位の発見の歴史、基質範囲、限界、他の類似反応との比較、実験手順などを含むCurtius反応の古いながらも総合レビューです。 H. Allen and Alan Bell
Org. Synth. 1944, 24, 94
DOI: 10.15227/orgsyn.024.0094
Curtius転位によるイソシアネート合成のための古いが再現性のある試験済み手順。 - An Expedient Protecting-Group-Free Total Synthesis of (±)-Dievodiamine
William P. Unsworth, Christiana Kitsiou, and Richard J. K.。 Taylor
Organic Letters 2013 15 (13), 3302-3305
DOI:1021/ol4013469
この全合成の最初のステップは、Curtius転位を用いてインドール置換カルボン酸の分子内環化反応を行うことです。 121. ヨウ化亜鉛触媒によるアロイルクロライドとトリメチルシリルアジドからのアロイルアジドの調製
K. Surya Prakash, Pradeep S. Iyer, Massoud Arvanaghi, and George A. Olah
The Journal of Organic Chemistry 1983 48 (19), 3358-3359
DOI: 10.1021/jo00167a051
Nobel Laureate Professor George A. Olahから芳香族アリールアジドを容易に準備する手順を紹介したものです。 Curtius転位に利用可能です。