Abstract
大腸手術後の吻合部漏出(AL)などの合併症は、大きな病的状態と関連しています。 大腸手術後の吻合部漏出(Subclinical AL)は,臨床的な挙動から誤解を招くことがあり,診断にジレンマがある。 また、放射線検査は補助的な検査であるが、診断の遠因となることがある。 我々は、診断のニアミスにより好ましくない結果を招いた不顕性 AL の一例を提示する。 本症例は不顕性 AL の診断にニアミスし、予後不良となった症例であり、診断結果は臨床背景を考慮し、慎重に解釈する必要がある。
キーワード
anastomotic leakage, subclinical leak, contrast enema
はじめに
大腸肛門手術は一般外科の中で大きな割合を占めている。 しかし、吻合部漏出(AL)などの合併症は、手術の進歩や正確な手術手技にもかかわらず、重大な罹患率と死亡率の原因となっている。 局所的あるいは限局的な漏れは憂慮すべき症状を伴わないため、不顕性吻合部漏出と呼ばれます。 腹部コンピュータ断層撮影(CT)は、術後合併症を評価する際に選択される方法となっている。 このような症例におけるCTの優位性は証明されていないが、報告におけるヒューマンエラーが標準以下の転帰をもたらすことも珍しくはない。
症例提示
82歳男性が異常な嗜眠のため内科病棟に入院した。 6週間前に直腸中部腺癌に対して腹腔鏡補助下前方切除術を行い、回腸吻合器を装着した。 吻合は30mm円形ステープラーで行われた。 本症例では、ストーマ排泄量の増加と異常な疲労感を訴えた。 身体所見に異常はなかった。 血液学的検査では尿素・クレアチニン比が高く、電解質異常が認められた。 その後、ストーマからの排泄量は徐々に減少し、患者は腹痛と嘔吐を訴え始めた。 この時点で外科チームが介入した。 腹部X線写真では、小腸ループの拡張と多量の空気液が確認された。 腹部CTでは小腸ループの拡張が確認された。 大腸吻合部は無傷で、漏出の所見はなかったと報告されている。 鑑別診断として、癒着性腸閉塞または電解質異常による二次性イレウスが考えられた。 経鼻胃管減圧と輸液による蘇生を開始した。 癒着と手術歴のため回復が遅れることが予想され、非経口栄養を開始した。 当初は48時間後にストーマ機能が回復し、閉塞症状は改善したが、経口清涼飲料水を再開したところ、疼痛と胆汁性嘔吐が再発した。 このため、経鼻胃管から水溶性造影剤を投与し、診断・治療を行っている。 検査で回腸吻合部近位の小腸閉塞を指摘され,確認のため放射線科医から回腸吻合部からの造影剤投与が指示された. ストーマからフォーリーカテーテルが挿入され、患者は再撮影のため画像診断部門に送られた。 腹腔内、気腹に造影剤の滲出を認めた。 回腸瘻穿孔を考慮し、緊急開腹手術が行われた。 初回手術から6週目であったため、必要に応じて回腸吻合部の切除・反転を行う前に、吻合部の健全性を確認するために水溶性造影剤による注腸が行われた。 直腸吻合部は無傷であり、直腸の膨張も良好であったとの報告であった。 骨盤内に造影剤が貯留しており、前回の回腸吻合部穿孔からの流出と考えられた(図1矢印)
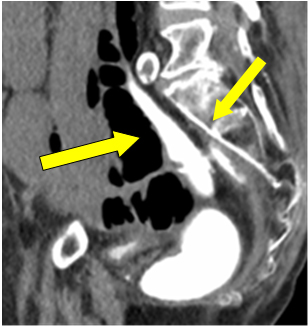
図1:骨盤内の造影剤の溢出
再開腹術が行われた。 マクロ的な穿孔は認めなかった。 所見では中等量の血漿があり、線維性癒着は少なく、閉塞性バンドはなかった。 骨盤内には正常サイズの癒着した小腸ループが認められた。 これらは外科医に邪魔されなかった(画像上、吻合部のリークはない)。 残存小腸の癒着切除が行われ、回腸吻合は解除された。 術後5日目に譫妄、急速な心房細動を発症するまで安定した経過をたどった。 術後5日目に譫妄、心房細動が出現し、開腹創の剥離を認めた。 術後5日目に心房細動が出現した。 その結果、広範な気腹と左傍大動脈に約200mlの縁強化貯留を認めた。 患者は再び緊急手術室に運ばれ、再探査が行われた。 開腹すると糞便性腹膜炎を呈し、大腸吻合部には小腸の癒着により大きな欠損が隠されていた。 吻合部を切除し、S状結腸端ストーマを造設し、直腸切片を閉鎖した
患者は回復に時間がかかり、リハビリテーション施設に転院した。 445>
考察
AL は依然として大腸手術における罹患および死亡の主因である。 ALは大腸手術における罹患率と死亡率の主な原因であり、速やかに発見し適切な治療を行わなければ、死亡率は50%に達する。 ストーマの機能不全は下部消化管吻合の完全性を保証しない可能性がある。 臨床管理は解剖学的部位、漏れの程度、症状の重症度によって異なる。 限局性漏出の亜臨床的特徴は、しばしば診断に混乱をもたらす。 迅速な臨床管理には、高い疑い指数と早期発見が重要である。
CT スキャンは、術後腸管合併症の検査として最も容易に利用できるものである。 吻合部周辺の空気、液体、またはその両方の組み合わせのような漏れの特定のX線的特徴は、まれにしか存在しないことがある。 しかし、下部腸管ALに対する診断的有効性は十分に確立されていない。 術後の変化や、残存気腹、仙骨前軟部組織の瘢痕化や炎症性ストランディングなどの交絡因子のため、画像の解釈には混乱が生じることがある。 造影剤は漏れの割合や範囲を示すだけでなく、仙骨前血液貯留のような現象の診断に役立ちます。 特に臨床的に疑わしくない患者に対して、ストーマ造設直前のルーチン検査としての役割はまだ疑問である。 しかし、遠位吻合部の漏れの検出においては、水溶性造影剤を用いた検査が優れていることが示されている
また、さまざまな研究により、吻合部漏れを疑うX線画像の偽陰性率は35%~49%であることが報告されている。
このシナリオでは、腸閉塞は赤信号でした(不顕性敗血症によるイレウスが進行している可能性が高い)。 初診時、回腸瘻に肉眼的な漏出は認めなかった。 切除標本の組織学的検査では、粘膜の損傷は認められなかった。 しかし、漿膜裂傷はカテーテルが腹膜に入る前に漿膜下層を通過したことを示唆するものであった。 放射線科で画像のレトロスペクティブな解析が行われた。 そのうちの一枚のフィルムで、カテーテルの先端が皮下面を通過していることが確認された(図2)。 これは回腸瘻孔の穿孔ではなく、腹腔内への造影剤の侵入を意味する。
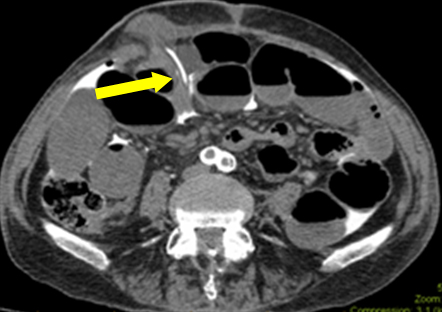
Figure 2: Axial image showing catheter’s tip entering from subcutaneous plane into peritoneal cavity
些細なことですが、注腸時に吻合部付近に造影剤が漏れ、溜まっていたことは大きな発見となりました。
患者は最近悪性腫瘍の手術を受け、栄養不良と腸閉塞が続いていたため、吻合の治癒はすでに危うい状態でした。
以前の低位前方切除術により、小腸ループは骨盤内に固着しており、当初は軽度のALであったため、古典的な臨床的特徴は欠落していました。 回腸吻合術が取り消され、吻合部の完全性を保護するための糞便迂回がなくなると、漏出サイズは進行し、腹膜炎と腹部剥離を伴う悪化につながった。 臨床的な洞察力を背景とした研究結果の解釈には注意が必要である。 また、手術所見と異なる画像に対して定期的に建設的なフィードバックを行うことで、将来の症例バンクを確立することができます。
他の合併症や栄養状態の悪化を伴う腫瘍性疾患患者は、腸管吻合の治癒を損なう可能性が非常に高い。 特に古典的な漏出の徴候がない場合は、不顕性吻合に対して脆弱であると考えるべきであろう。 また、外科医にとって、外科的放射線学を学ぶことは最も重要であり、放射線科医への定期的なフィードバックは、大腸手術後の新しい術後合併症の提示を特定するのに役立つと思われます。
- Trencheva K, Morrissey KP, Wells M, Mancuso CA, Lee SW, et al. (2013) Identifying important predictors for anastomotic leak after colon and rectal resection: prospective study on 616 patients.大腸切除術後の吻合部漏れの重要な予測因子の特定:616人の患者に関する前向き研究。 Ann Surg 257: 108-113.
- Lim M, Akhtar S, Sasapu K, Harris K, Burke D, et al. (2006) Low colorectal anastomosis after Clinical and subclinical leaks: a clinical and radiologic study. Dis Colon Rectum 49: 1611-1619.
- Bruce J, Krukowski ZH, Al-Khairy G, Russell EM, Park KG (2001) Systematic review of the definition and measurement of anastomotic leak after gastrointestinal surgery(消化管手術後の吻合部リークの定義と測定に関する体系的レビュー). Br J 外科 88: 1157-1168。
- Guillem JG, Cohen AM (1999) Current issues in colorectal cancer surgery. Semin Oncol 26: 505-513.
- Leester B, Asztalos I, Polnyib C (2002) Septic complications after low anterior rectal resection — Is diverting stoma still justified? Acta Chir Iugosl 49: 67-71.
- Power N, Atri M, Ryan S, Haddad R, Smith A (2007) CT assessment of anastomotic bowel leak(吻合部腸管漏出のCT評価). Clin Radiol 62: 37-42.
- Nicksa GA, Dring RV, Johnson KH, Sardella WV, Vignati PV, et al. (2007) Anastomotic Leaks: What is the best diagnostic imaging study? Dis Colon Rectum 50: 197-203.
- Kalady MF, Mantyh CR, Petrofski J, Ludwig KA (2008) Routine contrast imaging of low pelvic anastomosis prior to closure of defunctioning iileostomy: is it necessary? J Gastrointest Surg 12: 1227-1231.
- Khair G, Alhamarneh O, Avery J, Cast J, Gunn J, et al. (2007) Routine use of gastrograffin enema prior to the reversal of a loop Iileostomy. Dig Surg 24: 338-341.
- Akyol AM, McGregor JR, Galloway DJ, George WD (1992) Early postoperative contrast radiology in the assessment of colorectal anastomotic integrity. Int J Colorectal Dis 7: 141-143.
- Goligher JC, Graham NG, De Dombal FT (1970) Anastomotic dehiscence after anterior resection of rectum and Sigmoid. Br J Surg 57: 109-118。
- Haynes IG, Goldman M, Silverman SH, Alexander-Williams J, Keighley MR (1986) The Water-soluble contrast enema after colonic anastomosis. Br J Surg 69: 714-717.
- Khoury W, Ben-Yehuda A, Ben-Haim M, Klausner JM, Szold O (2009) Abdominal Computed Tomography for diagnosing postoperative lower gastrointestinal tract Leaks(術後下部消化管漏出診断のための腹部コンピュータ断層撮影). J Gastrointest Surg 13: 1454-1458.
- Doeksen A, Tanis PJ, Wüst AF, Vrouenraets BC, van Lanschot JJ, et al. (2008) Radiological evaluation of colorectal anastomoses(大腸吻合部の放射線評価). Int J Colorectal Dis 23: 863-868.