Ebben a sorozatban Colin Baker a Bedford Schoolból látványos bemutatókat tart, amelyek célja, hogy megragadja a diákok fantáziáját. A bemutatók könnyen elkészíthetők, biztonságosan eloszthatók és működnek.
Semmi sem szokta annyira bevésni az elmébe a kémiai tényeket, mint érdekes kísérletek bemutatása – Samuel Parkes, 1816
1931 szeptemberében Wallace Carothers amerikai kémikus, aki a DuPont laboratóriumaiban dolgozott, a gyapjú kémiai szerkezetének megértésén alapuló, polimereknek nevezett “óriás” molekulák kutatásáról számolt be. Munkája középpontjában egy olyan szál állt, amelyet egyszerűen “66”-nak neveztek, amely szám a molekulaszerkezetéből származott. 1935-re megszületett a nylon, a “csodaszál”, amely hatalmas sikert aratott kezdeti piacán, a női harisnyák piacán. Amikor az USA 1941 decemberében belépett a II. világháborúba, a Haditermelési Tanács a teljes nejlongyártást katonai felhasználásra irányította elő, beleértve az ejtőernyőket és a B29-es bombázók gumiabroncsait.

Forrás:

Source: Colin Baker
A dekan-dioil-diklorid és az 1,6-diaminohexán
A diaksav-klorid szerves oldószerben keverhetetlen réteget képez egy alifás diaminnal vízben. A határfelületen, ahol a két színtelen oldat találkozik, fehér, hosszú láncú polimer keletkezik. Ez a polimerfilm lehúzható a határfelületről, és eltávolításkor azonnal kicserélődik. Ha abbahagyjuk a húzást, látszólag semmi sem történik – a reakció leáll, de azonnal folytatódik, ha újra elkezdjük a húzást. A reakció több órán keresztül is lejátszódhat.

forrás: Colin Baker
Kit
- Ciklohexán, 100cm3 (irritáló, könnyen gyúlékony);
- Dekanidioil-diklorid, 5.0cm3;
- Desztillált víz, 100cm3;
- Vízmentes nátrium-karbonát, 10g;
- 1,6-diaminohexán, 5.0g;
- Két főzőpohár, 250cm3;
- Pohár, 5cm3;
- Pincér;
- Üvegrudak.
Védelem
A dekanidioil-diklorid és az 1,6-diaminohexán maró hatású. Lenyelve vagy belélegezve károsak, bőrrel érintkezve égési sérüléseket okoznak. Súlyosan irritáló hatásúak. A ciklohexán erősen gyúlékony és irritáló hatású.
Eljárás
Készítse el a következő két oldatot:
A oldat: dekándioil-diklorid ciklohexánban. Tegyünk 100 cm3 ciklohexánt egy 250 cm3-es főzőpohárba, adjunk hozzá 5,0 cm3 dekan-dioil-dikloridot, és keverjük meg, hogy feloldódjon. Ez az oldat körülbelül négy hétig eltartható.
B oldat: 1,6-diaminohexán vizes nátrium-karbonátban. Tegyünk 100 cm3 desztillált vizet egy 250 cm3-es főzőpohárba, adjunk hozzá 10 g vízmentes nátrium-karbonátot és keverjük meg, hogy feloldódjon. Adjunk hozzá 5,0 g szilárd 1,6-diaminohexánt, és keverjük meg, hogy feloldódjon.
Öntsünk 2 cm3 A oldatot egy 5 cm3-es főzőpohárba. Óvatosan adjunk hozzá ugyanannyi mennyiségű B oldatot. Az A oldat tartalmazza a szerves oldószert, sűrűbb, mint a vizes réteg, ezért ez az alsó réteg. Fogja meg csipesszel a két oldat határfelületén képződni kezdő poliamidfilmet (fehér szilárd anyag), és lassan húzza ki a főzőpohárból. Tekerjük a szálakat egy üvegrúd köré, és folytassuk a húzást. Állítsa le a folyamatot, amikor az egyik reaktáns elfogyott.
Speciális tippek
Vigyázni kell a második oldat hozzáadásakor, hogy elkerüljük a keveredést. Mutassuk be, hogyan lehet a szálakat egy folyamatos szálban kihúzni, majd rendezzünk versenyt, hogy melyik tanulópár tudja a leghosszabb szálakat előállítani. Képesnek kell lenniük akár 5 métert is előállítani, mielőtt a szál elszakad. Gyorsan rájönnek, hogy segítségre van szükségük a szál megtámasztásához – az osztályt két nagy csoportra osztom, amelyek mindegyike üvegrudakkal van felfegyverkezve. A tanítványaim több mint 30 méteres szálakat is készítettek, és még a sarkokat is megpróbálták megkerülni. Az egyes oldatok maximális térfogatát 10 cm3 -re kell korlátozni. A tanulóknak kesztyűt kell viselniük, és kerülniük kell a szálakkal való érintkezést. Ha a szál elpattan, akkor nedvszívó papírba kell csomagolni. Minden kiömlött folyadékot fel kell törölni nedvszívó papírral, és a hulladékba kell tenni.
Tanítási célok
A poliamidok olyan polimerek, amelyekben az ismétlődő egységeket amidkötések, -CO-NH- tartják össze.
Nylon-6,10
A Nylon-6,10 két monomerből áll, az egyik hat, a másik 10 szénatomot tartalmaz – innen a neve. A 10 szénatomos monomer a dekándioil-diklorid (ClOC(CH2)8 COCl), egy savas klorid, amelynek mindkét végén egy -COCl csoport található. A másik monomer egy hat szénatomos lánc, amelynek mindkét végén egy-egy aminocsoport, -NH2 található. Ez az 1,6-diaminohexán (H2 N(CH2)6 NH2, más néven hexán-1,6-diamin).
Amikor ez a két vegyület polimerizálódik, az amin- és savcsoportok egyesülnek, minden alkalommal egy molekula hidrogén-klorid elvesztésével:
n ClOC-(CH2)8-COCl + n H2N-(CH2)6-NH2 → -(CO-(CH2)8-CONH-(CH2)6-NH)n – + n HCl
Ezt a kis molekula elvesztésével járó polimerképző folyamatot nevezzük kondenzációs polimerizációnak.
Nylon-6,6
Ez a polimer két hat szénatomos molekula, a hexandionsav és az 1,6-diaminohexán kondenzációjával jön létre. Az iparban mindkét monomer előállításához ciklohexánt használnak. Ha a ciklohexánt oxidálják, a gyűrű kinyílik, és a lánc mindkét végén egy-egy savcsoport található – hexandionsav keletkezik. Ha ezt a savat ammóniával semlegesítjük, a diammóniumsó (NH4 OOCCH2 CH2 CH2 CH2 CH2 COONH4) keletkezik, amely dehidratálható (350 °C-ra hevítéssel) és redukálható (H2/Ni felhasználásával) 1,6-diaminohexánná. A diaksav és a diamin kondenzációs polimerizációja vízveszteséggel történik:
n HOOC-(CH2)4 -COOH + n H2 N-(CH2)6 -NH2 → -(CO-(CH2)4 -CONH-(CH2)6 -NH)n – + n H2 O
Nylon-6
Az egyetlen monomer kaprolaktámból (hexahidro-2H-azepin-2-on, 1) nylon készíthető.
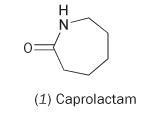
A kaprolaktám egy belső amidkötést tartalmaz. Ennek a molekulának a polimerizációja gyűrűnyílást és folyamatos láncot alkotó összekapcsolódást eredményez:
-(NH-(CH2)5 -CONH-(CH2)5 -CONH-(CH2)5 -CO)n –
A neylon forradalmasította a textilipart, és számos mai modern, szintetikus szál előfutára volt. Továbbra is fontos és széles körben használt anyag a gyártásban.