Generikus név: fluocinonid
Adagolási forma: Gél
A Drugs.com által orvosilag felülvizsgált. Utolsó frissítés: 2020. június 22.
- Áttekintés
- Mellékhatások
- Adagolás
- Szakmai
- Ellenyomások
- Tovább
Kizárólag orvosi rendelés
A Lidex márkanév megszűnt az USA-ban.S. Ha a készítmény generikus változatait az FDA engedélyezte, előfordulhat, hogy rendelkezésre állnak generikus megfelelői.
- Lidex leírása
- Lidex – Klinikai farmakológia
- Farmakokinetika
- A Lidex indikációi és alkalmazása
- Ellenejavallatok
- Figyelmeztetések
- Általános
- Tájékoztatás a betegnek
- Laborvizsgálatok
- Karcinogenezis, mutagenezis és a termékenység károsodása
- C kategóriájú terhesség
- Szoptató anyák
- GYermekkori alkalmazás
- Mellékhatások
- Túladagolás
- Lidex adagolás és alkalmazás
- Hogyan kerül forgalomba a Lidex
- Gyakori kérdések
- Több információ a Lidexről (fluocinonid helyileg alkalmazható)
- Fogyasztói források
- Szakmai források
- Kapcsolódó kezelési útmutatók
Lidex leírása
A Lidex® (fluocinonid) 0,05%-os gél helyileg történő alkalmazásra szolgál. Hatóanyaga a kortikoszteroid fluocinonid, amely a fluocinolon-acetonid 21-acetát észtere és kémiai neve pregna-1,4-dién-3,20-dion,21-(acetiloxi)-6,9-difluor-11-hidroxi-16,17–,(6α,11β,16α)-. A következő kémiai szerkezettel rendelkezik:
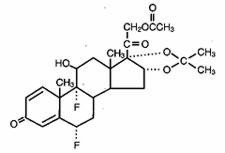
A Lidex gél 0,5 mg/g fluocinonidot tartalmaz egy speciálisan összeállított gélalapban, amely karbomer 940-ből, edetát-dinátriumból, popil-gallátból, propilén-glikolból, nátrium-hidroxidból és/vagy sósavból (a pH beállításához) és vízből (tisztított) áll. Ez a tiszta, színtelen, tixotróp vivőanyag zsírtalan, nem színez és teljesen vízzel keverhető.
Ebben a készítményben a hatóanyag teljesen oldatban van.
Lidex – Klinikai farmakológia
A helyi kortikoszteroidok gyulladáscsökkentő, viszketéscsillapító és érösszehúzó hatásúak.
A helyi kortikoszteroidok gyulladáscsökkentő hatásának mechanizmusa nem egyértelmű. A helyi kortikoszteroidok hatáserősségének és/vagy klinikai hatékonyságának összehasonlítására és előrejelzésére különböző laboratóriumi módszereket alkalmaznak, beleértve az érszűkítő vizsgálatokat is. Bizonyos bizonyítékok arra utalnak, hogy emberben felismerhető összefüggés van az érösszehúzó hatáserősség és a terápiás hatékonyság között.
Farmakokinetika
A helyi kortikoszteroidok perkután felszívódásának mértékét számos tényező határozza meg, beleértve a hordozót, az epidermális gát épségét és az okkluzív kötések használatát.
A helyi kortikoszteroidok felszívódhatnak a normál, ép bőrből. A bőr gyulladása és/vagy más betegségfolyamatok fokozzák a perkután felszívódást. Az okkluzív kötések jelentősen növelik a helyi kortikoszteroidok perkután felszívódását. Így az okkluzív kötések értékes terápiás kiegészítői lehetnek a rezisztens dermatózisok kezelésének (lásd ADAGOLÁS ÉS BEADAGOLÁS).
A bőrön keresztül történő felszívódás után a lokális kortikoszteroidok a szisztémásan beadott kortikoszteroidokhoz hasonló farmakokinetikai utakon keresztül kezelhetők. A kortikoszteroidok különböző mértékben kötődnek a plazmafehérjékhez. A kortikoszteroidok elsősorban a májban metabolizálódnak, majd a vesén keresztül kiválasztódnak. A helyi kortikoszteroidok és metabolitjaik egy része az epébe is kiválasztódik.
A Lidex indikációi és alkalmazása
A Lidex gél a kortikoszteroidokra reagáló bőrbetegségek gyulladásos és viszkető megnyilvánulásainak enyhítésére javallt.
Ellenejavallatok
A topikális kortikoszteroidok ellenjavallt azoknál a betegeknél, akiknél a készítmény bármely összetevőjével szemben túlérzékenység áll fenn.
Figyelmeztetések
Általános
A helyi kortikoszteroidok szisztémás felszívódása egyes betegeknél reverzibilis hipotalamusz-hypophysis-mellékvese (HPA) tengely szupressziót, a Cushing-szindróma megnyilvánulásait, hiperglikémiát és glükozuriát okozott.
A szisztémás felszívódást fokozó körülmények közé tartozik a hatásosabb szteroidok alkalmazása, a nagy felületen történő alkalmazás, a hosszan tartó alkalmazás és az okkluzív kötések hozzáadása.
Ezért a nagy felületen vagy okkluzív kötés alatt alkalmazott nagy dózisú, hatásos helyi szteroidot kapó betegeket rendszeresen értékelni kell a HPA tengely szuppressziójának bizonyítékai szempontjából a vizelet szabad kortizol és ACTH stimulációs tesztek alkalmazásával. Ha a HPA-tengely szuppresszióját észlelik, meg kell kísérelni a gyógyszer visszavonását, az alkalmazás gyakoriságának csökkentését vagy egy kevésbé hatékony szteroid helyettesítését.
A HPA-tengely működésének helyreállítása általában gyors és teljes a gyógyszer abbahagyását követően. Ritkán előfordulhatnak a szteroid megvonás jelei és tünetei, amelyek kiegészítő szisztémás kortikoszteroidok alkalmazását teszik szükségessé.
A gyermekek arányosan nagyobb mennyiségű lokális kortikoszteroidot szívhatnak fel, és így érzékenyebbek lehetnek a szisztémás toxicitásra (lásd: ÓVALMASZKODÁSOK – Gyermekkori alkalmazás). Ha irritáció alakul ki, a helyi kortikoszteroidokat abba kell hagyni és megfelelő terápiát kell alkalmazni.
Mint minden helyi kortikoszteroid készítmény esetében, a hosszan tartó alkalmazás a bőr és a bőr alatti szövetek sorvadását okozhatja. Az intertriginális vagy hajlító területeken, illetve az arcon történő alkalmazás esetén ez még rövid távú alkalmazás esetén is előfordulhat.
Bőrgyógyászati fertőzések jelenlétében megfelelő gombaölő vagy antibakteriális szer alkalmazását kell megkezdeni. Ha nem jelentkezik azonnal kedvező válasz, a kortikoszteroidot abba kell hagyni mindaddig, amíg a fertőzést nem sikerül megfelelően kontrollálni.
Tájékoztatás a betegnek
A helyi kortikoszteroidokat alkalmazó betegeknek a következő információkat és utasításokat kell kapniuk:
- Ezt a gyógyszert az orvos utasításai szerint kell alkalmazni. Kizárólag külsőleg alkalmazható. Kerülje a szemmel való érintkezést.
- A betegeknek azt kell tanácsolni, hogy ezt a gyógyszert ne használják más betegségre, mint amire felírták.
- A kezelt bőrfelületet nem szabad bekötözni vagy más módon lefedni vagy becsomagolni, hogy okkluzív legyen, kivéve, ha az orvos utasítása szerint.
- A betegeknek jelenteniük kell a helyi mellékhatások minden jelét, különösen az okkluzív kötés alatt.
- A gyermekbetegek szüleinek azt kell tanácsolni, hogy ne használjanak szűk pelenkát vagy műanyag nadrágot a pelenkás területen kezelt gyermeken, mivel ezek a ruhadarabok okkluzív kötésnek minősülhetnek.
Laborvizsgálatok
A következő vizsgálatok hasznosak lehetnek a HPA tengely szuppressziójának értékelésében:
Vizelet szabad kortizol teszt
ACTH stimulációs teszt
Karcinogenezis, mutagenezis és a termékenység károsodása
Hosszú távú állatkísérleteket nem végeztek a helyi kortikoszteroidok karcinogén potenciáljának vagy a termékenységre gyakorolt hatásának értékelésére.
A prednizolon és hidrokortizon mutagenitásának meghatározására végzett vizsgálatok negatív eredményeket mutattak.
C kategóriájú terhesség
A kortikoszteroidok általában teratogének laboratóriumi állatokban, ha szisztémásan, viszonylag alacsony dózisban adják őket. Az erősebb kortikoszteroidokról kimutatták, hogy teratogén hatásúak a laboratóriumi állatok bőrön történő alkalmazása után. Terhes nőkön nem állnak rendelkezésre megfelelő és jól ellenőrzött vizsgálatok a helyileg alkalmazott kortikoszteroidok teratogén hatásairól. Ezért a helyi kortikoszteroidok csak akkor alkalmazhatók terhesség alatt, ha a lehetséges előnyök igazolják a magzatra jelentett lehetséges kockázatot. Az ebbe az osztályba tartozó gyógyszerek nem alkalmazhatók kiterjedten, nagy mennyiségben vagy hosszabb ideig terhes betegeken.
Szoptató anyák
Nem ismert, hogy a kortikoszteroidok helyileg történő alkalmazása elegendő szisztémás felszívódást eredményezhet-e ahhoz, hogy kimutatható mennyiség kerüljön az anyatejbe. A szisztémásan alkalmazott kortikoszteroidok olyan mennyiségben választódnak ki az anyatejbe, amely valószínűleg nem gyakorol káros hatást a csecsemőre. Ennek ellenére óvatosságot kell tanúsítani, ha szoptatós nőnek helyileg alkalmazott kortikoszteroidokat adnak.
GYermekkori alkalmazás
A gyermekkori betegek nagyobb érzékenységet mutathatnak a helyileg alkalmazott kortikoszteroidok által kiváltott HPA-tengely szuppresszióra és Cushing-szindrómára, mint az érett betegek, mivel a bőrfelület és a testtömeg aránya nagyobb.
Hypothalamus-hipofízis-mellékvese (HPA) tengely szuppressziójáról, Cushing-szindrómáról és intrakraniális hipertóniáról számoltak be lokális kortikoszteroidokat kapó gyermekeknél. A mellékvesekéreg-szuppresszió megnyilvánulásai közé tartozik a lineáris növekedési elmaradás, a késleltetett súlygyarapodás, az alacsony plazma kortizolszint és az ACTH-stimulációra adott válasz hiánya. Az intrakraniális hipertónia megnyilvánulásai közé tartoznak a kidudorodó fontanellák, a fejfájás és a kétoldali papillödéma.
A helyi kortikoszteroidok gyermekeknek történő adását a hatékony terápiás kezeléssel összeegyeztethető legkisebb mennyiségre kell korlátozni. A krónikus kortikoszteroidterápia befolyásolhatja a gyermekek növekedését és fejlődését.
Mellékhatások
A helyi kortikoszteroidokkal kapcsolatban ritkán számoltak be a következő helyi mellékhatásokról, de gyakrabban fordulhatnak elő okkluzív kötések alkalmazásával. Ezek a reakciók az előfordulásuk megközelítőleg csökkenő sorrendjében vannak felsorolva:
| Égés | Periorális dermatitis | |
| Jegesedés | Allergiás kontakt dermatitis | |
| Irritáció | Bőrkeményedés | |
| Szárazság | Szekunder fertőzés | |
| Follikulitis | Bőrsorvadás | Bőrsorvadás |
| Hypertrichosis | Striae | |
| Acneiform eruptions | Miliaria | |
| Hypopigmentáció |
Túladagolás
A topikálisan alkalmazott kortikoszteroidok elegendő mennyiségben felszívódhatnak ahhoz, hogy szisztémás hatást fejtsenek ki (lásd: ÓVALÓSÍTÁSOK).
Lidex adagolás és alkalmazás
A Lidex gélt az állapot súlyosságától függően általában naponta kétszer-négyszer vékony filmként kell felvinni az érintett területre.
Okkluszív kötés alkalmazható a pikkelysömör vagy a recalcitráns állapotok kezelésére.
Ha fertőzés alakul ki, az okkluzív kötés használatát abba kell hagyni és megfelelő antimikrobiális terápiát kell indítani.
Hogyan kerül forgalomba a Lidex
A Lidex® (fluocinonid) gél 0.05%-os kiszerelésben
15 g-os tubus – NDC 99207-507-13
30 g-os tubus – NDC 99207-507-14
60 g-os tubus – NDC 99207-507-17
15°-30°C (59°-86°F) hőmérsékleten kell tárolni.
Az alábbi célokra gyártott:
MEDICIS, The Dermatology Company®
Scottsdale, AZ 85258
Aprilis 2001
IN-5071/S
| Lidex fluocinonid gél |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Címkéző – MEDICIS
Gyakori kérdések
- Hajhullásra használják?
- Mivel helyettesíthető a fluocinonid krém?
- A fluocinonid gombaölő krém?
- Meddig kell használni a fluocinonidot?
- Mire jó a fluocinonid krém?
- A fluocinonid alkalmazható mérges szömörce kiütés kezelésére?
- Az egy szteroid?
- Az egy antibiotikum?
Több információ a Lidexről (fluocinonid helyileg alkalmazható)
- Mellékhatások
- Terhesség vagy szoptatás alatt
- Adagolási információk
- Meghatások a gyógyszerekkel
- 8 értékelés
- Generikus elérhetőség
- A gyógyszercsoport:
Fogyasztói források
- Továbbképzés
- Lidex Mild (továbbképzés)
- Lidex Regular (továbbképzés)
Szakmai források
- Receptköteles információk
- Lidex helyi oldat (FDA)
- Lidex kenőcs (FDA)
Egyéb márkák Vanos, Lidex-E
Kapcsolódó kezelési útmutatók
- Atopikus bőrgyulladás
- Eczema
- Dermatitis
- Psoriasis
Egészségügyi nyilatkozat