Az Org 2-ben az “aminok” témakörével kapcsolatban a következő a helyzet: nincs elbeszélés.
A legtöbb fejezettel ellentétben nem egy sor fogalommal kezdődik, és nem épül fel egy sor példára, amelyekre aztán alkalmazhatod ezeket a fogalmakat.
Nem. Az aminokról szóló tipikus fejezet egy bevezető tankönyvben lényegében csak látszólag véletlenszerűen összedobott témák összevisszasága, amelyek máshová nem illettek. Az egyetlen egységesítő szál az, hogy valamilyen módon nitrogént tartalmaznak.
Egy példa: a mai random aminokról szóló bejegyzésünk a Hofmann- és Curtius-átrendeződésekről szól.
Mi késztet erre, kérdezhetnéd? Nincs jó válasz. A legtöbb kurzus foglalkozik velük valamikor, és valahol bele kell férniük. Szóval mi a fene. Miért ne most?
Tartalomjegyzék
- A Hofmann és Curtius átrendeződések
- A Hofmann és Curtius átrendeződések mechanizmusa, Első rész – Az átrendeződés felállítása
- Második rész: A legfontosabb átrendeződési lépés a Hofmann és Curtius átrendeződésekben
- Harmadik rész:
- A lépések összerendezése
- Az izocianát sorsa: Karbamátok, aminok és karbamidok képződése
- Összefoglaló: A Hofmann- és Curtius-átrendeződések
- Jegyzetek
- (Haladó) hivatkozások és további olvasmányok
- A Hofmann- és Curtius-átrendeződések
- A Hofmann- és Curtius-átrendeződések mechanizmusa, 1. rész: Az átrendeződés felállítása
- 1. rész: Előjáték
- 3. A legfontosabb átrendeződési lépés a Hofmann és a Curtiusban
- Izocianát képződése
- A lépések összeillesztése
- Az izocianát sorsa
- Összefoglaló: A Hofmann- és Curtius-átrendeződések
- Jegyzetek
- (Advanced) References and Further Reading
A Hofmann- és Curtius-átrendeződések
A Hofmann- és Curtius-átrendeződések két példája az átrendeződési reakciók egész családjának, amelyeknek közös mechanikai lépésük van.
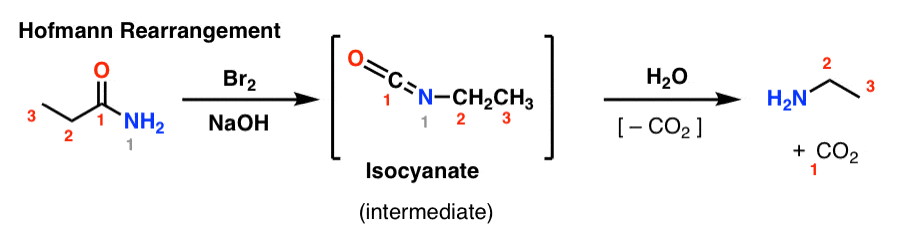
A Hofmann-átrendeződésben egy amidot brómmal és bázissal (általában NaOH vagy KOH) kezelünk. Hevítéskor egy köztes izocianát keletkezik, amelyet nem izolálnak. Víz jelenlétében az izocianát szén-dioxidot veszít (“dekarboxilálódik”), amin keletkezik.
A Hofmann-átrendeződésben kialakuló kulcsfontosságú kötés a C2-N kötés. Figyeljük meg, hogy a karbonilcsoport (C1) elveszik, szén-dioxidot (CO2) képezve. (megjegyzés: ez nem IUPAC számozás, csak számozás a vita megkönnyítése érdekében)
A Curtius-átrendeződésben egy acilazidot hevítünk, és izocianát keletkezik. A Curtius-átrendezésnél az izocianát izolálható, de általában tovább alakul más fajokká, például karbamáttá, karbamiddá, vagy (dekarboxiláció útján, mint a Hofmann-rendezésnél) aminná (ezekről bővebben alább).
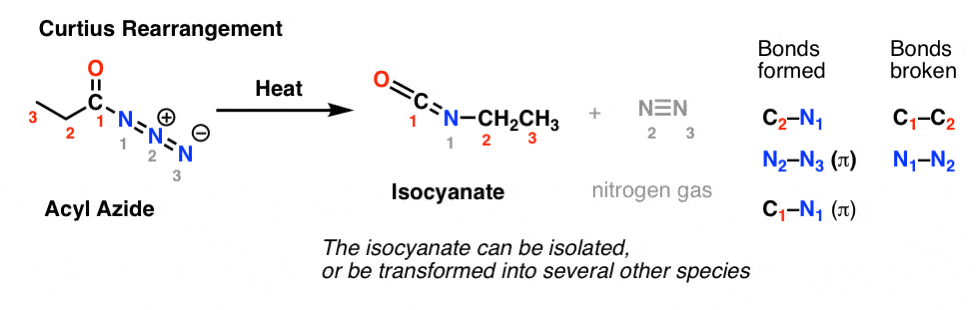
A legfontosabb megfigyelés, amit mindkét esetben meg kell jegyezni, hogy a C1-C2 kötés megszakadt, és egy új C2-N kötés jött létre.
A kérdés az, hogy HOGYAN?
A Hofmann- és Curtius-átrendeződések mechanizmusa, 1. rész: Az átrendeződés felállítása
A Curtius- és Hofmann-átrendeződések mechanizmusának négy fontos része van, és most mindegyiken végigmegyünk.
- Előzetes (egyszerű)
- A kulcsfontosságú migrációs lépés (trükkös, de kevésbé trükkös, ha rájössz, hogy ennek egy változatát már láttad az Org 1-ben !)
- Az izocianát képződése (egyszerű)
4. Epilógus: Az izocianát átalakulásai
1. rész: Előjáték
- A Hofmann-átrendeződés egy amiddal történik.
- A Curtius-átrendeződés egy acilaziddal történik.
Mindkettő kényelmesen előállítható acilhalogenidekből addíciós-eliminációs reakcióval. Ha most az aminokkal foglalkozunk, akkor a karbonilreakciók valószínűleg ismerős terület. Az acilhalogenideket karbonsavakból állíthatjuk elő olyan reagenssel, mint a tionil-klorid (SOCl2) vagy a foszfor-pentaklorid (PCl5).
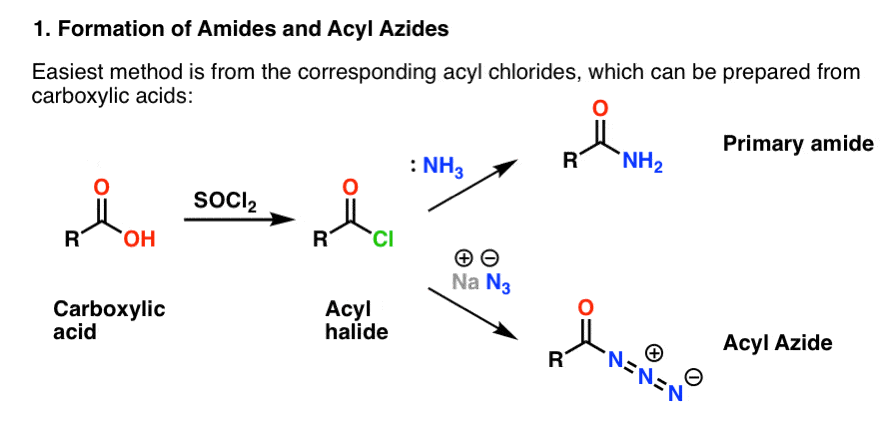
A Hofmann
A Hofmann-átrendeződésben az amidot brómmal (Br2) és egy bázissal, például NaOH-val kezeljük. Ennek eredményeképpen az N-H megbomlik és N-Br képződik, ami egy jó távozó csoport beépülését eredményezi a nitrogénre. Ezt nevezzük “N-brom-amidnak”.
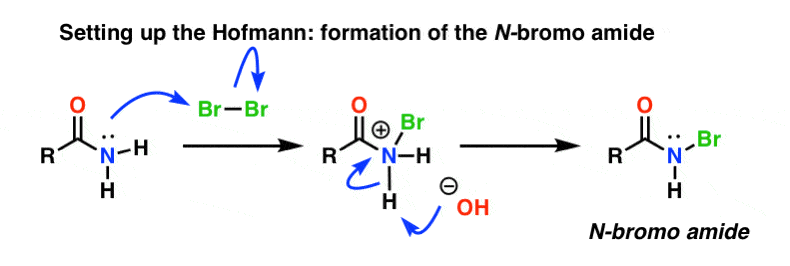
A Curtiusnak nincs szüksége “beállításra”, mivel az acil-azidnak már van egy pompás beépített távozó csoportja: N2. Ezért a szerves azidokkal óvatosan kell bánni, mert a durva kezelés robbanáshoz vezethet.
3. A legfontosabb átrendeződési lépés a Hofmann és a Curtiusban
Most rátérünk a lényegre.
A Hofmann- és Curtius-átrendeződések kulcsfontosságú lépése egy szénatom vándorlása egy szomszédos nitrogénen lévő kilépő csoport kiszorítása érdekében.
Ez két ívelt nyíl megrajzolását igényli, amelyeket a bal szélső bal oldali szerkezetben (lent) láthatunk.
- Az első ívelt nyílban a C-C kötés megszakad, és egy új C-N kötés alakul ki.
- A második ívelt nyílban az N-LG (kilépő csoport) kötés szakad meg.
Nem mindig könnyű azonban a bal oldali szélső szerkezetből közvetlenül a jobb oldali szélső szerkezetbe (amely szépen és rendezetten van megrajzolva! ) átmenni.
A vizsgákon minden évben számtalan pontot veszítenek feleslegesen azok a diákok, akik a görbe nyilakat helyesen rajzolják meg, de végül rossz szerkezetet rajzolnak! Ezért bátorítom a diákokat, hogy először rajzoljanak egy “csúnya változatot”, ami szarul néz ki, de legalább minden kötés a megfelelő helyen van. Később mindig van idő átrajzolni és csinossá tenni.
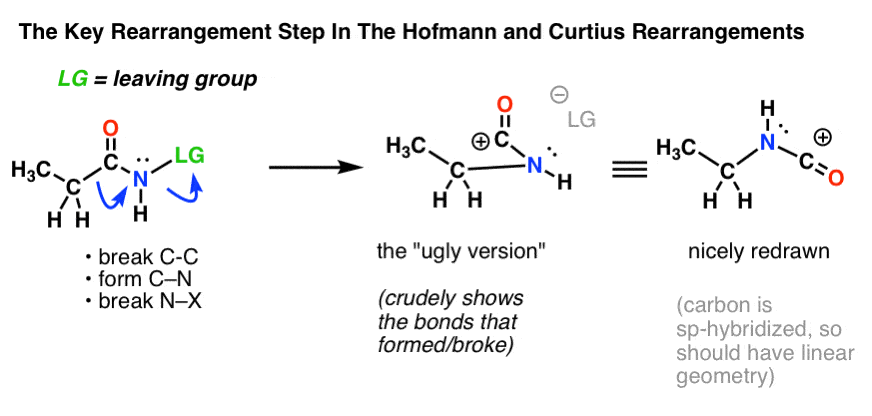
Elsőre ez az átrendeződés valószínűleg… furcsának tűnik. De valójában ez egy olyan reakció, amit már láttál korábban! (csak álcázott formában).
Memlékszik még valaki a hidroboráció-oxidáció “oxidációs” lépésének mechanizmusára?
Gyakorlatilag ugyanerről van szó!
Itt egy kis felfrissítés:
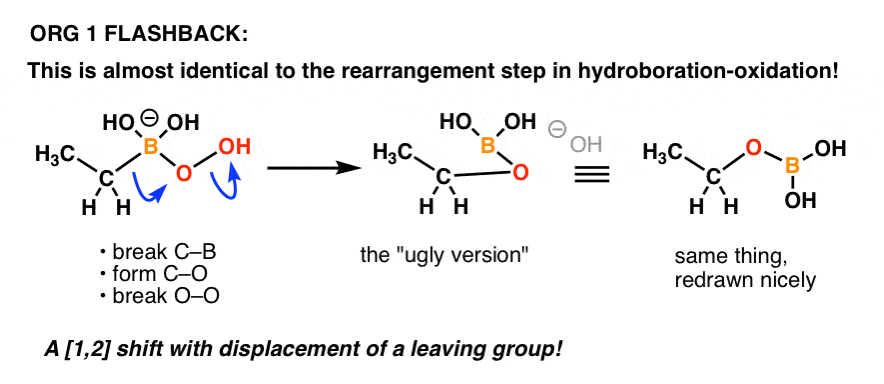
Még egy példa arra, hogy a szerves kémia egy korábbi részében tanult dolgok visszatérhetnek a kurzus egy későbbi részében!
Látogassunk el konkrét példákkal a Hofmann és Curtius átrendeződések konkrét átrendeződési lépéséhez.
Itt a Hofmann kulcslépése, ahol a hevítés hatására C-C bomlás , C-N képződés és N-Br bomlás következik be.
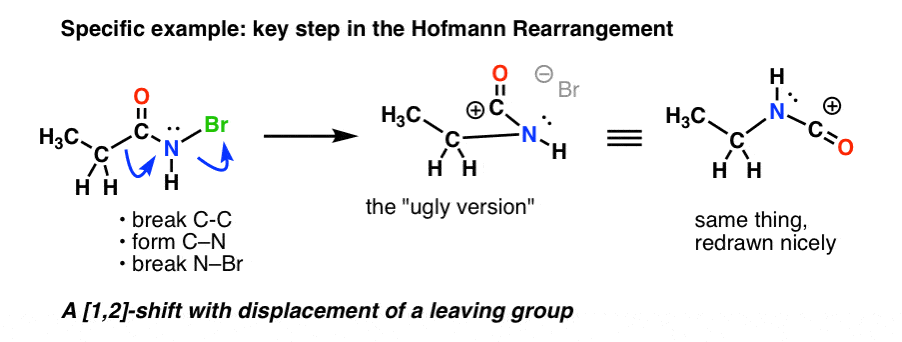
Ha követjük az összes nyilat, akkor egy furcsa kinézetű karbokationt kell kapnunk (jobbra fent), amellyel mindjárt foglalkozunk.
A Curtiusban az acilazid hevítése átrendeződést eredményez. A kilépő csoport a nitrogéngáz (N2).
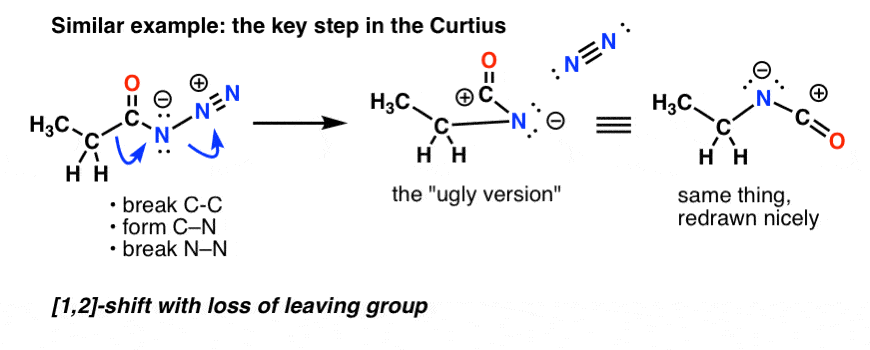
(Egy finom különbség a Curtius és a Hofmann között, hogy a Curtiusban az N-hez nem kapcsolódik hidrogén, így az átrendeződött fajban negatív töltést kapunk a nitrogénen.)
Izocianát képződése
A következő lépés az átrendeződött fajunkból az izocianátba vezet. Aki hozzászokott a rezonanciaformák rajzolásához, annak ez nem lehet túl nehéz.
(Amint azt alább tárgyalni fogjuk, vizsgálatok megállapították, hogy az izocianátképződés a migrációval egy időben történik. De tanítási céljaink szempontjából úgy gondolom, hogy segít, ha ezt a lépést elkülönítve kezeljük. Egy perc múlva össze tudjuk rakni az egészet).
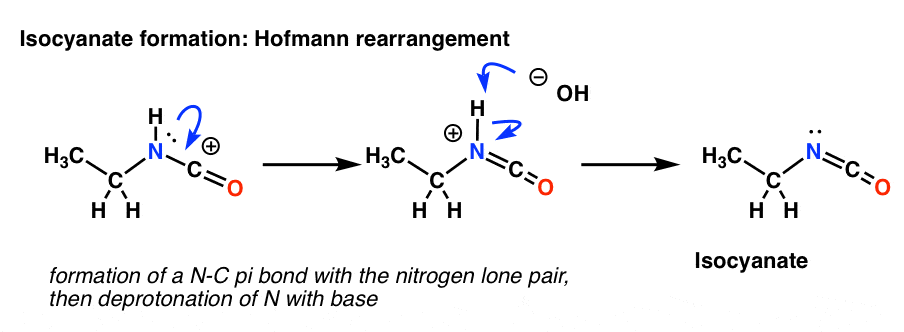
Amint talán emlékeztek a waayyyyyy vissza az Org 1-ből, egy teljes oktettekkel rendelkező rezonanciaforma jobb, mint egy oktett nélküli (gyors áttekintés). Az átrendeződésből származó furcsa kinézetű termékünkben egy karbokation szomszédos egy magányos párt tartalmazó nitrogénnel. Első lépésként tehát egy új C-N pi-kötés kialakulását rajzoljuk meg. Ez lényegében csak egy rezonanciaforma.
A Hofmann-átrendeződés bázis jelenlétében történik. Tehát a rezonanciaforma megrajzolása után a következő lépés az N-H kötés deprotonálása, ami a semleges izocianátot adja.
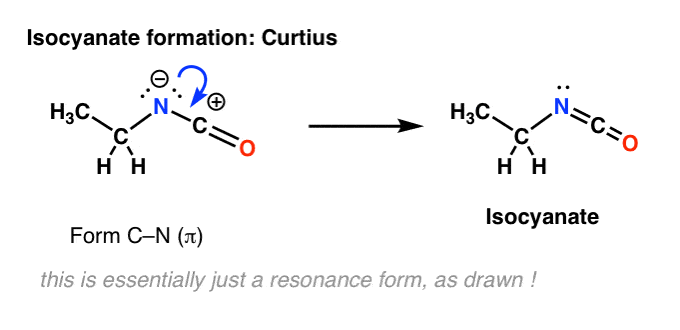
A Curtiusban nincs hidrogén a nitrogénen. Az izocianátképződés tehát pusztán egy magányos pár adományozásával valósul meg a nitrogénről a karbokationra. Tekinthetjük úgy is, mint egy rezonanciaforma rajzolását.
A lépések összeillesztése
A Hofmann- és Curtius-átrendeződések mechanizmusának tanulmányozása során megállapították, hogy ez a két lépés nem egymás után történik, hanem valójában egyszerre! (honnan tudjuk ezt? lásd 1. megjegyzés )
Ez azt jelenti, hogy a migráció az izocianátképződéssel egy időben történik.
Újra kell rajzolnunk a Hofmann és a Curtius mechanizmusát, hogy ezt tükrözze, beépítve mindkét lépést.
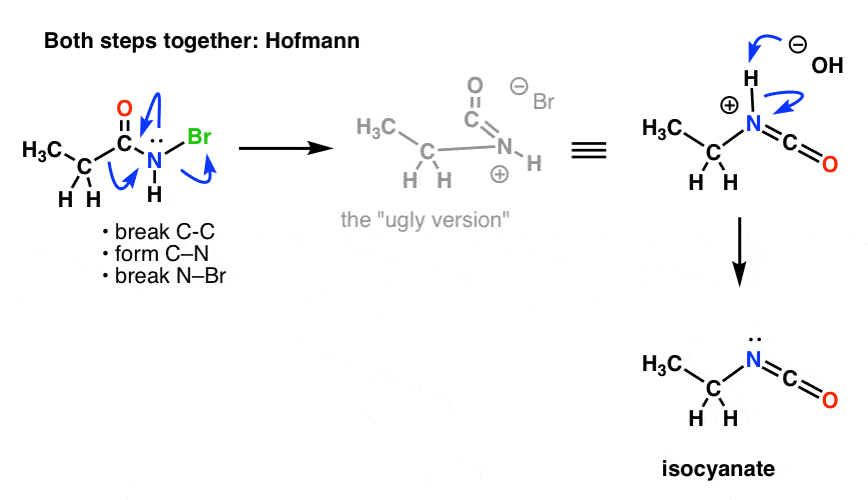
Itt a Hofmann (figyeljük meg, hogy a deprotonálási esemény valójában különálló).
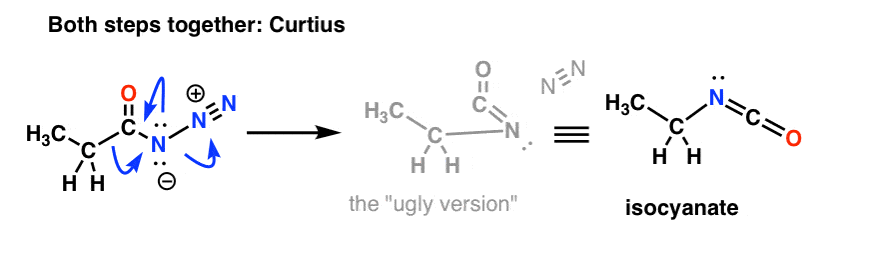
És a Curtius:
Az izocianát sorsa
Mind a Hofmann, mind a Curtius esetében izocianát keletkezik. Valószínűleg még nem találkoztál izocianátokkal. Első pillantásra elég furcsa kinézetű fajok, de kémiai felépítésük nem sokban különbözik más karbonil fajok, például az észterek, amidok és acilhalogenidek kémiai felépítésétől.
Az izocianát szerkezete nagyon hasonlít a szén-dioxid, a CO2 szerkezetére. A szén két erősen elektronegatív atomhoz pi-kötéssel kapcsolódik. Ez teszi a szenet kiváló elektrofillé.
Az izocianátok különböző nukleofilek hozzáadásával más hasznos fajokká alakíthatók át.
– Alkohol hozzáadásával karbamát keletkezik
– Amin hozzáadásával karbamid keletkezik
– Víz hozzáadásával karbaminsav keletkezik, amely instabil. A karbaminsavak gyorsan szén-dioxidot veszítenek, így amin keletkezik.
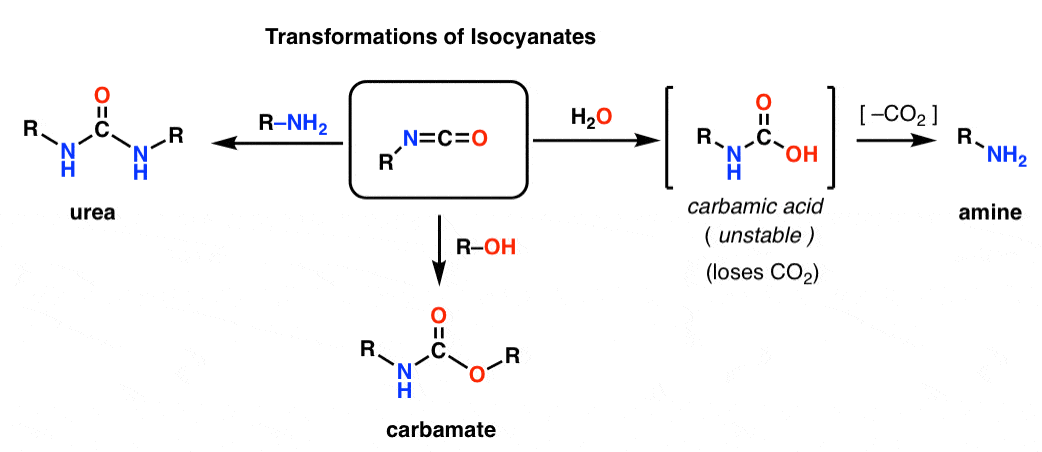
A dekarboxilációs útvonal különösen az aminok előállításának ügyes módját mutatja be. A karbonsavak előállításának rengeteg módját megtanultuk, de az aminok előállításának nem túl sok módját (a nukleofil szubsztitúción és a reduktív amináláson kívül). A Hofmann egy jó trükk, amit a hátsó zsebünkben tarthatunk olyan helyzetekben, amikor egyik sem alkalmazható – mint például szubsztituált anilinek előállítása.
Mechanizmusok? Oké, rendben. Lásd az 1. bónusztémát.
Összefoglaló: A Hofmann- és Curtius-átrendeződések
Ezeknek az átrendeződéseknek a mechanizmusa első pillantásra trükkös, de jelentősen megkönnyíti a dolgot, ha rájössz, hogy a migrációs reakció egy változatát már láttad korábban (pl.pl. a hidroboráció-oxidációban).
Azt ajánlom, hogy először a csúnya változatot rajzoljuk meg, mert ez segít abban, hogy a kialakuló és felbomló kötések meglátására koncentráljunk, mielőtt megpróbálnánk átrajzolni egy esztétikusabb szerkezetbe. Ez vonatkozik a Beckmann- és Wolff-átrendeződésekre is, amelyek hasonló lépést tartalmaznak (lásd alább)
Jegyzetek
Bónusz 1. téma: Izocianátok
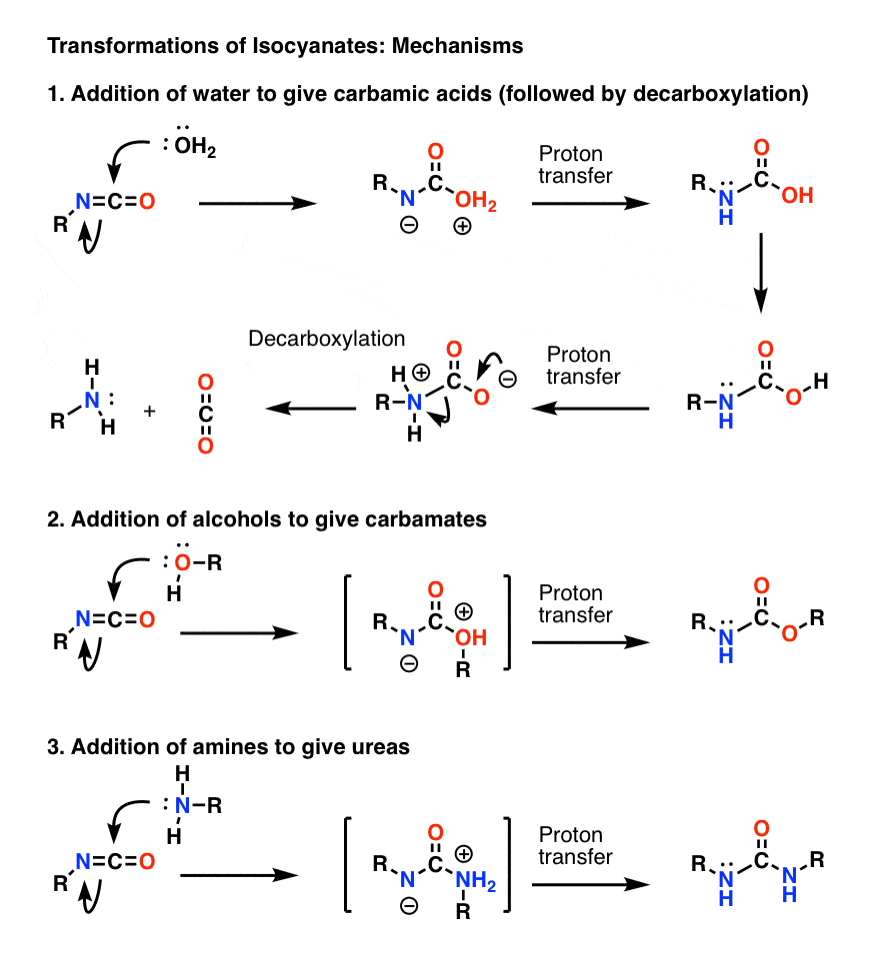
Az izocianátok legfontosabb mechanizmusa az elektrofil addíció (azaz egy nukleofil hozzáadása a központi, elektrofil szénhez). Az alábbi mechanizmusban a nukleofil hozzáadását a szénhez úgy mutattam be, hogy a nitrogénen anion képződik, bár valószínűleg nem ez a legjobb rezonanciaforma (az oxigén jobban stabilizálja a negatív töltést, mint a nitrogén). Az oxigénről a nitrogénre történő protonátadás semleges fajt eredményez. (Itt a Protonátvitel varázspálcáját használtam, mert az gyorsabb).
Megjegyezzük, hogy az 1) pontban szereplő dekarboxilezési lépést nem kell megelőznie az oxigén deportálásának, bár mindenképpen úgy kell történnie, hogy a lépés során a nitrogén protonálódjon (nem akarunk például erősen bázikus amidiont képezni).
Bónusz 2. téma: A Beckmann-, Wolff- és más átrendeződések hasonló lépéssel rendelkeznek
De várjunk csak, van még más is!
A Beckmann-átrendeződésben van egy 1,2-eltolódás egy távozó csoport elvesztésével. A kulcslépés lényegében ugyanaz, mint amit a Hofmann és Curtius átrendeződésben láttunk.
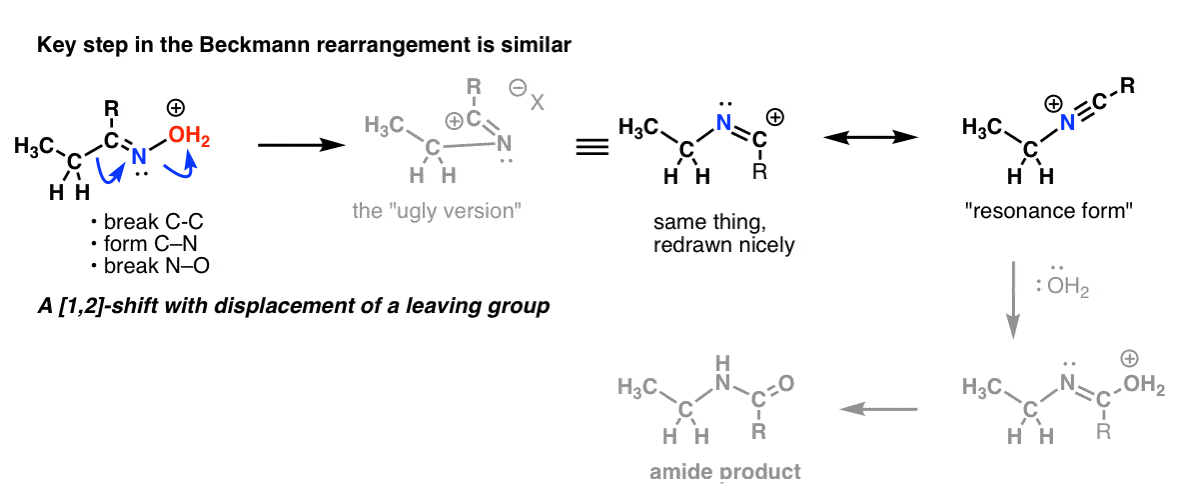
És a Wolff átrendeződésben, amit szintén gyakran tárgyalnak, ugyanezt a kulcslépést ismerhetjük fel.
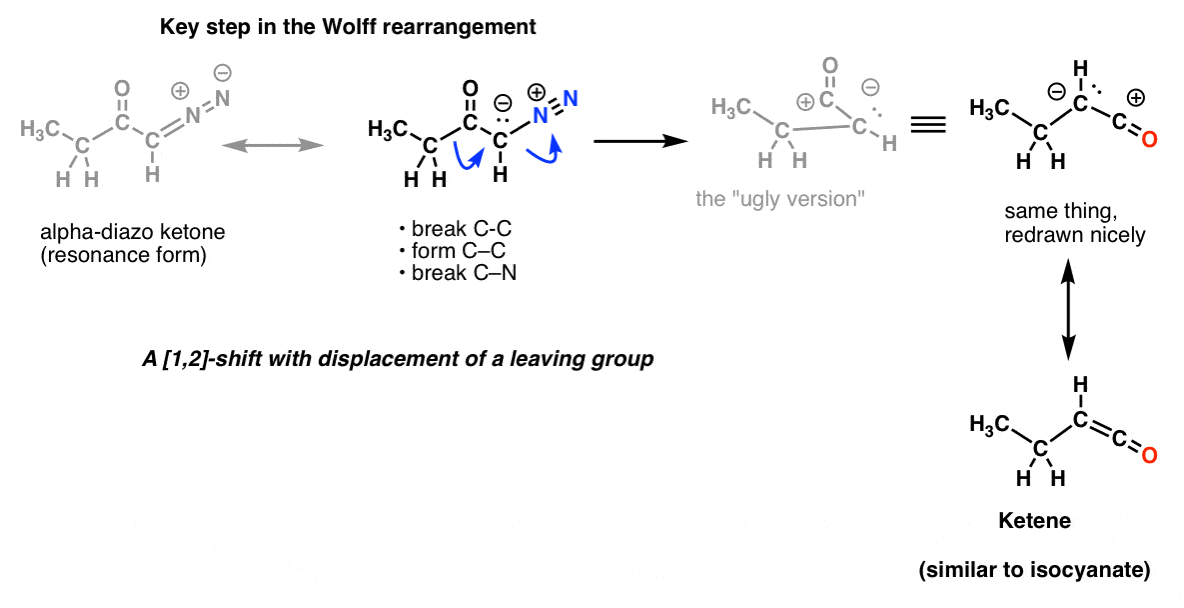
És ez még nem minden! Van egy Schmidt-átrendeződésnek nevezett reakció, amely a Curtius-féle, de HN3 hozzáadásával jön létre egy acil-kloridhoz (vagy karbonsavhoz). És van egy másik, a Lossen átrendeződés, amely hidroxi-aminsavakkal történik. A két folyamat kulcslépését nem kell kitalálni. És még nem is említettük a Baeyer-Villiger-átrendeződést, amely nem nitrogénnel történik, de nagyjából ugyanolyan típusú folyamat.
Amikor sok holddal ezelőtt megtanultam a hidroborálás-oxidáció lépését az Org 1-ben, biztosan nem számítottam arra, hogy ugyanaz a reakcióminta ennyi különböző formában ismétlődik majd meg.
A lényeg az, hogy rengeteg olyan reakció van, amelyek különböző neveken futnak, de ugyanazon a mechanikai folyamaton keresztül mennek végbe. Ez rávilágít annak fontosságára, hogy megtanuljuk a szerves kémia kulcsfontosságú mintáit, mert ezek bizony sokszor ismétlődnek.
Végjegyzet. Concerted, not separate?
Ha a Curtius lépcsőzetes lenne, akkor a nitrogénvesztés nitrénhez vezetne. A nitrének rengeteg érdekes reakción mennek keresztül, például C-H kötésekbe való beillesztésen (!). Tehát tervezhetünk egy kísérletet ennek tesztelésére: ha megpróbáljuk a következő Curtius-átrendeződést, bizonyítékot kereshetünk egy öttagú gyűrű kialakulására.
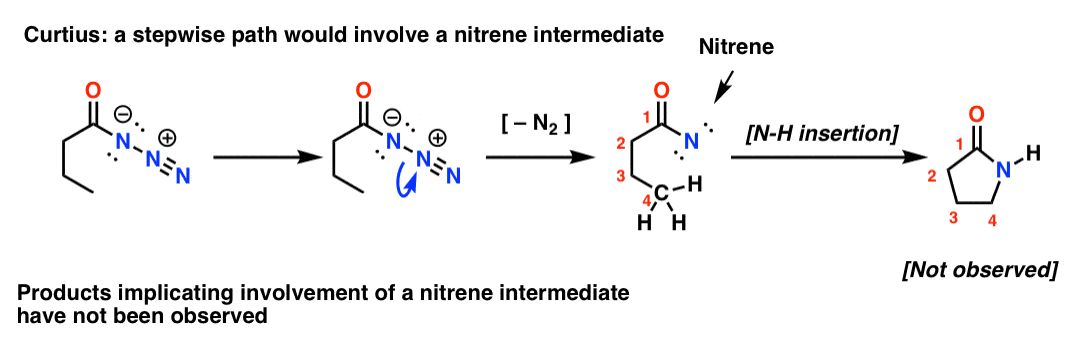
Az ilyen termékek hiánya, más bizonyítékokkal együtt, összehangolt mechanizmusra utal.
(Advanced) References and Further Reading
- Ueber die Einwirkung des Broms in alkalischer Lösung auf Amide
W. Hofmann
Chem. Ber. 1881, 14, 2725-2736
DOI: 10.1002/cber.188101402242
A. W. Hofmann (aki nagyon termékeny kémikus volt, és számos más átalakítás is a nevéhez fűződik) eredeti tanulmánya az amidok primer aminokká történő lebontásáról. - A Mild and Efficient Modified Hofmann Rearrangement
Xicai Huang, Mehran Seid, and Jeffrey W. Keillor
The Journal of Organic Chemistry 1997, 62 (21), 7495-7496
DOI:10.1021/jo9708553
Ez egy metanolban végzett módosított Hofmann-átrendeződés – ebben az esetben a köztes karbaminsav a metanolos oldószerrel reagálva jó hozammal metil-karbamátokat állít elő. - METHIL-KARBAMÁTOK KÉPZÉSE MODIFIKÁLT HOFMANN-átrendeződések útján: METHYL N-(p-METHOXYPHENYL)CARBAMATE
Jeffrey W. Keillor and Xicai Huang
Org. Synth. 2002, 78, 234
DOI: 10.15227/orgsyn.078.0234
Egy megbízható és egymástól függetlenül tesztelt eljárás a módosított Hofmann-átrendeződéshez a 2. hivatkozásban. - The Hofmann Reaction
Wallis, Everett L.; Lane, John F.
Org. React. 1946, 3, 267-306
DOI: 10.1002/0471264180.or003.07
Egy régi, de (a maga idejében) átfogó áttekintés a Hofmann-reakcióról (az amid-amin reakcióról, nem összetévesztendő más reakcióival). - Notes – A Re-examination of the Limitations of the Hofmann Reaction
Ernest Magnien and Richard Baltzly
The Journal of Organic Chemistry 1958, 23 (12), 2029-2032
DOI:10.1021/jo01106a630
Ez egy érdekes cikk, amelyben a szerzők megkísérelték a Hofmann-átrendeződés hatókörét az eredeti cikkben leírtakon túlra kiterjeszteni a reakciókörülmények gondos beállításával. - 20. Hydrazide und Azide organischer Säuren
Curtius, T. I. Abhandlung.
Journal Für Praktische Chemie, 50(1), 275-294. (1894).
DOI:1002/prac.18940500125 - Ueber Stickstoffwasserstoffsäure (Azoimid) N3H.
Curtius, T.
Berichte Der Deutschen Chemischen Gesellschaft, 23(2), 3023-3033. (1890).
DOI:1002/cber.189002302232
Theodore Curtius első, az acilhirazidok és acilazidok reaktivitását leíró cikkei. - The Curtius Reaction
Smith, P. A. S.
Org. React. 1946, 3, 336
DOI: 10.1002/0471264180.or003.09
A Curtius-reakció régi, de átfogó áttekintése, amely tartalmazza az átrendeződés felfedezésének történetét, a szubsztrátkörnyezetet, a korlátokat, az összehasonlítást más hasonló reakciókkal és a kísérleti eljárásokat. - UNDECYL ISOCYANATE
F. H. Allen és Alan Bell
Org. Synth. 1944, 24, 94
DOI: 10.15227/orgsyn.024.0094
Egy régi, de reprodukálható és kipróbált eljárás izocianátok szintézisére a Curtius-átrendeződés révén. - An Expedient Protecting-Group-Free Total Synthesis of (±)-Dievodiamine
William P. Unsworth, Christiana Kitsiou, and Richard J. K. Taylor
Organic Letters 2013 15 (13), 3302-3305
DOI:1021/ol4013469
A totálszintézis első lépése Curtius-átrendeződést alkalmaz az indol-szubsztituált karbonsav intramolekuláris ciklizációjához. - Szintetikus módszerek és reakciók. 121. Cink-jodiddal katalizált aroil-azidok előállítása aroil-kloridokból és trimetil-szilil-azidból
K. Surya Prakash, Pradeep S. Iyer, Massoud Arvanaghi és George A. Olah
The Journal of Organic Chemistry 1983 48 (19), 3358-3359
DOI: 10.1021/jo00167a051
Kényelmes eljárás aromás aril-azidok előállítására a Nobel-díjas Prof. George A. Olah-tól. Ezek aztán felhasználhatók Curtius átrendeződésekhez.