Her er sagen med dækningen af “aminer” i Org 2: der er ingen fortælling.
I modsætning til de fleste kapitler starter det ikke med et sæt begreber og bygger derefter op til en række eksempler, som du derefter kan anvende disse begreber på.
Nej. Et typisk kapitel om aminer i en introducerende lærebog er i bund og grund bare et sammensurium af tilsyneladende tilfældige emner, der er smidt sammen, og som ikke passede ind andre steder. Den eneste samlende tråd er, at de indeholder kvælstof på en eller anden måde.
Et eksempel: Dagens tilfældige aminoplæg handler om Hofmann- og Curtius-omlægningerne.
Hvad er årsagen til dette, spørger du måske? Intet godt svar. De fleste kurser dækker dem på et tidspunkt, og de skal jo passe ind et eller andet sted. Så hvad pokker. Hvorfor ikke nu?
Indholdsfortegnelse
- Hofmann- og Curtius-omlægningerne
- Mekanismen bag Hofmann- og Curtius-omlægningerne, første del – opsætning af omlægningen
- Del to: Det vigtigste omlægningsskridt i Hofmann- og Curtius-omlægningerne
- Del tre: Dannelse af isocyanat
- Sammenlægning af trinene
- Isocyanatets skæbne: Dannelse af carbamater, aminer og urinstoffer
- Summarum: Hofmann- og Curtius-omlægninger
- Noter
- (Avanceret) Referencer og yderligere læsning
- Hofmann- og Curtius-omlægninger
- Mekanismen for Hofmann- og Curtius-omlægningerne, del 1: Opsætning af omlægningen
- Del 1: Optakt
- 3. Det vigtige omarrangementstrin i Hofmann og Curtius
- Formation af isocyanat
- Sæt trinene sammen
- Isocyanatets skæbne
- Summary: The Hofmann and Curtius Rearrangements
- Noter
- (Avanceret) Referencer og videre læsning
Hofmann- og Curtius-omlægninger
Hofmann- og Curtius-omlægninger er to eksempler på en hel familie af omlægningsreaktioner, der har et fælles mekanistisk trin.
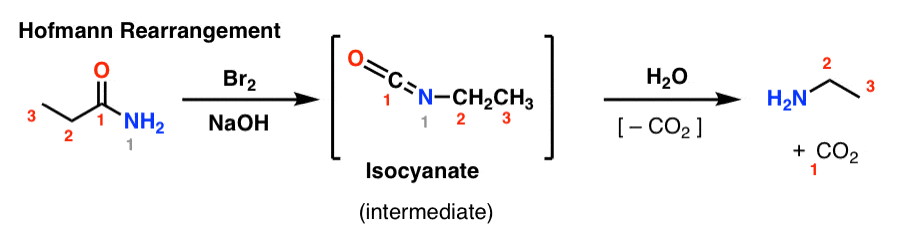
I Hofmann-omlægningen behandles et amid med bromin og base (normalt NaOH eller KOH). Ved opvarmning dannes der et mellemliggende isocyanat, som ikke isoleres. I tilstedeværelse af vand mister isocyanatet kuldioxid (“decarboxylater”) og giver en amin.
Den nøglebinding, der dannes i Hofmann-omdannelsen, er C2-N-bindingen. Bemærk, hvordan carbonylgruppen (C1) går tabt og danner kuldioxid (CO2). (Bemærk: dette er ikke IUPAC-nummerering, blot nummerering for at lette diskussionen)
I Curtius-omlægningen opvarmes et acylazid, og der dannes et isocyanat. I Curtius-omdannelsen kan isocyanatet isoleres, men det omdannes normalt yderligere til andre arter såsom en carbamat, en urinstof eller (via decarboxylering, som i Hofmann-omdannelsen) til en amin (mere om disse nedenfor).
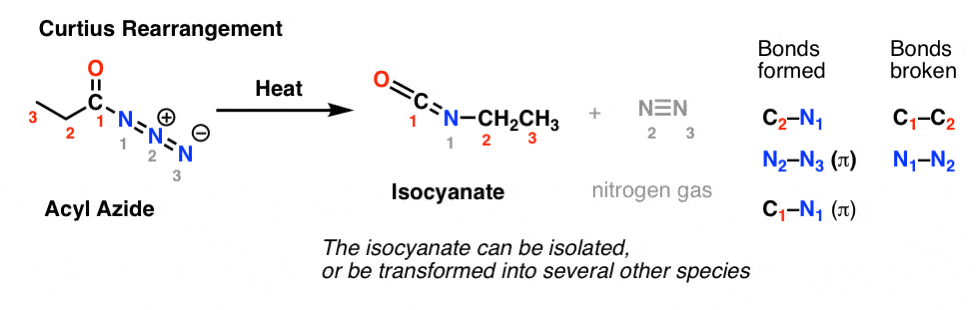
Den vigtigste observation at bemærke i begge tilfælde er, at C1-C2-bindingen er brudt, og en ny C2-N-binding er dannet.
Spørgsmålet er HVORDAN?
Mekanismen for Hofmann- og Curtius-omlægningerne, del 1: Opsætning af omlægningen
Der er fire vigtige dele i mekanismen for Curtius- og Hofmann-omlægningerne, og vi vil gennemgå dem alle.
- Præmieren (ligetil)
- Det centrale migrationstrin (tricky, men mindre tricky, hvis du indser, at du har set en variant af det i Org 1 !)
- Formning af isocyanat (ligetil)
4. Epilog: Transformationer af isocyanatet
Del 1: Optakt
- Hofmann-omlægningen sker med et amid.
- Curtius-omlægningen finder sted med et acylazid.
Både fremstilles bekvemt fra acylhalogenider gennem en additions-elimineringsreaktion. Hvis du behandler aminer nu, så er carbonylreaktioner sandsynligvis velkendt område. Acylhalogeniderne kan fremstilles fra carboxylsyrer ved hjælp af et reagens som thionylchlorid (SOCl2) eller fosforpentachlorid (PCl5).
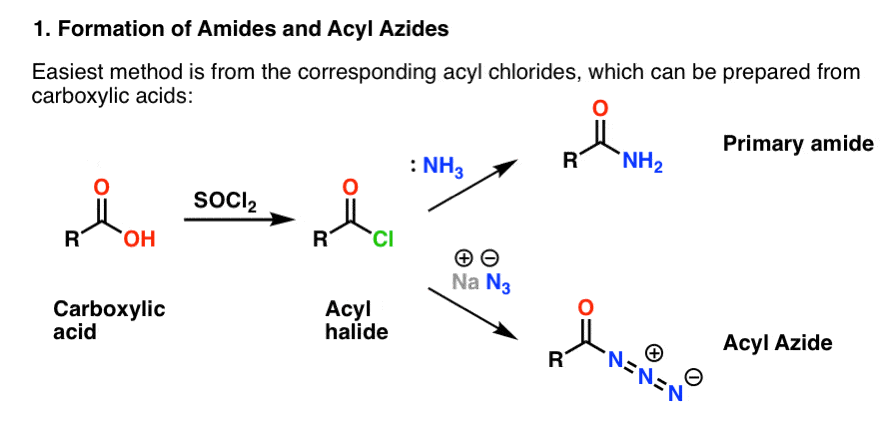
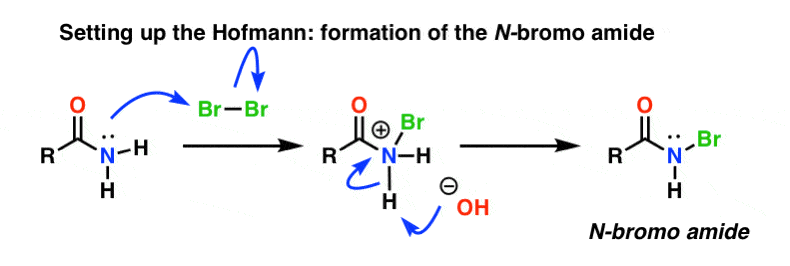
Opsætning af Hofmann
I Hofmann-omlægningen behandles amidet med brom (Br2) og en base som NaOH. Dette resulterer i bruddet af N-H og dannelsen af N-Br, hvilket resulterer i installation af en god afgangsgruppe på nitrogenet. Vi kalder dette et “N-bromoamid”.
Kurtius behøver ingen “opsætning”, da acylazidet allerede har en glimrende indbygget afgangsgruppe: N2. Derfor skal organiske azider behandles med forsigtighed, da grov behandling kan føre til eksplosioner.
3. Det vigtige omarrangementstrin i Hofmann og Curtius
Nu kommer vi til sagen.
Det centrale trin i Hofmann- og Curtius-omlægningerne er migration af et kulstofatom for at fortrænge en afgangsgruppe på et tilstødende nitrogen.
Dette kræver to buede pile at tegne, som er vist i strukturen længst til venstre (nedenfor).
- I den første buede pil brydes C-C-bindingen, og der dannes en ny C-N-binding.
- I den anden buede pil brydes N-LG-bindingen (leaving group).
Det er imidlertid ikke altid let at gå direkte fra strukturen yderst til venstre til strukturen yderst til højre (som er tegnet pænt og ryddeligt! ).
Utallige point går unødigt tabt til eksamen hvert år af elever, der får de buede pile rigtigt, men som ender med at tegne den forkerte struktur! Derfor opfordrer jeg eleverne til først at tegne en “grim version”, som ligner noget lort, men som i det mindste har alle bindingerne på det rigtige sted. Der er altid tid til at tegne den om og få den til at se pæn ud senere.
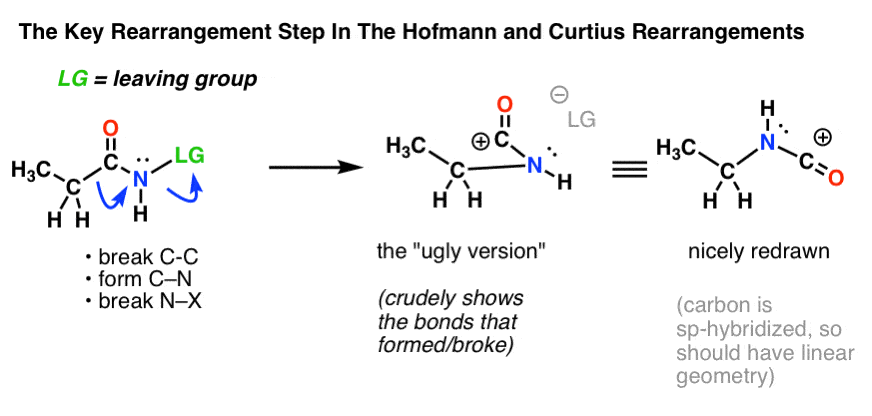
I første omgang ser denne omlægning sikkert … mærkelig ud. Men det er faktisk en reaktion, som du har set før! (men i forklædt form).
Nogen der kan huske mekanismen for “oxidations”-trinnet i hydroborations-oxidation?
Det er stort set det samme!
Her er en genopfriskning:
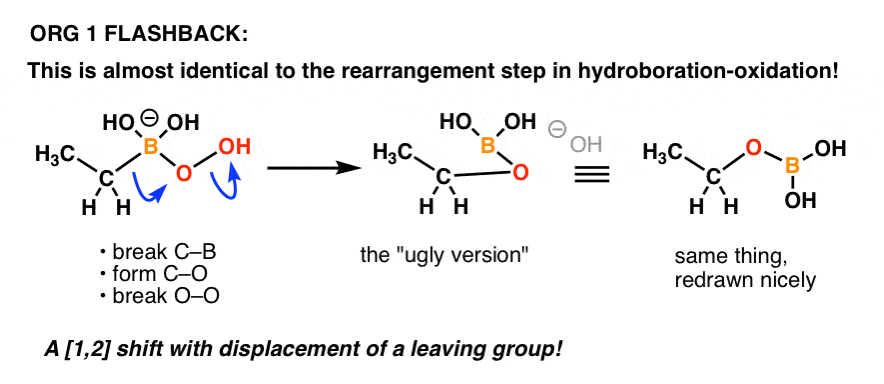
Så er der endnu et eksempel på, at ting, man lærer i en tidligere del af organisk kemi, kan vende tilbage i en senere del af kurset!
Lad os besøge det specifikke omlægningstrin i Hofmann- og Curtius-omlægningerne med konkrete eksempler.
Her er det centrale trin i Hofmann, hvor opvarmning resulterer i brud af C-C , dannelse af C-N og brud af N-Br.
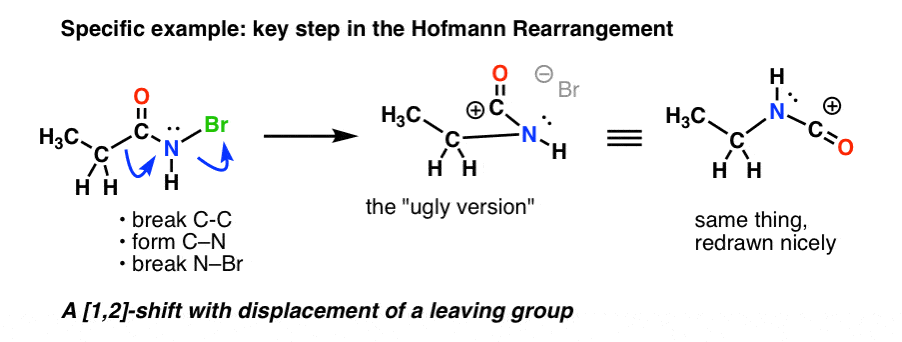
Hvis man følger alle pilene, skulle man ende med en underligt udseende carbocation (ovenfor til højre), som vi skal beskæftige os med om lidt.
I Curtius resulterer opvarmning af acylazidet i en omlejring. Den afgående gruppe er nitrogengas (N2).
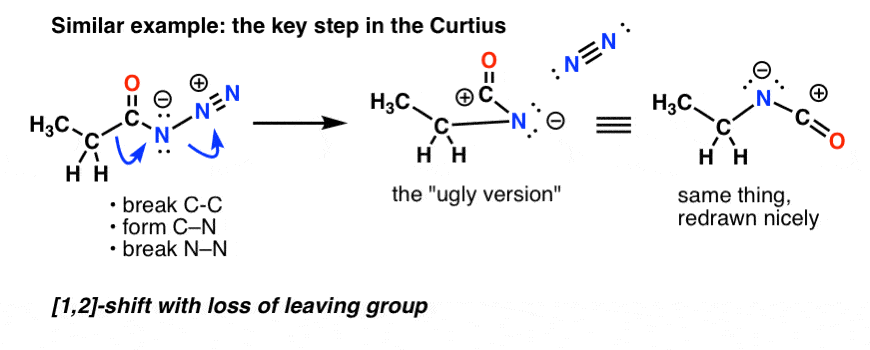
(En subtil forskel mellem Curtius og Hofmann er, at der ikke er noget hydrogen knyttet til N i Curtius, så vi ender med en negativ ladning på nitrogenet i den omarrangerede art.)
Formation af isocyanat
Det næste trin er at gå fra vores omarrangerede art til isocyanatet. For alle, der er vant til at tegne resonansformer, burde dette ikke være alt for svært.
(Som vi vil diskutere nedenfor, har undersøgelser fastslået, at isocyanatdannelsen sker samtidig med migrationen. Men til vores undervisningsformål tror jeg, at det hjælper at behandle dette trin isoleret. Vi kan sætte det hele sammen om et øjeblik).
Som du måske husker fra waayyyy tilbage i Org 1, er en resonansform med fulde oktetter overlegen i forhold til en uden (hurtig gennemgang). Vores underligt udseende produkt fra rearrangement har en karbokation ved siden af et nitrogen, der indeholder et lonepar. Så det første skridt er at tegne dannelsen af en ny C-N pi-binding. Dette er i det væsentlige blot en resonansform.
Hofmann-omlægningen sker i tilstedeværelse af base. Så efter tegning af resonansformen er det næste trin deprotonering af N-H-bindingen, hvilket giver det neutrale isocyanat.
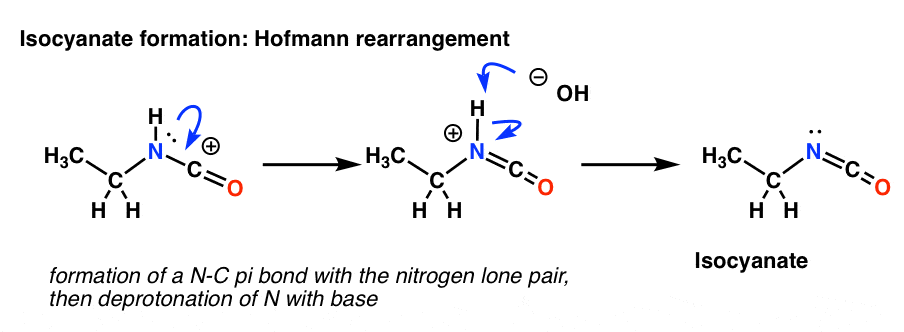
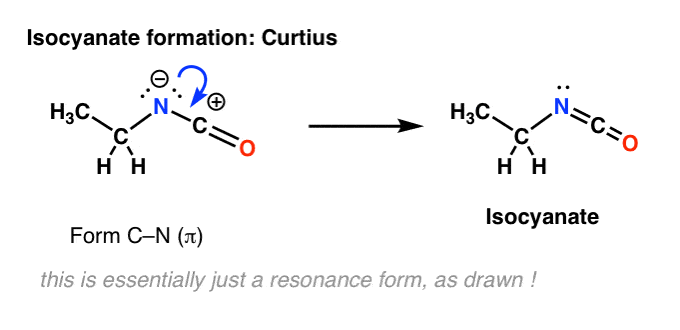
Der er ikke noget hydrogen på nitrogenet i Curtius. Isocyanatdannelsen sker altså blot ved donation af et lonepar fra nitrogen til carbocationen. Man kan bare se på det som at tegne en resonansform.
Sæt trinene sammen
Undersøgelser af mekanismen for Hofmann- og Curtius-omlægningerne har fastslået, at disse to trin ikke sker sekventielt; de sker faktisk på samme tid! (hvordan ved vi det? se note 1 )
Det vil sige, at migrationen sker samtidig med isocyanatdannelsen.
Vi er nødt til at omtegne Hofmann- og Curtius-mekanismerne for at afspejle dette og inkorporere begge trin.
Her er Hofmann (bemærk, at deprotoneringshændelsen faktisk er separat).
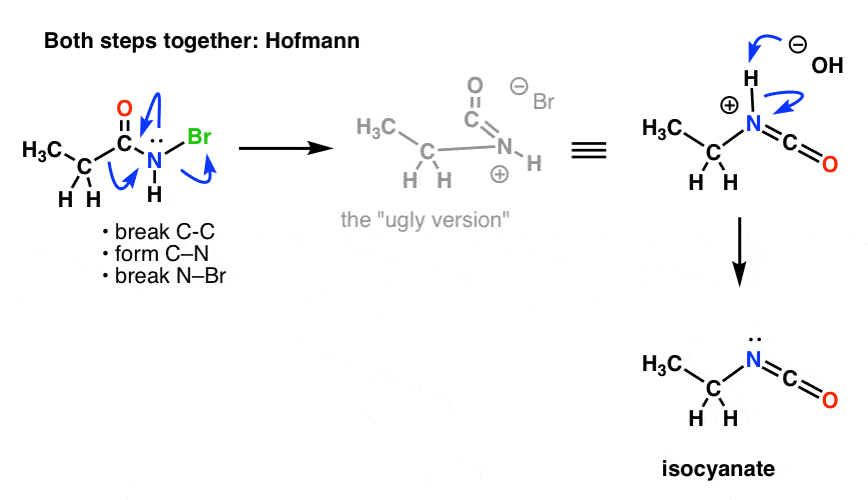
Og Curtius:
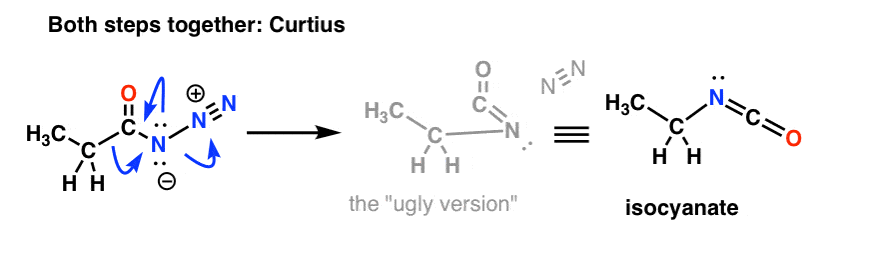
Isocyanatets skæbne
Både Hofmann og Curtius giver anledning til et isocyanat. Du har sandsynligvis ikke stødt på isocyanater før. Ved første øjekast er de ret mærkeligt udseende arter, men deres kemi er ikke så forskellig fra andre carbonylarter som estere, amider og acylhalogenider.
Isocyanatets struktur ligner nøje kuldioxidens, CO2’s, struktur. Kulstoffet er pi-bundet til to stærkt elektronegative atomer. Dette gør kulstoffet til en fremragende elektrofil.
Ved at tilsætte forskellige nukleofile stoffer kan isocyanater omdannes til andre nyttige arter.
– Tilsætning af en alkohol resulterer i dannelse af en carbamat
– Tilsætning af en amin resulterer i en urea
– Tilsætning af vand resulterer i en carbaminsyre, som er ustabil. Carbaminsyrer mister hurtigt kuldioxid og giver en amin.
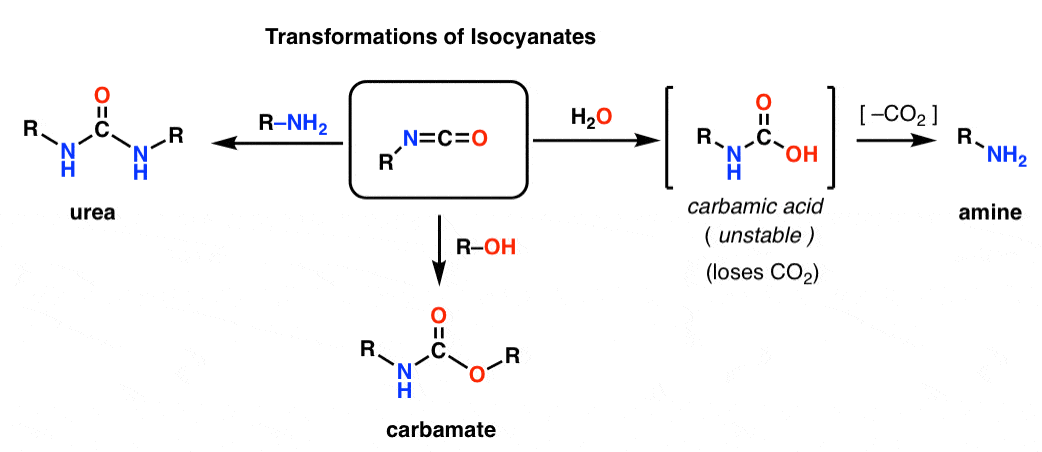
Den decarboxyleringsvej udgør især en smart måde at fremstille aminer på. Vi har lært tonsvis af måder at fremstille carboxylsyrer på, men ikke ret mange måder at fremstille aminer på (ud over nukleofil substitution og reduktiv aminering). Hofmann er et godt trick at have i baglommen i situationer, hvor ingen af disse situationer kan være relevante – som f.eks. at lave substituerede aniliner.
Mekanismer? OK, fint nok. Se bonusemne 1.
Summary: The Hofmann and Curtius Rearrangements
Mekanismen for disse omlægninger er vanskelig ved første øjekast, men bliver betydeligt nemmere, når du indser, at du har set en variant af migrationsreaktionen før (i.f. eks. i hydroborations-oxidation).
Jeg anbefaler stærkt at tegne den grimme version først, fordi det vil hjælpe dig med at fokusere på at se de bindinger, der dannes og brydes, før du forsøger at tegne den om til en mere æstetisk tiltalende struktur. Dette gælder også for Beckmann- og Wolff-omlægningerne, som har et lignende trin (se nedenfor)
Noter
Bonustema 1: Isocyanater
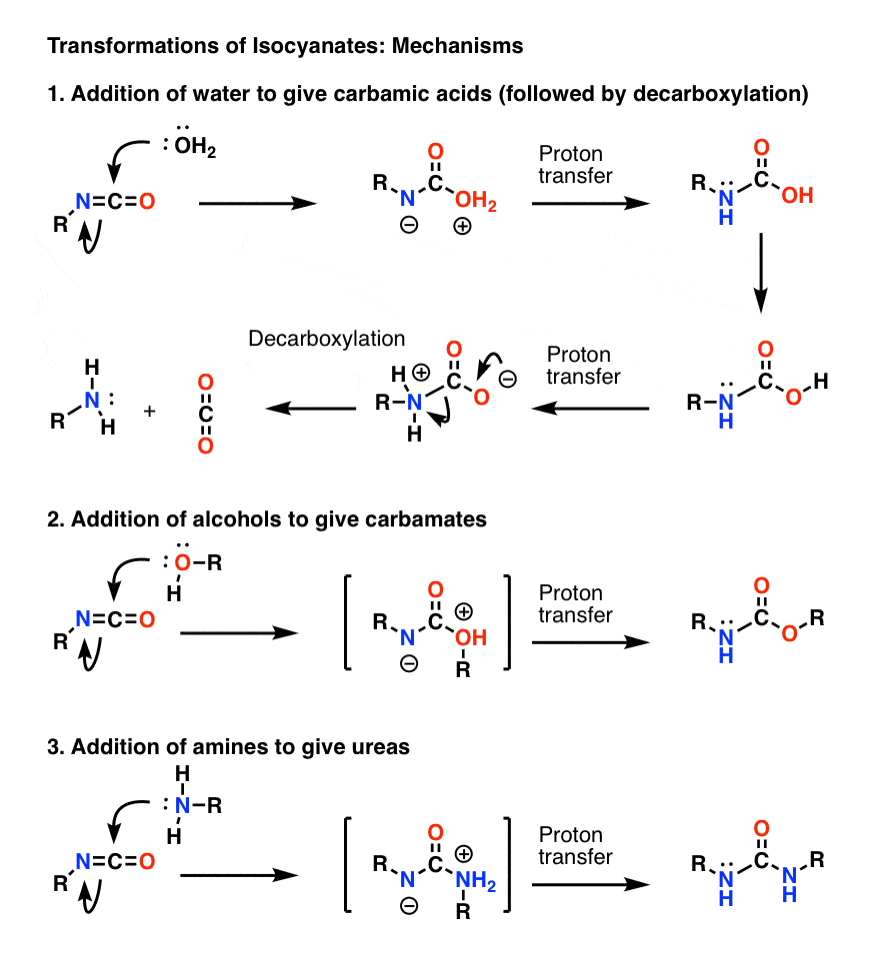
Den vigtigste mekanisme for isocyanater er elektrofil addition (dvs. tilføjelse af en nukleofil til det centrale, elektrofilt kulstof). I mekanismen nedenfor har jeg vist nukleofilen, der adderer til kulstoffet, så der dannes en anion på nitrogenet, selv om dette sandsynligvis ikke er er er den bedste resonansform (oxygenet er bedre til at stabilisere negativ ladning end nitrogenet). Protonoverførsel fra oxygen til nitrogen resulterer i en neutral art. (Jeg har brugt den magiske stav til protonoverførsel her, fordi det er hurtigere).
Bemærk, at decarboxyleringstrinnet i 1) ikke behøver at blive forudgået af deportation af ilten, selv om det absolut skal ske således, at nitrogenet protoneres under trinnet (man ønsker ikke at danne en stærkt basisk amidion, f.eks.).
Bonus emne 2: Beckmann-, Wolff- og andre omlejringer har et lignende trin til fælles
Men vent, der er mere!
Der er en 1,2-forskydning med tab af en afgangsgruppe i Beckmann-omlejringen. Nøgletrinet er stort set det samme som vi så i Hofmann- og Curtius-omlægningen.
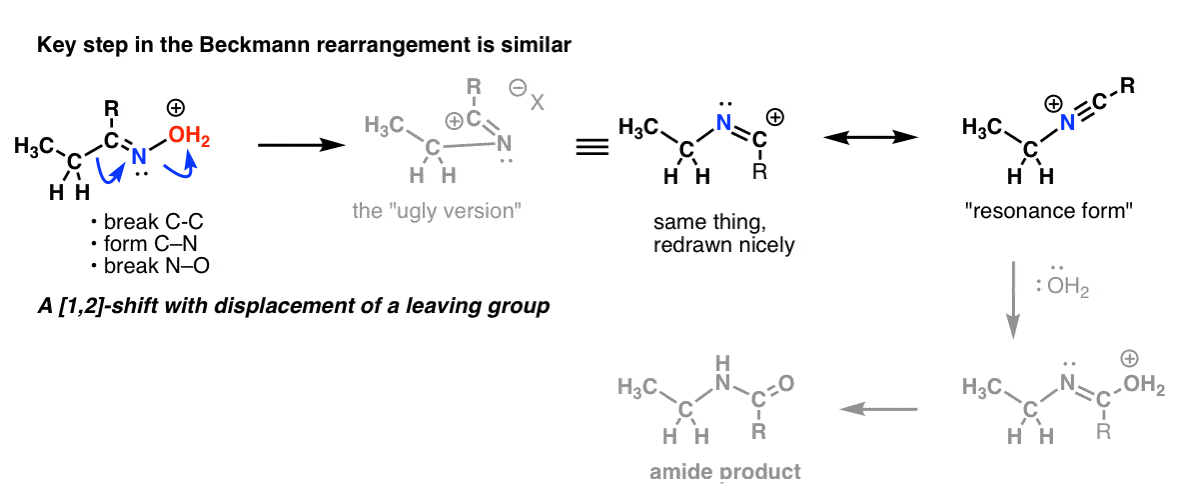
Og i Wolff-omlægningen, som almindeligvis også er dækket, kan du måske også genkende det samme nøgletrin.
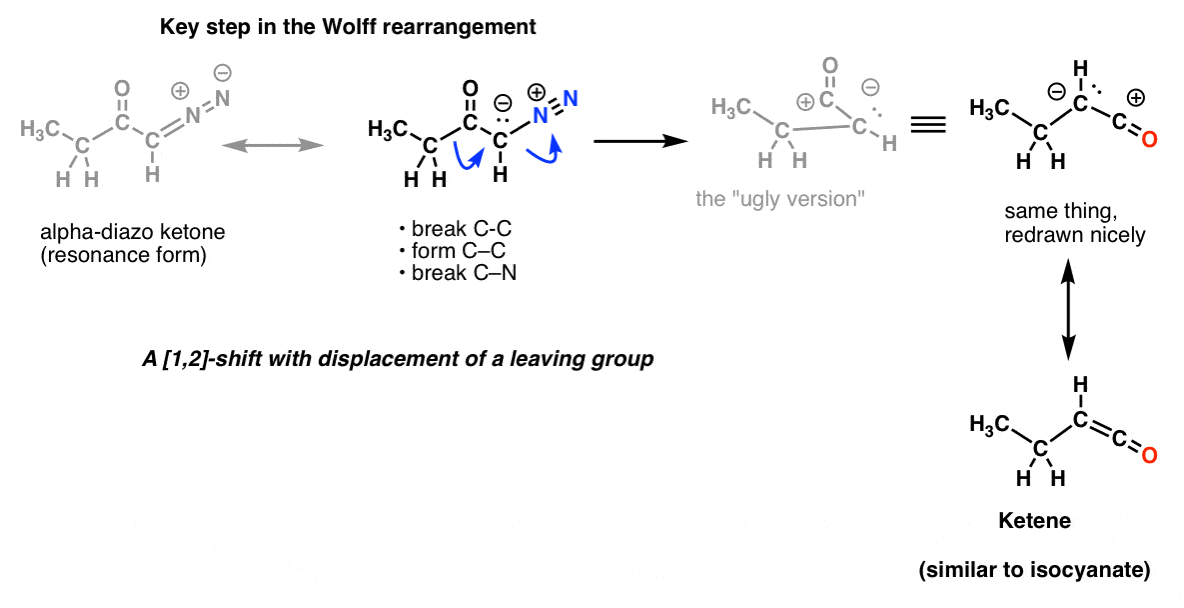
Og det er ikke alt! Der findes en reaktion kaldet Schmidt-omlægning, som er ligesom Curtius, men som kommer ved at tilsætte HN3 til et acylchlorid (eller en carboxylsyre). Og der er en anden, der kaldes Lossen-omlægning, som opstår med hydroxyaminsyrer. Der er ingen præmier for at gætte det vigtigste trin i disse to processer. Og vi har ikke engang nævnt Baeyer-Villiger, som ikke involverer kvælstof, men som stort set er den samme type proces.
Da jeg for mange måner siden lærte hydroborations-oxidationstrinnet i Org 1, havde jeg bestemt ikke forventet, at jeg ville se det samme reaktionsmønster gentage sig selv i så mange forskellige udgaver.
Det afgørende er, at der er en masse reaktioner, der går under forskellige navne, men som forløber gennem den samme mekanistiske proces. Dette understreger vigtigheden af at lære de vigtigste mønstre i organisk kemi, for de gentager sig sandelig meget.
Endnote. Koncerterede, ikke separate?
Hvis Curtius var trinvis, ville tabet af nitrogen føre til et nitren. Nitrener gennemgår et væld af interessante reaktioner, som f.eks. indsættelse i C-H-bindinger (!). Så man kan designe et eksperiment for at teste dette: hvis man prøver den følgende Curtius-omlægning, kan man kigge efter tegn på dannelse af en femleddet ring.
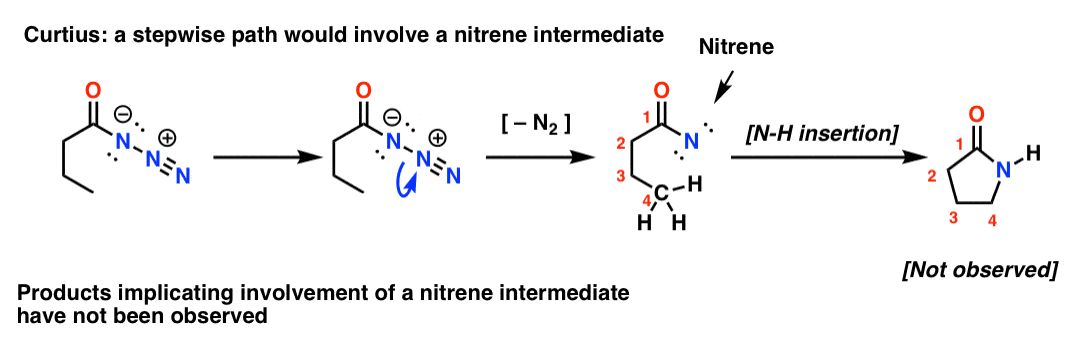
Afstanden af sådanne produkter, sammen med andre beviser, peger på en samordnet mekanisme.
(Avanceret) Referencer og videre læsning
- Ueber die Einwirkung des Broms in alkalischer Lösung auf Amide
W. Hofmann
Chem. Ber. 1881, 14, 2725-2736
DOI: 10.1002/cber.188101402242
Originalartikel af A. W. Hofmann (som var en meget produktiv kemiker og har sit navn tilknyttet mange andre transformationer) om nedbrydning af amider til primære aminer. - A Mild and Efficient Modified Hofmann Rearrangement
Xicai Huang, Mehran Seid, and Jeffrey W. Keillor
The Journal of Organic Chemistry 1997, 62 (21), 7495-7496
DOI:10.1021/jo9708553
Dette er en modificeret Hofmann-omlægning udført i methanol – i dette tilfælde kan den intermediære carbaminsyre reagere med methanolopløsningsmidlet for at producere methylcarbamater med et godt udbytte. - METHYLCARBAMATFORMNING VIA MODIFICEREDE HOFMANN-OMLØSNINGSREGNINGSREAKTIONER: METHYL N-(p-METHOXYPHENYL)CARBAMAT
Jeffrey W. Keillor og Xicai Huang
Org. Synth. 2002, 78, 234
DOI: 10.15227/orgsyn.078.0234
En pålidelig og uafhængigt afprøvet procedure for den modificerede Hofmann-omlægning i Ref #2. - The Hofmann Reaction
Wallis, Everett L.; Lane, John F.
Org. React. 1946, 3, 267-306
DOI: 10.1002/0471264180.or003.07
En gammel, men omfattende (for sin tid) gennemgang af Hofmann-reaktionen (amid til amin-reaktionen, der ikke må forveksles med hans andre reaktioner). - Noter – A Re-examination of the Limitations of the Hofmann Reaction
Ernest Magnien og Richard Baltzly
The Journal of Organic Chemistry 1958, 23 (12), 2029-2032
DOI:10.1021/jo01106a630
Dette er en interessant artikel, hvor forfatterne har forsøgt at udvide omfanget af Hofmann-omlægningen ud over det, der blev beskrevet i den oprindelige artikel, ved omhyggeligt at justere reaktionsbetingelserne. - 20. Hydrazide und Azide organischer Säuren
Curtius, T. I. Abhandlung.
Journal Für Praktische Chemie, 50(1), 275-294. (1894).
DOI:1002/prac.18940500125 - Ueber Stickstoffwasserstoffsäure (Azoimid) N3H.
Curtius, T.
Berichte Der Deutschen Chemischen Gesellschaft, 23(2), 3023-3033.(1890).
DOI:1002/cber.189002302232
Første artikler af Theodore Curtius, der beskriver reaktiviteten af acylhyrazider og acylazider. - The Curtius Reaction
Smith, P. A. S.
Org. React. 1946, 3, 336
DOI: 10.1002/0471264180.or003.09
En gammel, men omfattende gennemgang af Curtius-reaktionen, som omfatter historien om opdagelsen af denne omlægning, substratets omfang, begrænsninger, sammenligning med andre lignende reaktioner og eksperimentelle procedurer. - UNDECYL ISOCYANATE
F. H. Allen og Alan Bell
Org. Synth. 1944, 24, 94
DOI: 10.15227/orgsyn.024.0094
En gammel, men reproducerbar og afprøvet procedure til syntese af isocyanater gennem Curtius-omlægning. - En hensigtsmæssig beskyttelsesgruppe-fri totalsyntese af (±)-Dievodiamin
William P. Unsworth, Christiana Kitsiou og Richard J. K. Taylor
Organic Letters 2013 15 (13), 3302-3305
DOI:1021/ol4013469
Det første trin i denne totalsyntese anvender en Curtius-omlægning til at foretage en intramolekylær cyklisering af den indol-substituerede carboxylsyre. - Syntetiske metoder og reaktioner. 121. Zinkjodid-katalyseret fremstilling af aroylazider fra aroylchlorider og trimethylsilylazid
K. Surya Prakash, Pradeep S. Iyer, Massoud Arvanaghi og George A. Olah
The Journal of Organic Chemistry 1983 48 (19), 3358-3359
DOI: 10.1021/jo00167a051
En bekvem fremgangsmåde til fremstilling af aromatiske arylazider fra nobelprismodtageren professor George A. Olah. Disse kan derefter anvendes til Curtius-omlægninger.