US Pharm. 2018;43(9):21-26.
ABSTRACT: Hormonersättningsterapi (HRT) är den mest effektiva behandlingen för vasomotoriska och genitourinära symtom i samband med klimakteriet. Biverkningar i samband med HRT är beroende av olika faktorer, inklusive dosering, väg, användningstid, tidpunkt för initiering och val av medel. Beslutet att påbörja HRT bör innefatta en riskbedömning, och HRT bör individanpassas till patienten. De många befintliga HRT-alternativen finns i ett brett utbud av doser och doseringsformer. Apotekare bör kunna ge råd till patienter om HRT och dess biverkningar.
Den genomsnittliga kvinnan kommer att leva en tredjedel av sitt liv i eller efter menopausen.1 Behandling av menopausala symtom har fått allt större betydelse på grund av den sjuklighet som är förknippad med åldrande hos kvinnor.2 Hormonersättningsterapi (HRT), en term som används för att beskriva östrogenbehandling, östrogen-progesteronkombinationsterapi eller östrogenreceptoragonist- eller antagonistbehandling, fortsätter att spela en viktig roll för att lindra perimenopausala och postmenopausala symtom.3 Även om varje kvinnas upplevelse är annorlunda är vasomotoriska symtom (VMS) och vulvovaginala symtom två av de vanligaste klagomålen i samband med de hormonella förändringar som är involverade i klimakteriet.4
Menopausala symtom
VMS är några av de vanligaste och mest besvärliga menopausala symtomen. Värmeböljor, som kännetecknas av en plötslig värmekänsla i övre delen av bröstet och ansiktet som varar i 2-4 minuter, förekommer hos cirka 75 % av kvinnor i klimakteriet.1 Andra möjliga VMS är svettningar, hjärtklappning och ångest.1 VMS har förknippats med försämrad sömnkvalitet, irritabilitet, koncentrationssvårigheter och minskad livskvalitet.3 Dessutom har dessa symtom kopplats till kardiovaskulära, ben- och kognitiva risker.5-9 HRT har länge erkänts som den mest effektiva behandlingen för VMS.4,10
Förutom besvärande VMS upplever många kvinnor vulvovaginala symtom. Man uppskattar att 10-40 % av kvinnorna upplever vaginal atrofi.3 Vaginal atrofi kan orsaka smärta, sveda och klåda i vulvan, vaginal torrhet, vaginala flytningar, dyspareuni (svårt eller smärtsamt samlag) samt fläckar eller blödningar efter samlag.1 Dessa symtom tenderar att uppträda i det sena postmenopausala skedet och kan leda till obehag av åtsittande kläder, när man sitter eller tränar eller vid sexuell aktivitet.1 Topisk HRT rekommenderas vanligtvis för behandling av vulvovaginala symtom.1
Förutom att lindra de tidigare nämnda symtomen finns det bevis för att standardiserad lågdos HRT också kan förebygga postmenopausala höft-, ryggmärgs- och icke ryggmärgsfrakturer.10 Fördelarna med HRT för VMS och genitourinära symtom är bland annat förbättringar av överaktiv blåsa, minskade sömnstörningar, minskad risk för typ 2-diabetes, potentiellt skydd mot kranskärlssjukdom (CAD) och hjärtinfarkt, minskad risk för osteoporos eller frakturer och en potentiell minskning av mortalitet av alla orsaker.1,10 Fördelarna HRT ger på bentäthet minskar dock snabbt efter avbrytande. Dessutom, även om vissa produkter har FDA-godkännande för förebyggande av osteoporos, är ingen av dem för närvarande godkänd för behandling av osteoporos. Stora risker som är förknippade med användningen av dessa medel inkluderar venös tromboembolism (VTE), ischemisk stroke, ökad förekomst av endometriecancer (om ett östrogen utan motsats används hos en kvinna med livmoder) och ökad risk för bröstcancer när HRT används längre än 3-5 år.4,10
Tillgängliga HRT-produkter
Ett brett utbud av HRT-produkter är tillgängliga i olika doseringsformer.4 Bland de orala preparaten finns bland annat konjugerade ekvina östrogener (CEE), mikroniserat 17-beta-östradiol (mikroniserat för att förbättra absorptionen), förestrade östrogener, etinylöstradiol (ett mycket potent östrogenpreparat som används i mycket lägre doser för HRT än för orala preventivmedel), östrogen-gestagen-kombinationstabletter och en kombinationstablett av CEE/bazedoxifen.4
CEE/bazedoxifen-tabletten, en kombination av östrogen och en selektiv östrogenreceptormodulator, finns tillgänglig i USA för behandling av menopausalt VMS och förebyggande av osteoporos. I denna kombination förhindrar bazedoxifen östrogeninducerad endometriehyperplasi, vilket gör administrering av ett gestagen onödig. Bazedoxifen är dock förknippat med ökad risk för VTE.4 Användning av bazedoxifen har befunnits vara säker när den studerats i upp till 7 år vid behandling av osteoporos, men kombinationen har endast studerats under kortare tidsperioder.11,12 VMS-studier som pågått i upp till 2 år har inte visat på någon ökning av förekomsten av bröstömhet eller risk för bröstcancer.3 Nuvarande riktlinjer rekommenderar användning av CEE/bazedoxifen hos postmenopausala kvinnor med livmoder och utan kontraindikationer för att behandla VMS och bidra till att förebygga benförlust, men anger inte hur länge behandlingen ska pågå.1 Baserat på tillgänglig evidens förefaller behandling av VMS med CEE/bazedoxifen i upp till 2 år vara säker; säkerheten vid användning efter 2 år är fortfarande oklar.
HRT finns också tillgänglig i olika topiska applikationer. Transdermala plåsterpreparat av 17-beta-estradiol eller östrogen-gestagenkombinationer finns tillgängliga. Andra topiska preparat inkluderar gelpaket eller doseringspumpar, sprayer och emulsioner.4 Depotinjektioner kan också övervägas, men dessa produkter används sällan i samband med HRT.4 En sammanfattning av tillgängliga systemiska HRT-formuleringar ges i TABELL 1.13-15
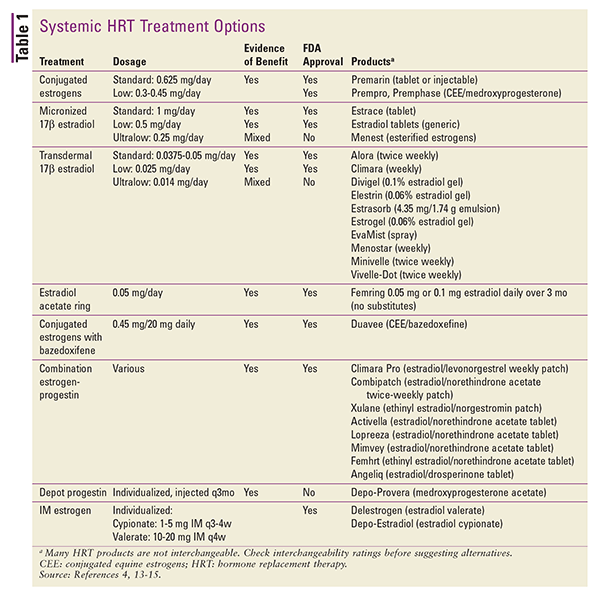
Vid omräkning från en doseringsform till en annan kan skillnader i administreringsväg och produktstyrka beaktas med hjälp av uppskattade dosekvivalenter.4 Dosekvivalenterna för orala preparat är följande: 1 mg mikroniserat 17-beta-estradiol motsvarar 1,25 mg piperazinestronsulfat. Vid omräkningar mellan orala och transdermala östrogenpreparat motsvarar 0,05 mg/24 timmar transdermalt ungefär 0,625 mg dagligen via munnen.4
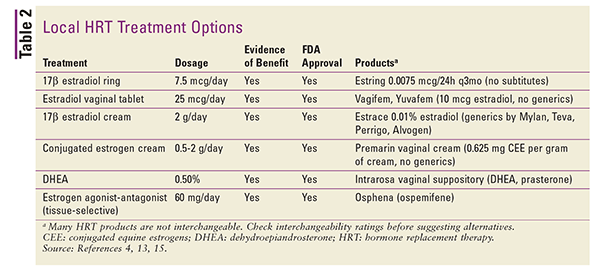
Lokala preparat är i allmänhet lågdoserade och används specifikt för behandling av symtom på vulvovaginal atrofi.4 Högre doser kan användas för behandling av systemisk VMS, men detta rekommenderas generellt sett inte.4 Lokala preparat inkluderar vaginalringar, tabletter och krämer. Se TABELL 2 för en sammanfattning av tillgängliga lokala HRT-preparat.4,13,15
Aktuella riktlinjerekommendationer
Tre organisationer – American College of Obstetricians and Gynecologists, North American Menopause Society (NAMS) och Endocrine Society – har tagit fram riktlinjer för användning av HRT i klimakteriet. Såsom anges i dessa riktlinjer omfattar indikationerna för HRT behandling av VMS i samband med klimakteriet och behandling av vulvovaginala effekter i avsaknad av besvärande systemiska symtom.1,3,4 Östrogen, ensamt eller i kombination med ett gestagen, har visat sig minska veckovis VMS med 75 % och signifikant minska symtomens allvarlighetsgrad jämfört med placebo.4
I kvinnor yngre än 60 år som är mindre än 10 år efter menopausen, har besvärande VMS och inte har några kontraindikationer för HRT eller överdriven kardiovaskulär eller bröstcancerrisk, rekommenderas användning av enbart östrogenbehandling för dem som saknar livmoder. Tillägg av ett gestagen rekommenderas hos patienter med en livmoder för att förebygga endometriehyperplasi och potentiell endometriecancer.1,3,4 För närvarande är den nödvändiga gestagenexponeringen oklar, men många leverantörer ger gestagener i en 14-dagarscykel varje månad.4 För kvinnor som är äldre än 60 år eller som är mer än 10 år efter menopausen rekommenderas övervägande av andra (icke-hormonella) terapier i stället för HRT.3
För kvinnor med förhöjd risk för kardiovaskulär sjukdom (CVD; definierat som >10% 10-års risk för CVD enligt American College of Cardiology/American Heart Association cardiovascular risk estimator tool) är icke-hormonella terapier att föredra.3 Hos kvinnor med måttlig CVD-risk är transdermalt östrogen med eller utan gestagen att föredra framför oral behandling, eftersom dessa preparat har mindre effekt på blodtryck, lipider och kolhydratmetabolism.1 Hos patienter med förhöjd risk för VTE är användning av icke-orala vägar vid lägsta effektiva dos att föredra. Slutligen, hos patienter med hög eller intermediär risk för bröstcancer föredras icke-hormonella terapier.4
Om HRT väljs rekommenderar alla riktlinjer användning av den lägsta effektiva dosen.1,4,10 En fördel med lägre doser HRT är den bättre biverkningsprofilen jämfört med högdosregimer.4 Det finns ingen för närvarande föredragen terapirutt för behandling av VMS; därför bör administreringsvägen styras av patientens preferenser. Det bör noteras att transdermala produkter kan vara förknippade med en lägre incidens av biverkningar, t.ex. VTE, men studier genomförs fortfarande.10
För behandling av genitourinära symtom hos kvinnor utan anamnes på hormonberoende cancer kan lågdos vaginalt östrogen användas.1 För enbart vaginala symtom rekommenderar riktlinjerna att man avråder från att tillsätta progestin oavsett om livmodern finns eller inte. Denna behandling kan också vara lämplig för patienter med en historia av hormonberoende cancer, men i dessa fall bör valet av behandling baseras på en gemensam beslutsprocess som inkluderar en diskussion om risker och fördelar. Potentiella fördelar med vaginalt östrogen är bland annat snabb förbättring av vaginala och urinlika symtom och eventuellt förebyggande av återkommande urinvägsinfektioner. Icke-östrogena FDA-godkända och riktlinjerkonsekventa terapier som används för att lindra dyspareunier inkluderar ospemifen och intravaginalt dehydropiandrosteron.16,17
Enbart gestagenbehandling, testosteron, växtbaserade alternativa icke-hormonella terapier och sammansatta bioidentiska hormoner saknar data och rekommenderas i allmänhet inte.1,4 NAMS anger att förskrivare kan överväga sammansatt HRT i situationer där en patient inte kan tolerera FDA-godkända terapier.3 Icke-hormonella behandlingsalternativ för vasomotoriska symtom inkluderar selektiva serotoninåterupptagshämmare och selektiva serotonin-norepinefrinåterupptagshämmare, klonidin och gabapentin, och icke-hormonella behandlingsalternativ för vaginala symtom inkluderar smörjmedel, östrogenagonist-antagonister och naturläkemedel.4 Bevisen som stöder användningen av icke-hormonella behandlingar varierar, och inte alla alternativ har bevisad evidens eller en FDA-godkänd indikation.4
Kontroll av HRT bör inkludera regelbundna bröstcancerscreeningar under och efter avslutad behandling. Återkommande oplanerade blödningar bör bedömas snabbt.1 Behandlingens varaktighet bör ses över minst en gång per år, och den kortaste behandlingstiden är att föredra.1 När patienter och vårdgivare bestämmer sig för att avbryta HRT kan antingen en avsmalnande eller en abrupt avbrottsstrategi användas. Det saknas evidens när det gäller metoder för avbrytande; därför rekommenderas delat beslutsfattande för processen för avbrytande.1,4
Läkemedels-läkemedelsinteraktioner
Majoriteten av kommersiellt tillgängliga HRT-produkter (TABELL 1) genomgår en levermetabolism som förmedlas av CYP450-systemet.15 Specifikt metaboliseras östrogenprodukter delvis av CYP3A4; därför kan starka inducerare av CYP3A4 minska effekten av östrogen HRT och starka hämmare kan öka serumkoncentrationerna av östrogen. Dessutom kan andra läkemedelssubstrat för dessa enzymer interferera med metabolismen av HRT.15
Svåra och vanliga biverkningar
De viktigaste biverkningarna som förknippas med HRT är CVD, bröstcancer, endometrie- eller äggstockscancer, stroke och VTE.1 Användning av östrogen utan motverkande effekt ökar risken för endometriehyperplasi och cancer, därav rekommendationen att lägga till progestagen hos kvinnor med livmoder. När det gäller risken för bröstcancer verkar det finnas en liten risk för att utveckla bröstcancer när en kvinna får östrogen i 5 år.3 Den nuvarande litteraturen är inkonsekvent när det gäller att fastställa risken för att utveckla äggstockscancer av HRT.3 Det behövs fler randomiserade, kontrollerade studier för att fastställa den verkliga risken för att utveckla äggstockscancer vid HRT-användning.1 Effekterna av HRT på kranskärlssjukdom (CAD), stroke och VTE varierar beroende på en kvinnas ålder när hon börjar med HRT eller tiden sedan menopausen inträdde. Det verkar som om kvinnor som tar HRT i mer än 10 år från menopausens början löper en ökad risk att utveckla CAD.3 Sammantaget tyder studier på att lägre doser av orala och transdermala formuleringar ger en minskad risk för stroke och VTE jämfört med HRT i standarddos.3 Patienter som är äldre än 60 år när de börjar med HRT eller som är mer än 10 år från menopausens början löper en ökad risk för dessa negativa effekter. Dessutom löper kvinnor som tar HRT med östrogen antingen ensamt eller i kombination en ökad risk för gallstenar, kolecystit och kolecystektomi.3 Risken för gallblåsesjukdom har förknippats med användning av oral HRT och kanske inte finns med topiska eller transdermala formuleringar.1,3
Kontraindikationer
Riktlinjerna för professionella sällskap har inte specificerat någon lista över absoluta eller relativa kontraindikationer för HRT.2 Därför är det, precis som vid de flesta kliniska beslut, viktigt med en individualiserad risk-nytta-bedömning. I allmänhet bör HRT undvikas hos patienter med oförklarlig vaginal blödning, anamnes på stroke eller transitorisk ischemisk attack, hjärtinfarkt, lungemboli eller VTE, bröst- eller endometriecancer, aktiv leversjukdom, känd protein C-, protein S- eller antitrombinbrist eller andra trombofila störningar samt känd eller misstänkt graviditet1. Dessutom bör försiktighet iakttas hos patienter med diabetes, gallblåsesjukdom, hypertriglyceridemi (>400 mg/dag), hypoparatyreoidism, benignt meningiom, intermediär eller hög risk för bröstcancer, hög risk för hjärtsjukdom eller migrän med aura.2
Rådgivningspunkter
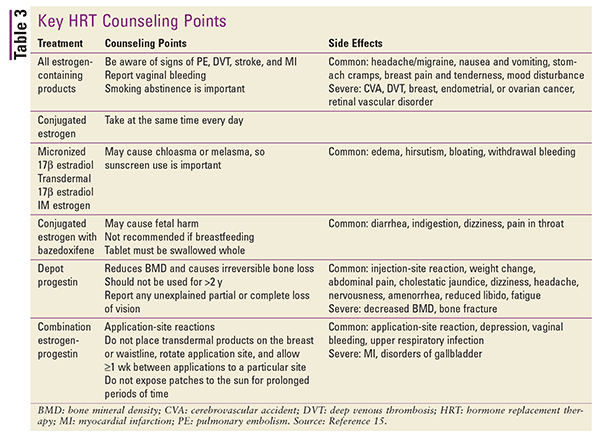
Hänvisa till TABELL 3 för en sammanfattning av viktiga patientrådgivningspunkter och biverkningar för de olika typerna av HRT.15
Slutsats
HRT, som finns tillgängligt i ett stort antal olika preparat, är den effektivaste behandlingen för både VMS och genitourinära symptom. Eftersom de risker som är förknippade med HRT är olika för varje kvinna bör behandlingen individualiseras och syfta till att maximera effekten, minimera behandlingstiden och minska risken för biverkningar. I scenarier där HRT inte är ett alternativ finns icke-hormonella behandlingsalternativ för både VMS och genitourinära symtom, men effekten och FDA-godkännandet av dessa produkter varierar; därför bör effektdata för dessa produkter granskas.
1. Stuenkel CA, Davis SR, Gompel A, et al. Behandling av symtom i klimakteriet: en klinisk riktlinje från Endocrine Society. J Clin Endocrinol Metab. 2015;100(11):3975-4011.
2. Shifren JL, Schiff I. Role of hormone therapy in the management of menopause. Obstet Gynecol. 2010;115(4):839-855.
3. NAMS 2017 Hormone Therapy Position Statement Advisory Panel. 2017 års ställningstagande om hormonterapi från North American Menopause Society (NAMS). Klimakteriet. 2017;24(7):728-753.
4. ACOG Practice Bulletin No. 141: Management of menopausal symptoms. Obstet Gynecol. 2014;123(1):202-216.
5. Thurston RC, Sutton-Tyrrell K, Everson-Rose SA, et al. Hot flashes and subclinical cardiovascular disease: findings from the Study of Women’s Health Across the Nation Heart Study. Circulation. 2008;118(12):1234-1240.
6. Thurston RC, Kuller LH, Edmundowicz D, Matthews KA. Historia av värmevallningar och aortaförkalkning bland postmenopausala kvinnor. Menopause. 2010;17(2):256-261.
7. Thurston RC, Sutton-Tyrrell K, Everson-Rose SA, et al. Hot flashes and carotis intima media thickness among midlife women. Menopause. 2011;18(4):352-358.
8. Crandall CJ, Aragaki A, Cauley JA, et al. Associations of menopausal vasomotor symptoms with fracture incidence. J Clin Endocrinol Metab. 2015;100(2):524-534.
9. Maki PM. Verbalt minne och klimakteriet. Maturitas. 2015;82(3):288-290.
10. North American Menopause Society. Positionspromemoria om hormonterapi från 2012 av: North American Menopause Society. Menopause. 2012;19(3):257-271.
11. Palacios S, Silverman SL, de Villiers TJ, et al. En sjuårig randomiserad, placebokontrollerad studie som utvärderar den långsiktiga effekten och säkerheten av bazedoxifen hos postmenopausala kvinnor med osteoporos: effekter på bentäthet och frakturer. Menopause. 2015;22(8):806-813.
12. Archer DF, Freeman EW, Komm BS, et al. Pooled analysis of the effects of conjugated estrogens/bazedoxifene on vasomotor symptoms in the selective estrogens, menopause, and response to therapy trials. J Womens Health (Larchmt). 2016;25(11):1102-1111.
13. FDA. Orange book: godkända läkemedelsprodukter med utvärderingar av terapeutisk likvärdighet. Produktinformation för ANDA 204726. www.accessdata.fda.gov/scripts/cder/ob/results_product.cfm?Appl_Type=A&Appl_No=204726. Tillgänglig den 18 mars 2018.
14. FDA. Drugs@FDA: FDA-godkända läkemedel. www.accessdata.fda.gov/scripts/cder/daf/index.cfm. Tillgänglig den 17 juni 2018.
15. DrugDex . Greenwood Village, CO: Truven Health Analytics, Inc. www.micromedexsolutions.com. Tillgänglig den 15 juni 2018.
16. Constantine G, Graham S, Portman DJ, et al. Kvinnlig sexuell funktion förbättrad med ospemifen hos postmenopausala kvinnor med vulvära och vaginal atrofi: resultat av en randomiserad, placebokontrollerad studie. Climacteric. 2015;18(2):226-232.
17. Labrie F, Archer DF, Koltun W, et al. Efficacy of intravaginal dehydroepiandrosterone (DHEA) on moderate to severe dyspareunia and vaginal dryess, symptoms of vulvovaginal atrophy, and of the genitourinary syndrome of menopause. Menopause. 2016;23(3):243-256.