US Pharm. 2018;43(9):21-26.
ABSTRACT: Terapia de substituție hormonală (HRT) este cel mai eficient tratament pentru simptomele vasomotorii și genito-urinare asociate menopauzei. Efectele adverse asociate cu HRT depind de diverși factori, inclusiv doza, calea, durata de utilizare, momentul inițierii și alegerea agentului. Decizia de a începe TSH trebuie să includă o evaluare a riscurilor, iar TSH trebuie să fie individualizată în funcție de pacientă. Numeroasele opțiuni HRT existente se prezintă într-o gamă largă de doze și forme farmaceutice. Farmaciștii ar trebui să fie capabili să consilieze pacientele cu privire la HRT și la efectele secundare ale acesteia.
Femeia medie va trăi o treime din viață la menopauză sau după menopauză.1 Tratamentul simptomelor menopauzei a căpătat o importanță din ce în ce mai mare din cauza morbidității asociate cu îmbătrânirea la femei.2 Terapia de substituție hormonală (TRH), un termen utilizat pentru a descrie terapia cu estrogeni, terapia combinată estrogen-progesteron sau terapia agonistă sau antagonistă a receptorilor de estrogen, continuă să joace un rol major în atenuarea simptomelor perimenopauzei și postmenopauzei.3 Deși experiența fiecărei femei este diferită, simptomele vasomotorii (VMS) și simptomele vulvovaginale sunt două dintre cele mai frecvente plângeri asociate cu modificările hormonale implicate de menopauză.4
Simptomele menopauzei
VMS sunt unele dintre cele mai frecvente și mai supărătoare simptome ale menopauzei. Bufeurile, caracterizate printr-o senzație bruscă de căldură în partea superioară a pieptului și a feței, care durează între 2 și 4 minute, apar la aproximativ 75% dintre femeile aflate la menopauză.1 Alte VMS posibile sunt transpirația, palpitațiile și anxietatea.1 VMS au fost asociate cu scăderea calității somnului, iritabilitate, dificultăți de concentrare și reducerea calității vieții.3 Mai mult, aceste simptome au fost legate de riscuri cardiovasculare, osoase și cognitive.5-9 HRT a fost recunoscută de mult timp ca fiind cel mai eficient tratament pentru VMS.4,10
În plus față de VMS deranjante, multe femei se confruntă cu simptome vulvovaginale. Se estimează că între 10% și 40% dintre femei se confruntă cu atrofie vaginală.3 Atrofia vaginală poate provoca durere vulvară, arsură și mâncărime; uscăciune vaginală; scurgeri vaginale; dispareunie (raporturi sexuale dificile sau dureroase); și pete sau sângerări după actul sexual.1 Aceste simptome tind să apară în etapa postmenopauzală târzie și pot duce la disconfort la îmbrăcămintea strâmtă, în timpul șederii sau al exercițiilor fizice, sau în timpul activității sexuale.1 HRT topică este de obicei recomandată pentru tratamentul simptomelor vulvovaginale.1
În plus față de ameliorarea simptomelor menționate anterior, există dovezi că HRT standard în doze mici poate preveni, de asemenea, fracturile postmenopauză de șold, de coloană vertebrală și non-spinale.10 Beneficiile TRH pentru SMV și simptomele genito-urinare includ îmbunătățiri ale vezicii urinare hiperactive, scăderea tulburărilor de somn, reducerea riscului de diabet de tip 2, o potențială protecție împotriva bolii coronariene (CAD) și a infarctului miocardic, scăderea riscului de osteoporoză sau fractură și o potențială reducere a mortalității din toate cauzele.1,10 Beneficiile pe care le conferă TRH asupra densității osoase, cu toate acestea, se diminuează rapid după întrerupere. În plus, deși unele produse au aprobarea FDA pentru prevenirea osteoporozei, niciunul dintre ele nu este aprobat în prezent pentru tratamentul osteoporozei. Riscurile majore asociate cu utilizarea acestor agenți includ tromboembolismul venos (TEV), accidentul vascular cerebral ischemic, creșterea incidenței cancerului endometrial (în cazul în care se utilizează un estrogen neopus la o femeie cu uter) și creșterea riscului de cancer de sân atunci când HRT este utilizată peste 3 până la 5 ani.4,10
Produse HRT disponibile
O gamă largă de produse HRT sunt disponibile în diferite forme de dozare.4 Dintre preparatele orale, opțiunile includ estrogeni cabalini conjugați (CEE), 17-beta-estradiol micronizat (micronizat pentru a îmbunătăți absorbția), estrogeni esterificați, etinilestradiol (un preparat estrogenic foarte puternic care este utilizat la doze mult mai mici pentru TRH decât pentru contracepția orală), tablete combinate estrogen-progestativ și o tabletă combinată CEE/bazedoxifen.4
Comprimatul CEE/bazedoxifen, o combinație de estrogeni și un modulator selectiv al receptorilor de estrogeni, este disponibil în Statele Unite pentru tratamentul VMS la menopauză și pentru prevenirea osteoporozei. În această combinație, bazedoxifenul previne hiperplazia endometrială indusă de estrogeni, făcând inutilă administrarea unui progestativ. Cu toate acestea, bazedoxifenul este asociat cu un risc crescut de TEV.4 Utilizarea bazedoxifenului s-a dovedit a fi sigură atunci când a fost studiată timp de până la 7 ani în tratamentul osteoporozei, dar combinația a fost studiată numai pentru durate mai scurte.11,12 Studiile VMS cu o durată de până la 2 ani nu au demonstrat nicio creștere a incidenței sensibilității mamare sau a riscului de cancer mamar.3 Ghidurile actuale recomandă utilizarea CEE/bazedoxifenului la femeile aflate în postmenopauză cu uter și fără contraindicații pentru a trata SMV și a contribui la prevenirea pierderii osoase, dar nu specifică durata tratamentului.1 Pe baza dovezilor disponibile, tratamentul SMV cu CEE/bazedoxifen timp de până la 2 ani pare sigur; siguranța utilizării peste 2 ani rămâne neclară.
HRT este, de asemenea, disponibilă în diverse aplicații topice. Sunt disponibile preparate transdermice cu plasture de 17-betaestradiol sau combinații de estrogeni și progestativ. Alte preparate topice includ pachete de gel sau pompe cu doză măsurată, spray-uri și emulsii.4 Pot fi luate în considerare, de asemenea, injecțiile de depozit, dar aceste produse sunt rareori utilizate în cadrul TRH.4 Un rezumat al formulărilor disponibile de TRH sistemică este prezentat în TABELUL 1.13-15
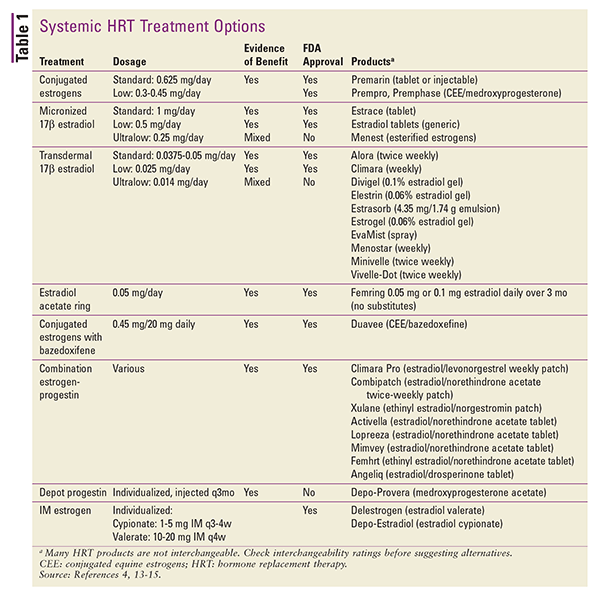
În conversia de la o formă de dozare la alta, diferențele în ceea ce privește calea de administrare și potența produsului pot fi luate în considerare prin utilizarea echivalențelor dozelor estimate.4 Echivalentele dozelor pentru preparatele orale sunt după cum urmează: 1 mg de 17-beta-estradiol micronizat echivalează cu 1,25 mg de sulfat de estronă piperazinică. În conversiile între preparatele de estrogeni orale și transdermice, 0,05 mg/24 ore transdermice echivalează cu aproximativ 0,625 mg zilnic pe cale orală.4
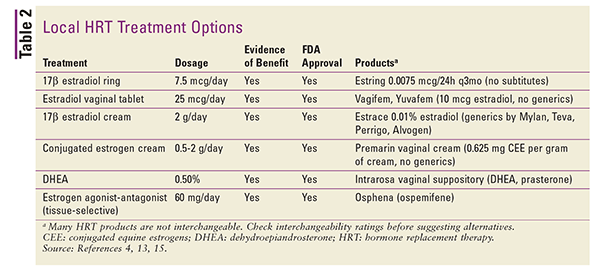
Pregătirile locale sunt, în general, în doze mici și sunt utilizate în mod specific pentru tratamentul simptomelor atrofiei vulvovaginale.4 Doze mai mari pot fi utilizate pentru tratamentul SMV sistemice, dar acest lucru nu este, în general, recomandat.4 Preparatele locale includ inele vaginale, tablete și creme. Consultați TABELUL 2 pentru un rezumat al formulărilor locale disponibile de TRH.4,13,15
Recomandări actuale ale ghidurilor
Trei organizații – Colegiul American al Obstetricienilor și Ginecologilor, Societatea Nord-Americană de Menopauză (NAMS) și Societatea Endocrinologică – au elaborat ghiduri privind utilizarea TRH la menopauză. După cum se menționează în aceste ghiduri, indicațiile pentru HRT includ gestionarea VMS asociate menopauzei și tratamentul efectelor vulvovaginale în absența unor simptome sistemice supărătoare.1,3,4 S-a constatat că estrogenul singur sau în combinație cu un progestativ reduce VMS săptămânal cu 75% și reduce semnificativ severitatea simptomelor în comparație cu placebo.4
La femeile cu vârsta mai mică de 60 de ani care au mai puțin de 10 ani de la menopauză, au SGV deranjante și nu au contraindicații la HRT sau risc cardiovascular sau de cancer mamar excesiv, se recomandă utilizarea terapiei numai cu estrogeni pentru cele fără uter. Adăugarea unui progestativ este recomandată la pacientele cu uter pentru a preveni hiperplazia endometrială și potențialul cancer endometrial.1,3,4 În prezent, expunerea necesară la progestativ este neclară, dar mulți furnizori administrează progestative într-un ciclu de 14 zile în fiecare lună.4 Pentru femeile cu vârsta mai mare de 60 de ani sau care au mai mult de 10 ani după menopauză, se recomandă luarea în considerare a altor terapii (nonhormonale) în locul TRH.3
La femeile cu un risc crescut de boală cardiovasculară (MCV; definit ca >10% risc de MCV pe 10 ani conform instrumentului de estimare a riscului cardiovascular al Colegiului American de Cardiologie/American Heart Association), sunt preferate terapiile nonhormonale.3 La femeile cu risc moderat de MCV, estrogenii transdermici cu sau fără progestativ sunt de preferat terapiei orale, deoarece aceste preparate au un efect mai redus asupra tensiunii arteriale, lipidelor și metabolismului glucidic.1 La pacientele cu un risc crescut de TEV, este preferată utilizarea căilor nonorale la cea mai mică doză eficientă. În cele din urmă, la pacientele cu risc ridicat sau intermediar de cancer de sân, se preferă terapiile nonhormonale.4
Dacă se alege TRH, toate ghidurile recomandă utilizarea celei mai mici doze eficiente.1,4,10 Un beneficiu al dozelor mai mici de TRH este profilul mai bun de efecte secundare în comparație cu regimurile cu doze mari.4 Nu există în prezent o cale terapeutică preferată pentru tratamentul SMV; prin urmare, calea de administrare trebuie să fie ghidată de preferințele pacientei. Trebuie remarcat faptul că produsele transdermice pot fi asociate cu o incidență mai mică a efectelor adverse, cum ar fi TEV, dar studiile sunt încă în curs de desfășurare.10
Pentru tratamentul simptomelor genito-urinare la femeile fără antecedente de cancere hormono-dependente, se pot utiliza estrogeni vaginali în doze mici.1 Pentru simptomele vaginale numai, ghidurile recomandă să nu se adauge progestativ, indiferent dacă este prezent uterul sau nu. Această terapie poate fi, de asemenea, adecvată la pacientele cu antecedente de cancere hormono-dependente, dar în aceste cazuri, alegerea terapiei trebuie să se bazeze pe un proces decizional comun care să includă discutarea riscurilor și beneficiilor. Beneficiile potențiale ale estrogenului vaginal includ îmbunătățirea rapidă a simptomelor vaginale și urinare și posibila prevenire a infecțiilor recurente ale tractului urinar. Terapiile non-estrogenice aprobate de FDA și în concordanță cu ghidurile utilizate pentru ameliorarea dispareuniei includ ospemifenul și dehidropiandrosteronul intravaginal.16,17
Terapia numai cu progestativ, testosteronul, terapiile non-hormonale alternative pe bază de plante și hormonii bioidentici compuși nu dispun de date și, în general, nu sunt recomandate.1,4 NAMS afirmă că medicii prescriptori pot lua în considerare HRT compuși în situațiile în care o pacientă nu poate tolera terapiile aprobate de FDA.3 Opțiunile de tratament nonhormonal pentru simptomele vasomotorii includ inhibitori selectivi ai recaptării serotoninei și inhibitori selectivi ai recaptării serotoninei-norepinefrinei, clonidină și gabapentin, iar tratamentul nonhormonal pentru simptomele vaginale include lubrifianți, agoniști-antagoniști de estrogeni și remedii pe bază de plante.4 Dovezile care susțin utilizarea terapiilor nonhormonale variază și nu toate opțiunile au dovezi dovedite sau o indicație aprobată de FDA.4
Monitorizarea HRT trebuie să includă screening-uri regulate pentru cancerul de sân în timpul și după finalizarea tratamentului. Sângerările recurente neprogramate trebuie evaluate rapid.1 Durata terapiei trebuie revizuită cel puțin o dată pe an, fiind preferată cea mai scurtă durată a tratamentului.1 Atunci când pacientele și furnizorii decid să întrerupă HRT, se poate utiliza fie o strategie de întrerupere conică, fie o strategie de întrerupere bruscă. Lipsesc dovezile cu privire la metodele de întrerupere; prin urmare, se recomandă luarea deciziilor în comun pentru procesul de întrerupere.1,4
Interacțiuni medicamentoase
Majoritatea produselor HRT disponibile în comerț (TABELUL 1) suferă un metabolism hepatic mediat de sistemul CYP450.15 În mod specific, produsele estrogenice sunt parțial metabolizate de CYP3A4; prin urmare, inductorii puternici ai CYP3A4 pot reduce eficacitatea HRT cu estrogeni, iar inhibitorii puternici pot crește concentrațiile serice de estrogen. În plus, alți substraturi medicamentoase pentru aceste enzime pot interfera cu metabolismul TRH.15
Efecte secundare severe și frecvente
Efectele secundare majore asociate cu TRH includ boli cardiovasculare, cancer de sân, cancer endometrial sau ovarian, accident vascular cerebral și TEV.1 Utilizarea estrogenilor fără opoziție crește riscul de hiperplazie endometrială și cancer, de unde și recomandarea de adăugare a progestativului la femeile cu uter. În ceea ce privește riscul de cancer mamar, se pare că există un risc mic de apariție a cancerului mamar atunci când o femeie ia estrogeni timp de 5 ani.3 Literatura de specialitate actuală este inconsecventă în ceea ce privește determinarea riscului de apariție a cancerului ovarian în urma utilizării TRH.3 Sunt necesare mai multe studii randomizate și controlate pentru a stabili adevăratul risc de apariție a cancerului ovarian în urma utilizării TRH.1 Efectele TRH asupra bolii coronariene (CAD), accidentului vascular cerebral și TEV variază în funcție de vârsta femeii la momentul inițierii sau de timpul scurs de la instalarea menopauzei. Se pare că femeile care iau TRH timp de peste 10 ani de la debutul menopauzei prezintă un risc crescut de apariție a bolii coronariene.3 În general, studiile sugerează că formulările orale și transdermice cu doze mai mici conferă un risc mai mic de accident vascular cerebral și TEV în comparație cu TRH cu doze standard.3 Pacientele care au peste 60 de ani la inițierea tratamentului cu TRH sau care au mai mult de 10 ani de la debutul menopauzei prezintă un risc crescut pentru aceste efecte adverse. Mai mult, femeile care iau TRH cu estrogeni, fie singure, fie în combinație, prezintă un risc crescut de calculi biliari, colecistită și colecistectomie.3 Riscul de afecțiuni ale vezicii biliare a fost asociat cu utilizarea TRH pe cale orală și este posibil să nu existe în cazul formulărilor topice sau transdermice.1,3
Contraindicații
Cadrele directoare ale societăților profesionale nu au specificat o listă de contraindicații absolute sau relative la TRH.2 Prin urmare, ca în cazul majorității deciziilor clinice, este importantă o evaluare individualizată a raportului risc-beneficiu. În general, HRT trebuie evitată la pacientele cu sângerare vaginală inexplicabilă; antecedente de accident vascular cerebral sau atac ischemic tranzitoriu; infarct miocardic; embolie pulmonară sau TEV; cancer mamar sau endometrial; boală hepatică activă; deficiență cunoscută de proteină C, proteină S sau antitrombină sau alte tulburări trombofilice; și sarcină cunoscută sau suspectată.1 În plus, trebuie manifestată prudență la pacienții cu diabet zaharat, afecțiuni ale vezicii biliare, hipertrigliceridemie (>400 mg/zi), hipoparatiroidism, meningiom benign, risc intermediar sau ridicat de cancer de sân, risc ridicat de afecțiuni cardiace sau migrenă cu aură.2
Puncte de consiliere
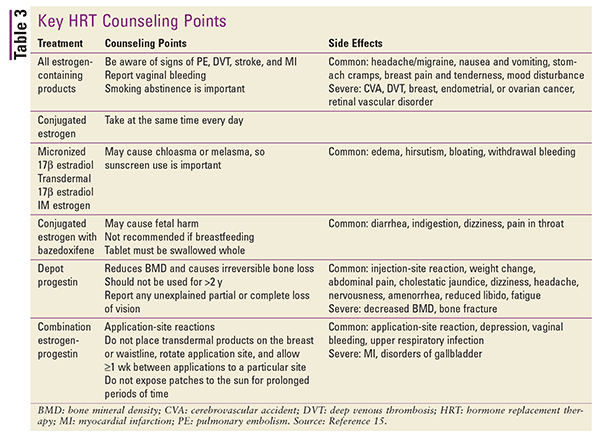
Referiți-vă la TABELUL 3 pentru un rezumat al punctelor cheie de consiliere a pacientelor și al efectelor secundare pentru diferitele tipuri de TRH.15
Concluzie
TRH, care este disponibilă într-o gamă largă de preparate, este cel mai eficient tratament atât pentru SMV, cât și pentru simptomele genito-urinare. Deoarece riscurile asociate cu HRT sunt diferite pentru fiecare femeie, tratamentul trebuie să fie individualizat și să vizeze maximizarea eficacității, minimizarea duratei tratamentului și reducerea riscului de efecte adverse. În scenariile în care TRH nu este o opțiune, sunt disponibile opțiuni de tratament nonhormonal atât pentru SMV, cât și pentru simptomele genito-urinare, dar eficacitatea și aprobarea FDA pentru aceste produse variază; prin urmare, trebuie analizate datele de eficacitate pentru aceste produse.
1. Stuenkel CA, Davis SR, Gompel A, et al. Tratamentul simptomelor menopauzei: un ghid de practică clinică al Societății Endocrine. J Clin Endocrinol Metab. 2015;100(11):3975-4011.
2. Shifren JL, Schiff I. Rolul terapiei hormonale în managementul menopauzei. Obstet Gynecol. 2010;115(4):839-855.
3. The NAMS 2017 Hormone Therapy Position Statement Advisory Panel. Declarația de poziție privind terapia hormonală 2017 a Societății Nord-Americane de Menopauză. Menopauză. 2017;24(7):728-753.
4. ACOG Practice Bulletin No. 141: managementul simptomelor menopauzei. Obstet Gynecol. 2014;123(1):202-216.
5. Thurston RC, Sutton-Tyrrell K, Everson-Rose SA, et al. Bufeurile și bolile cardiovasculare subclinice: constatări din Studiul privind sănătatea femeilor în toată țara Studiul cardiac. Circulation. 2008;118(12):1234-1240.
6. Thurston RC, Kuller LH, Edmundowicz D, Matthews KA. Istoricul de bufeuri și calcifierea aortică în rândul femeilor aflate la postmenopauză. Menopauză. 2010;17(2):256-261.
7. Thurston RC, Sutton-Tyrrell K, Everson-Rose SA, et al. Bufeuri fierbinți și grosimea mediei intime carotide în rândul femeilor de vârstă mijlocie. Menopauză. 2011;18(4):352-358.
8. Crandall CJ, Aragaki A, Cauley JA, et al. Asociații ale simptomelor vasomotorii ale menopauzei cu incidența fracturilor. J Clin Endocrinol Metab. 2015;100(2):524-534.
9. Maki PM. Memoria verbală și menopauza. Maturitas. 2015;82(3):288-290.
10. Societatea nord-americană de menopauză. Declarația de poziție privind terapia hormonală din 2012 a: The North American Menopause Society. Menopauză. 2012;19(3):257-271.
11. Palacios S, Silverman SL, de Villiers TJ, et al. A 7-year randomized, placebo-controlled trial assessing the long-term efficacy and safety of bazedoxifene in postmenopausal women with osteoporosis: effects on bone density and fracture. Menopauză. 2015;22(8):806-813.
12. Archer DF, Freeman EW, Komm BS, et al. Analiza combinată a efectelor estrogenilor conjugați/bazedoxifenului asupra simptomelor vasomotorii în cadrul studiilor privind estrogenii selectivi, menopauza și răspunsul la terapie. J Womens Health (Larchmt). 2016;25(11):1102-1111.
13. FDA. Cartea portocalie: produse medicamentoase aprobate cu evaluări ale echivalenței terapeutice. Detalii despre produs pentru ANDA 204726. www.accessdata.fda.gov/scripts/cder/ob/results_product.cfm?Appl_Type=A&Appl_No=204726. Accesat la 18 martie 2018.
14. FDA. Drugs@FDA: Produse medicamentoase aprobate de FDA. www.accessdata.fda.gov/scripts/cder/daf/index.cfm. Accesat la 17 iunie 2018.
15. DrugDex . Greenwood Village, CO: Truven Health Analytics, Inc. www.micromedexsolutions.com. Accesat la 15 iunie 2018.
16. Constantine G, Graham S, Portman DJ, et al. Funcția sexuală feminină îmbunătățită cu ospemifene la femeile aflate la postmenopauză cu atrofie vulvară și vaginală: rezultatele unui studiu randomizat, controlat cu placebo. Climacteric. 2015;18(2):226-232.
17. Labrie F, Archer DF, Koltun W, et al. Eficacitatea dehidroepiandrosteronului (DHEA) intravaginal asupra dispareuniei moderate până la severe și a uscăciunii vaginale, a simptomelor de atrofie vulvovaginală și a sindromului genito-urinar al menopauzei. Menopauză. 2016;23(3):243-256.