Iată care este problema cu privire la acoperirea „aminelor” în Org 2: nu există nicio narațiune.
În comparație cu majoritatea capitolelor, nu începe cu un set de concepte și apoi se construiește până la o serie de exemple la care puteți aplica apoi acele concepte.
Nu. Un capitol tipic despre amine într-un manual introductiv este, în esență, doar o amestecătură de subiecte aparent aleatorii aruncate împreună care nu se potriveau nicăieri altundeva. Singurul fir unificator este faptul că ele conțin azot într-un fel sau altul.
Cazul de față: postul de astăzi despre amine la întâmplare este despre rearanjamentele Hofmann și Curtius.
Ce ne îndeamnă la asta, ați putea întreba? Nu există un răspuns bun. Majoritatea cursurilor le acoperă la un moment dat și trebuie să se încadreze undeva. Așa că, ce naiba. De ce nu acum?
Tabloul cuprinsului
- Rearanjamentele Hofmann și Curtius
- Mecanismul rearanjamentelor Hofmann și Curtius, Prima parte – Configurarea rearanjamentului
- Partea a doua: Pasul cheie al rearanjamentului în rearanjamentele Hofmann și Curtius
- Partea a treia: Formarea izocianatului
- Completarea etapelor
- Soarta izocianatului: Formarea carbamaților, aminei și ureei
- Summary: The Hofmann and Curtius Rearrangements
- Note
- (Avansat) Referințe și lecturi suplimentare
- Rearanjamentele Hofmann și Curtius
- Mecanismul rearanjamentelor Hofmann și Curtius, Partea 1: Configurarea rearanjamentului
- Partea 1: Preludiu
- 3. Etapa cheie de rearanjare în Hofmann și Curtius
- Formarea izocianatului
- Consolidarea etapelor
- Destinul Izocianatului
- Rezolvare: Rearanjările Hofmann și Curtius
- Note
- (Avansat) Referințe și lecturi suplimentare
Rearanjamentele Hofmann și Curtius
Rearanjamentele Hofmann și Curtius sunt două exemple ale unei întregi familii de reacții de rearanjare care au o etapă mecanică comună.
În rearanjarea Hofmann, o amidă este tratată cu brom și o bază (de obicei NaOH sau KOH). La încălzire, se formează un izocianat intermediar, care nu este izolat. În prezența apei, izocianatul pierde dioxidul de carbon („decarboxilat”) pentru a da o amină.
Legătura cheie care se formează în Hofmann este legătura C2-N. Observați cum se pierde grupa carbonil (C1), formând dioxid de carbon (CO2). (notă: aceasta nu este o numerotare IUPAC, ci doar o numerotare pentru a facilita discuția)
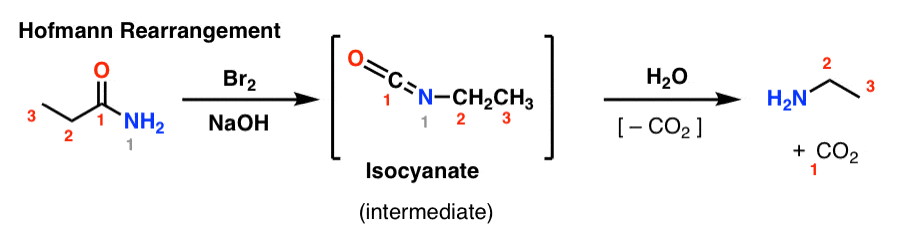
În rearanjarea Curtius, se încălzește o azidă de acil și se formează un izocianat. În Curtius, izocianatul poate fi izolat, dar de obicei este transformat mai departe în alte specii, cum ar fi un carbamat, o uree sau (prin decarboxilare, ca în Hofmann) într-o amină (mai multe despre acestea mai jos).
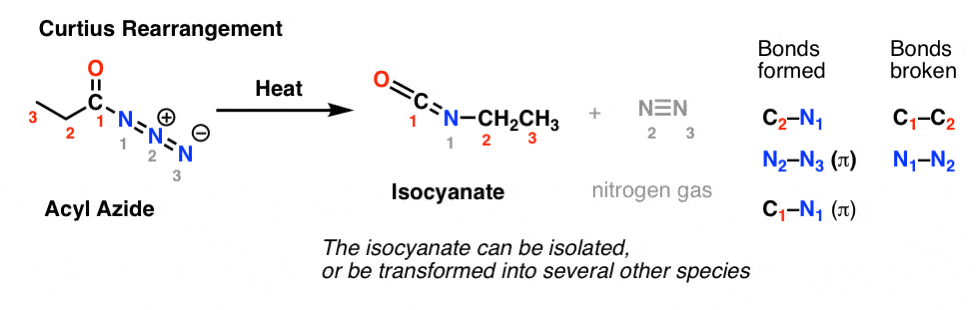
Observația cheie de remarcat în ambele cazuri este că legătura C1-C2 s-a rupt și s-a format o nouă legătură C2-N.
Întrebarea este CUM?
Mecanismul rearanjamentelor Hofmann și Curtius, Partea 1: Configurarea rearanjamentului
Există patru părți importante în mecanismul rearanjamentelor Curtius și Hofmann, iar noi le vom parcurge pe toate.
- Preludiu (simplu)
- Etapa cheie de migrare (complicată, dar mai puțin complicată dacă vă dați seama că ați văzut o variantă a acesteia în Org 1 !)
- Formarea izocianatului (simplu)
4. Epilog: Transformări ale izocianatului
Partea 1: Preludiu
- Rearanjarea Hofmann are loc cu o amidă.
- Rearanjarea Curtius are loc cu o azidă de acil.
Ambele se prepară convenabil din halogenuri de acil printr-o reacție de adiție-eliminare. Dacă vă ocupați acum de amine, atunci reacțiile cu carbonil sunt probabil un teritoriu familiar. Halogenurile de aciil pot fi preparate din acizi carboxilici prin utilizarea unui reactiv cum ar fi clorura de thionil (SOCl2) sau pentaclorura de fosfor (PCl5).
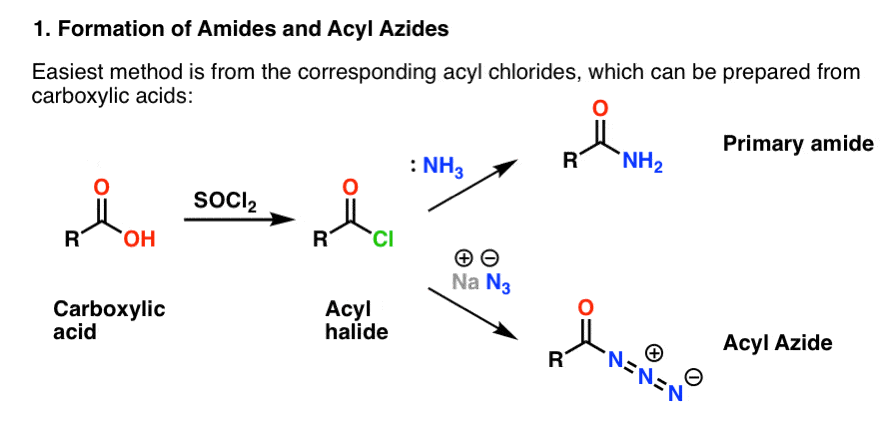
Punerea la punct a reacției Hofmann
În rearanjarea Hofmann, amida este tratată cu brom (Br2) și o bază cum ar fi NaOH. Aceasta are ca rezultat ruperea N-H și formarea de N-Br, ceea ce duce la instalarea unei bune grupări de plecare pe azot. Noi numim aceasta o „N-bromoamidă”.
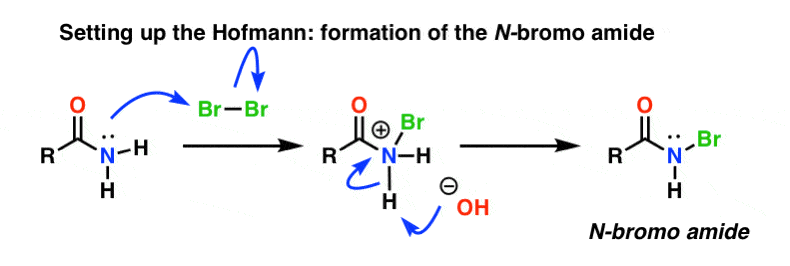
Curtiul nu are nevoie de „instalare”, deoarece azida de acil are deja o splendidă grupare de plecare încorporată: N2. Acesta este motivul pentru care azidele organice trebuie tratate cu grijă, deoarece un tratament dur poate duce la explozii.
3. Etapa cheie de rearanjare în Hofmann și Curtius
Acum trecem la treabă.
Etapa cheie în rearanjările Hofmann și Curtius este migrarea unui atom de carbon pentru a deplasa o grupare de plecare de pe un azot adiacent.
Aceasta necesită desenarea a două săgeți curbe, care sunt prezentate în structura din extrema stângă (mai jos).
- În prima săgeată curbă, se rupe legătura C-C și se formează o nouă legătură C-N.
- În a doua săgeată curbă, se rupe legătura N-LG (grup de plecare).
Cu toate acestea, nu este întotdeauna ușor să treci direct de la structura din extrema stângă la structura din extrema dreaptă (care este desenată frumos și ordonat! ).
În fiecare an, nenumărate puncte sunt pierdute inutil la examene de către elevii care obțin săgețile curbe corect, dar sfârșesc prin a desena structura greșită! De aceea îi încurajez pe studenți să deseneze mai întâi o „versiune urâtă”, care arată ca naiba, dar care cel puțin are toate legăturile la locul potrivit. Există întotdeauna timp pentru a o redesena și a o face să arate frumos mai târziu.
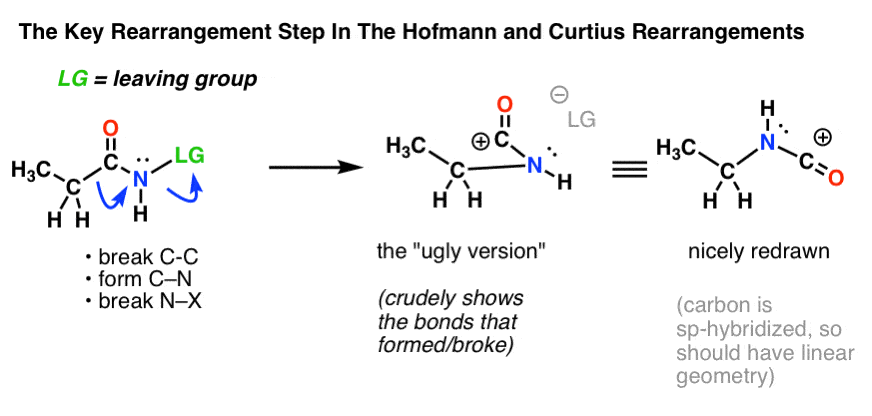
La început, această rearanjare probabil că arată… ciudat. Dar este de fapt o reacție pe care ați mai văzut-o! (dar într-o formă deghizată).
Își mai amintește cineva mecanismul pentru etapa de „oxidare” din hidroborare-oxidare?
Este practic același lucru!
Iată o reîmprospătare:
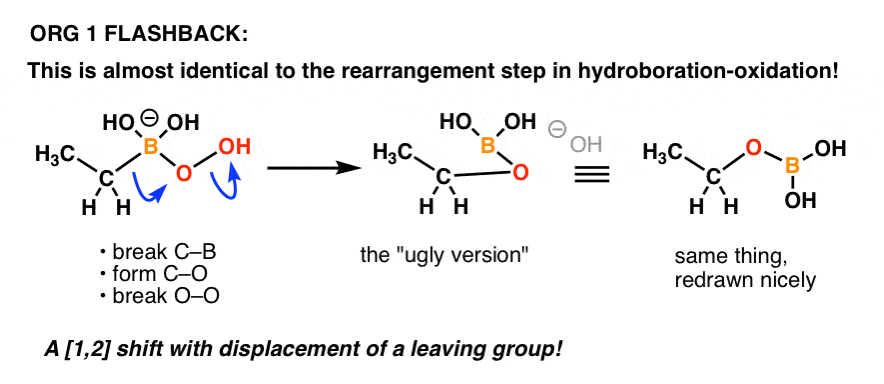
Încă un exemplu despre cum lucrurile pe care le înveți într-o parte anterioară a chimiei organice pot reveni într-o parte ulterioară a cursului!
Să vizităm etapa specifică de rearanjare din rearanjamentele Hofmann și Curtius cu exemple concrete.
Iată etapa cheie din Hofmann, în care încălzirea duce la ruperea C-C , formarea de C-N și ruperea N-Br.
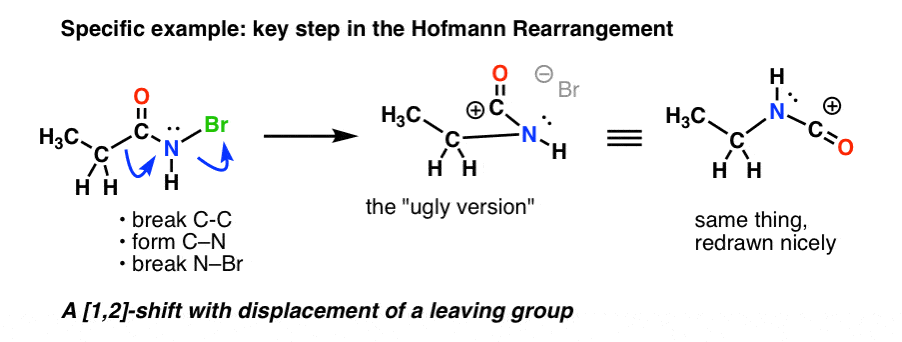
Dacă urmați toate săgețile, ar trebui să ajungeți la un carbocation cu aspect ciudat (mai sus, în dreapta), de care ne vom ocupa imediat.
În Curtius, încălzirea azidei de acil duce la rearanjarea. Gruparea care pleacă este azotul gazos (N2).
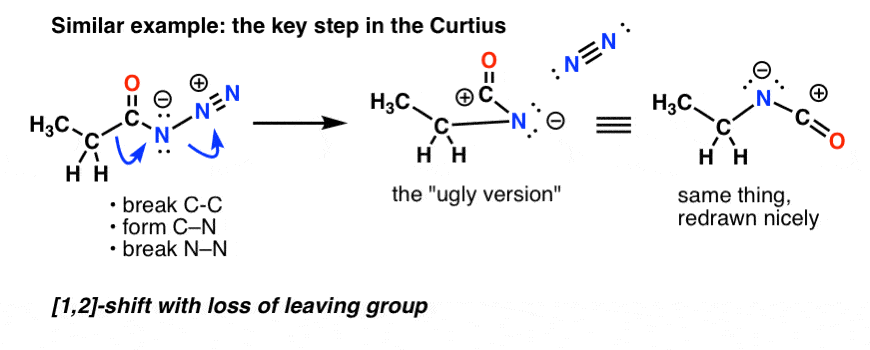
(O diferență subtilă între Curtius și Hofmann este că nu există hidrogen atașat la N în Curtius, astfel încât ajungem să avem o sarcină negativă pe azotul din specia rearanjată.)
Formarea izocianatului
Postul următor este trecerea de la specia noastră rearanjată la izocianat. Pentru oricine este obișnuit să deseneze forme de rezonanță, acest lucru nu ar trebui să fie prea dificil.
(După cum vom discuta mai jos, studiile au determinat că formarea izocianatului are loc în același timp cu migrarea. Dar, pentru scopurile noastre didactice, cred că este util să tratăm această etapă în mod izolat. Putem pune totul cap la cap peste un minut).
După cum poate vă amintiți de la waayyyy back în Org 1, o formă de rezonanță cu octeți compleți este superioară uneia fără (recapitulare rapidă). Produsul nostru cu aspect ciudat de la rearanjarea are un carbocation adiacent unui azot care conține o pereche solitară. Așadar, primul pas este să desenăm formarea unei noi legături C-N pi. Aceasta este, în esență, doar o formă de rezonanță.
Rearanjarea Hofmann are loc în prezența bazei. Deci, după desenarea formei de rezonanță, următorul pas este deprotonarea legăturii N-H care dă izocianatul neutru.
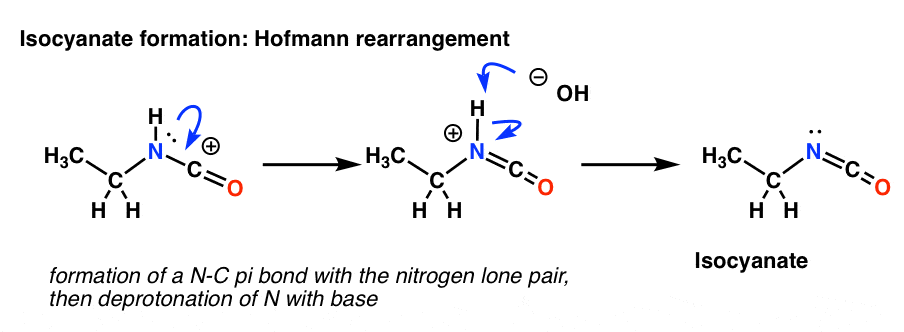
Nu există hidrogen pe azotul din Curtius. Deci formarea izocianatului se realizează pur și simplu prin donarea unei perechi singulare de la azot la carbocation. Se poate privi pur și simplu ca și cum ai desena o formă de rezonanță.
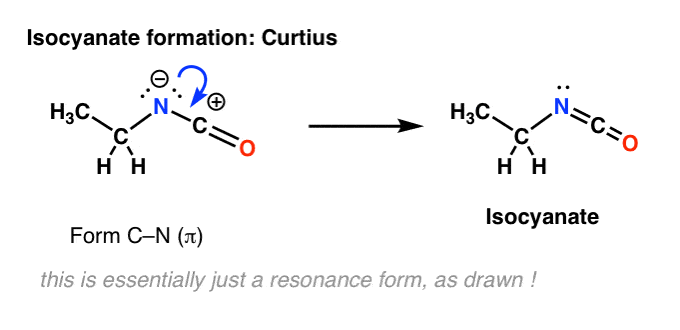
Consolidarea etapelor
Studiile privind mecanismul rearanjamentelor Hofmann și Curtius au determinat că aceste două etape nu au loc secvențial; ele au loc de fapt în același timp! (de unde știm acest lucru? a se vedea Nota 1 )
Acesta este, migrarea are loc în același timp cu formarea izocianatului.
Trebuie să redesenăm mecanismele lui Hofmann și Curtius pentru a reflecta acest lucru, încorporând ambele etape.
Iată Hofmann (observați că evenimentul deprotonării este de fapt separat).
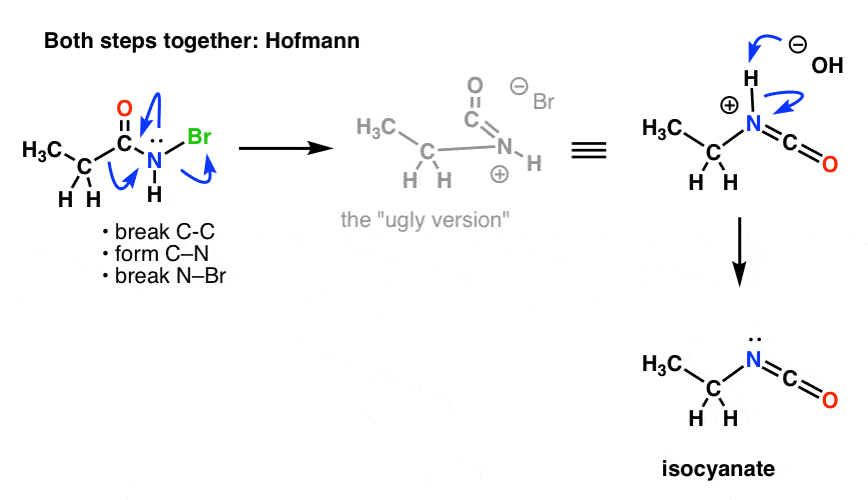
Și Curtius:
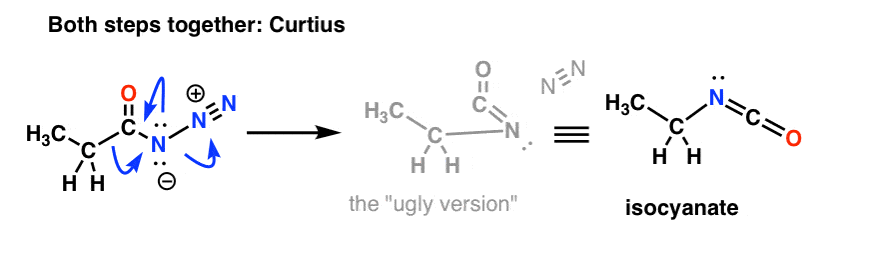
Destinul Izocianatului
Atât Hofmann cât și Curtius dau naștere unui izocianat. Probabil că nu ați mai întâlnit până acum izocianați. La prima vedere, sunt specii cu un aspect destul de ciudat, dar chimia lor nu este atât de diferită de cea a altor specii carbonilice, cum ar fi esterii, amidele și halogenurile de acil.
Structura izocianatului seamănă foarte mult cu cea a dioxidului de carbon, CO2. Carbonul este legat prin legături pi la doi atomi puternic electronegativi. Acest lucru face ca carbonul să fie un electrofil excelent.
Prin adăugarea de diverși nucleofili, izocianații pot fi transformați în alte specii utile.
– Adăugarea unui alcool duce la formarea unui carbamat
– Adăugarea unei amine duce la obținerea unei uree
– Adăugarea de apă duce la obținerea unui acid carbamic, care este instabil. Acizii carbamici pierd rapid dioxidul de carbon pentru a da o amină.
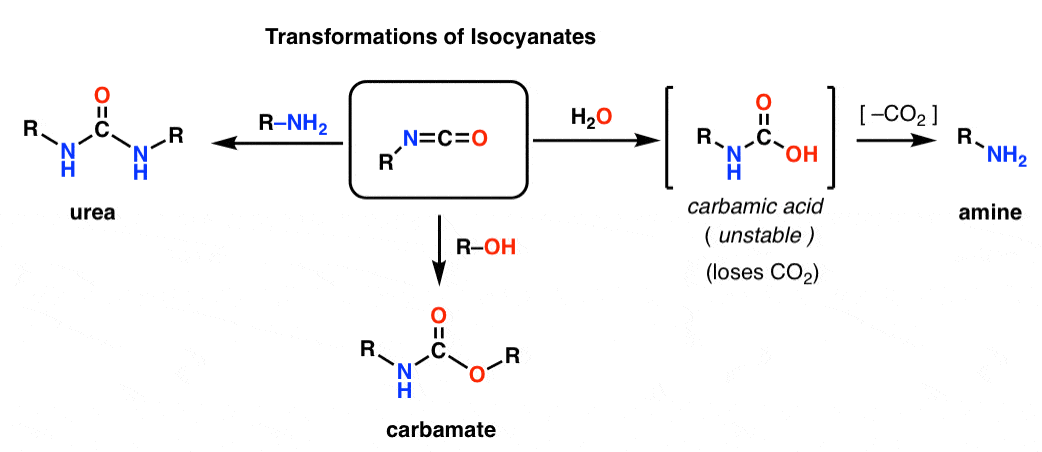
În special, calea de decarboxilare prezintă o modalitate ingenioasă de a obține amine. Am învățat tone de modalități de obținere a acizilor carboxilici, dar nu prea multe modalități de obținere a aminelor (în afară de substituția nucleofilă și aminarea reductivă). Hofmann este un truc bun de avut în buzunarul de la spate în situații în care niciuna dintre aceste situații nu se poate aplica – cum ar fi fabricarea de aniline substituite, de exemplu.
Mecanisme? OK, bine. Vezi subiectul bonus 1.
Rezolvare: Rearanjările Hofmann și Curtius
Mecanismul acestor rearanjări este complicat la prima vedere, dar devine considerabil mai ușor odată ce vă dați seama că ați mai văzut o variantă a reacției de migrare (i.e. în hidroborare-oxidare).
Vă recomand să desenați mai întâi varianta urâtă, pentru că vă va ajuta să vă concentrați pe a vedea legăturile care se formează și se rup, înainte de a încerca să o redesenați într-o structură mai atrăgătoare din punct de vedere estetic. Acest lucru este valabil și pentru rearanjamentele Beckmann și Wolff, care au o etapă similară.(vezi mai jos)
Note
Tema bonus 1: Izocianați
Mecanismul cel mai important al izocianaților este adiția electrofilă (adică adăugarea unui nucleofil la carbonul central, electrofil). În mecanismul de mai jos am arătat nucleofilul care se adaugă la carbon astfel încât să formeze un anion pe azot, deși probabil că aceasta nu este cea mai bună formă de rezonanță (oxigenul stabilizează mai bine sarcina negativă decât azotul). Transferul de protoni de la oxigen la azot are ca rezultat o specie neutră. (Am folosit aici bagheta magică a transferului de protoni, pentru că este mai rapidă).
Rețineți că etapa de decarboxilare din 1) nu trebuie să fie precedată de deportarea oxigenului, deși cu siguranță trebuie să aibă loc astfel încât azotul să fie protonat în timpul etapei (nu doriți să formați un ion amidă puternic bazic, de exemplu).
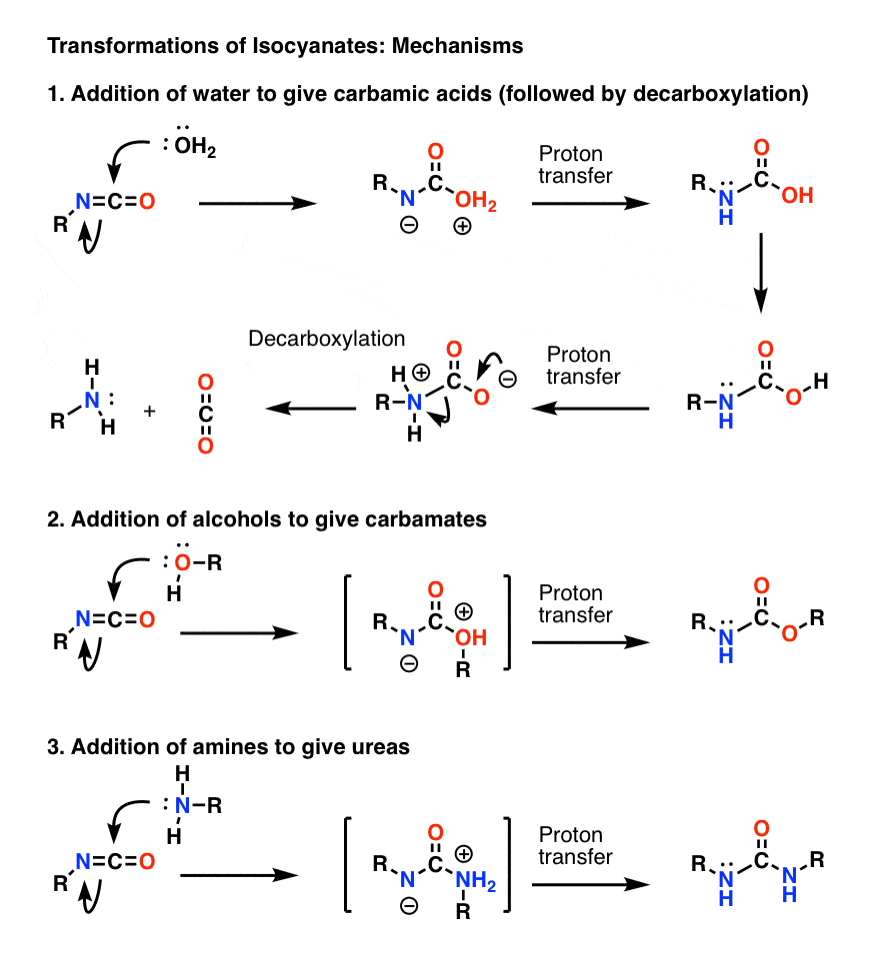
Subiectul bonus 2: Rearanjamentele Beckmann, Wolff și alte rearanjamente au în comun o etapă similară
Dar așteptați, mai este ceva!
Există o deplasare 1,2 cu pierderea unei grupări de plecare în rearanjarea Beckmann. Pasul cheie este, în esență, același pe care l-am văzut în Hofmann și Curtius.
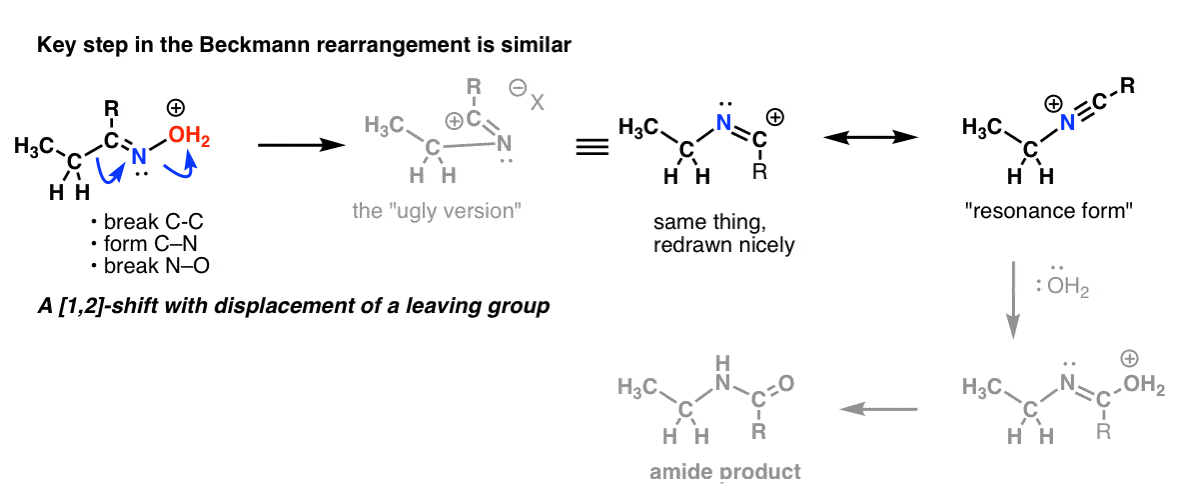
Și în rearanjarea Wolff, care este de asemenea abordată în mod obișnuit, s-ar putea să recunoașteți același pas cheie.
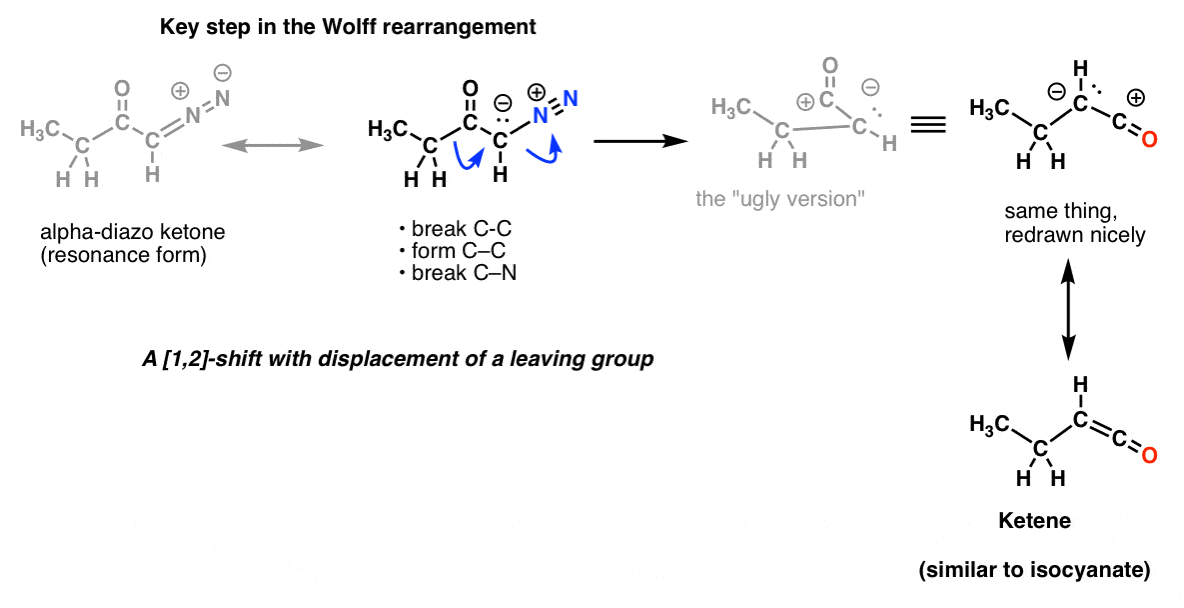
Și asta nu e tot! Există o reacție numită rearanjarea Schmidt, care este ca și cea de Curtius, dar care provine din adăugarea de HN3 la o clorură de acil (sau la un acid carboxilic). Și mai există o alta, numită rearanjarea Lossen, care are loc cu acizii hidroxiamici. Nu există premii pentru a ghici care este pasul cheie în aceste două procese. Și nici măcar nu am menționat Baeyer-Villiger, care nu implică azotul, dar care este cam același tip de proces.
Când am învățat etapa de hidroborare-oxidare din Org 1, cu multe luni în urmă, cu siguranță nu m-am așteptat niciodată că voi vedea același model de reacție repetându-se în atât de multe forme diferite.
Legătura de bază este că există o mulțime de reacții care poartă nume diferite și care se desfășoară prin același proces mecanic. Acest lucru evidențiază importanța învățării modelelor cheie în chimia organică, deoarece cu siguranță se repetă foarte mult.
Nota finală. Concertată, nu separată?
Dacă Curtius a fost în trepte, pierderea de azot ar duce la un nitren. Nitrenii suferă o serie de reacții interesante, cum ar fi inserția în legături C-H (!). Așadar, se poate concepe un experiment pentru a testa acest lucru: dacă se încearcă următoarea rearanjare Curtius, se pot căuta dovezi de formare a unui inel cu cinci membri.
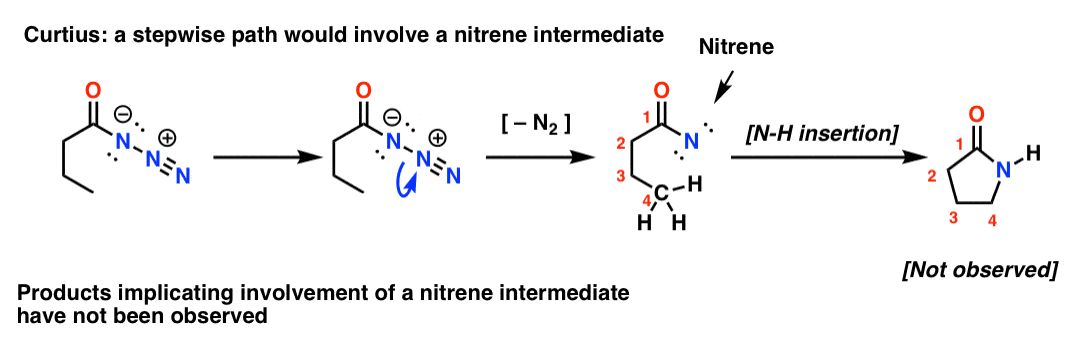
Absența unor astfel de produși, împreună cu alte dovezi, indică un mecanism concertat.
(Avansat) Referințe și lecturi suplimentare
- Ueber die Einwirkung des Broms in alkalischer Lösung auf Amide
W. Hofmann
Chem. Ber. 1881, 14, 2725-2736
DOI: 10.1002/cber.188101402242
Articol original al lui A. W. Hofmann (care a fost un chimist foarte productiv și al cărui nume este atribuit multor alte transformări) privind degradarea amidelor în amine primare. - A Mild and Efficient Modified Hofmann Rearrangement
Xicai Huang, Mehran Seid, and Jeffrey W. Keillor
The Journal of Organic Chemistry 1997, 62 (21), 7495-7496
DOI:10.1021/jo9708553
Aceasta este o rearanjare Hofmann modificată efectuată în metanol – în acest caz, acidul carbamic intermediar poate reacționa cu solventul metanol pentru a produce carbamați de metil cu un randament bun. - FORMAREA DE CARBAMAȚI DE METIL PRIN REACȚII MODIFICATE DE REARANJARE HOFMANN: METHYL N-(p-METHOXYPHENYL)CARBAMATE
Jeffrey W. Keillor și Xicai Huang
Org. Synth. 2002, 78, 234
DOI: 10.15227/orgsyn.078.0234
O procedură fiabilă și testată independent pentru rearanjarea Hofmann modificată din Ref. 2. - Reacția Hofmann
Wallis, Everett L.; Lane, John F.
Org. React. 1946, 3, 267-306
DOI: 10.1002/0471264180.or003.07
O analiză veche, dar cuprinzătoare (pentru vremea sa) a reacției Hofmann (reacția de la amidă la amină, a nu se confunda cu celelalte reacții ale sale). - Notes – A Re-examination of the Limitations of the Hofmann Reaction
Ernest Magnien and Richard Baltzly
The Journal of Organic Chemistry 1958, 23 (12), 2029-2032
DOI:10.1021/jo01106a630
Aceasta este o lucrare interesantă în care autorii au încercat să extindă domeniul de aplicare al rearanjării Hofmann dincolo de ceea ce a fost descris în lucrarea originală prin ajustarea atentă a condițiilor de reacție. - 20. Hydrazide und Azide organischer Säuren
Curtius, T. I. Abhandlung.
Journal Für Praktische Chemie, 50(1), 275-294. (1894).
DOI:1002/prac.18940500125 - Ueber Stickstoffwasserstoffsäure (Azoimid) N3H.
Curtius, T.
Berichte Der Deutschen Chemischen Gesellschaft, 23(2), 3023-3033.(1890).
DOI:1002/cber.189002302232
Primele lucrări ale lui Theodore Curtius care descriu reactivitatea hirazidelor de acil și a azidelor de acil. - The Curtius Reaction
Smith, P. A. S.
Org. React. 1946, 3, 336
DOI: 10.1002/0471264180.or003.09
O analiză veche, dar cuprinzătoare a reacției Curtius, care include istoria descoperirii acestei rearanjări, domeniul de aplicare a substratului, limitările, comparația cu alte reacții similare și procedurile experimentale. - ISOCIANATE DE UNDECIL
F. H. Allen și Alan Bell
Org. Synth. 1944, 24, 94
DOI: 10.15227/orgsyn.024.0094
O procedură veche, dar reproductibilă și testată pentru sinteza izocianaților prin rearanjarea Curtius. - O sinteză totală expeditivă fără grup de protecție a (±)-Dievodiaminei
William P. Unsworth, Christiana Kitsiou și Richard J. K. K. Taylor
Organic Letters 2013 15 (13), 3302-3305
DOI:1021/ol4013469
Prima etapă a acestei sinteze totale folosește o rearanjare Curtius pentru a efectua o ciclizare intramoleculară a acidului carboxilic substituit cu indol. - Metode și reacții de sinteză. 121. Prepararea catalizată cu iodură de zinc a azidelor de aroil din cloruri de aroil și azidă de trimetilsililil
K. Surya Prakash, Pradeep S. Iyer, Massoud Arvanaghi și George A. Olah
The Journal of Organic Chemistry 1983 48 (19), 3358-3359
DOI: 10.1021/jo00167a051
O procedură convenabilă pentru prepararea azidelor arilice aromatice de la Prof. George A. Olah, laureat al Premiului Nobel. Acestea pot fi apoi folosite pentru rearanjamentele Curtius.
.