Denumire generică: fluocinonidă
Forma farmaceutică: Gel
Revizuit medical de Drugs.com. Actualizat ultima dată la 22 iunie 2020.
- Overview
- Efecte secundare
- Dosare
- Profesional
- Interacțiuni
- Mai mult
Dozaj numai pentru prescripție medicală
Numele de marcă Lidex a fost întrerupt în SUA.S. Dacă versiunile generice ale acestui produs au fost aprobate de FDA, este posibil să existe echivalente generice disponibile.
- Lidex Descriere
- Lidex – Farmacologie clinică
- Farmacocinetică
- Indicații și mod de utilizare pentru Lidex
- Contraindicații
- Precauții
- Generalități
- Informații pentru pacient
- Teste de laborator
- Carcinogeneză, mutageneză și afectarea fertilității
- Categoria de fertilitate C
- Mamele care alăptează
- Utilizare pediatrică
- Reacții adverse
- Supradozaj
- Dosare și mod de administrare a Lidex
- Cum se administrează Lidex
- Întrebări frecvente
- Mai multe informații despre Lidex (fluocinonidă topică)
- Resurse pentru consumatori
- Resurse profesionale
- Ghiduri de tratament conexe
Lidex Descriere
Lidex® (fluocinonidă) Gel 0,05% este destinat administrării topice. Componenta activă este corticosteroidul fluocinonidă, care este esterul 21-acetat al acetonidei de fluocinolonă și are denumirea chimică pregna-1,4-dienă-3,20-dionă,21-(acetiloxi)-6,9-difluoro-11-hidroxi-16,17–,(6α,11β,16α)-. Are următoarea structură chimică:
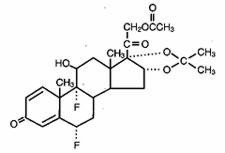
Lidex Gel conține fluocinonidă 0,5 mg/g într-o bază de gel special formulată, compusă din carbomer 940, edetat disodic, galat de popil, propilenglicol, hidroxid de sodiu și/sau acid clorhidric (pentru ajustarea pH-ului) și apă (purificată). Acest vehicul limpede, incolor, tixotropic este lipsit de grăsime, nu pătează și este complet miscibil cu apa.
În această formulare, ingredientul activ este în totalitate în soluție.
Lidex – Farmacologie clinică
Corticosteroizii topici au în comun acțiuni antiinflamatoare, antipruriginoase și vasoconstrictoare.
Mecanismul activității antiinflamatoare a corticosteroizilor topici este neclar. Diferite metode de laborator, inclusiv teste de vasoconstricție, sunt utilizate pentru a compara și a prezice potențele și/sau eficacitatea clinică a corticosteroizilor topici. Există unele dovezi care sugerează că există o corelație recognoscibilă între potența vasoconstrictorului și eficacitatea terapeutică la om.
Farmacocinetică
Dimensiunea absorbției percutanate a corticosteroizilor topici este determinată de mai mulți factori, inclusiv vehiculul, integritatea barierei epidermice și utilizarea pansamentelor ocluzive.
Corticosteroizii topici pot fi absorbiți din pielea normală intactă. Inflamația și/sau alte procese patologice la nivelul pielii cresc absorbția percutanată. Pansamentele ocluzive cresc substanțial absorbția percutanată a corticosteroizilor topici. Astfel, pansamentele ocluzive pot fi un adjuvant terapeutic valoros pentru tratamentul dermatozelor rezistente (vezi DOZE ȘI ADMINISTRARE).
După ce sunt absorbiți prin piele, corticosteroizii topici sunt gestionați prin căi farmacocinetice similare cu corticosteroizii administrați pe cale sistemică. Corticosteroizii sunt legați de proteinele plasmatice în grade diferite. Corticosteroizii sunt metabolizați în principal în ficat și sunt apoi excretați de rinichi. Unii dintre corticosteroizii topici și metaboliții lor sunt, de asemenea, excretați în bilă.
Indicații și mod de utilizare pentru Lidex
Lidex Gel este indicat pentru ameliorarea manifestărilor inflamatorii și pruriginoase ale dermatozelor care răspund la corticosteroizi.
Contraindicații
Corticosteroizii topici sunt contraindicați la acei pacienți cu antecedente de hipersensibilitate la oricare dintre componentele preparatului.
Precauții
Generalități
Absorbția sistemică a corticosteroizilor topici a produs suprimarea reversibilă a axei hipotalamo-hipofizo-suprarenale (HPA), manifestări ale sindromului Cushing, hiperglicemie și glucozurie la unii pacienți.
Condițiile care măresc absorbția sistemică includ aplicarea steroizilor mai puternici, utilizarea pe suprafețe mari, utilizarea prelungită și adăugarea de pansamente ocluzive.
Prin urmare, pacienții care primesc o doză mare de un steroid topic puternic aplicat pe o suprafață mare sau sub un pansament ocluziv trebuie evaluați periodic pentru a se constata dacă există dovezi de supresie a axei HPA prin utilizarea testelor de stimulare cu cortizol liber urinar și ACTH. Dacă se observă suprimarea axei HPA, trebuie să se încerce retragerea medicamentului, reducerea frecvenței de aplicare sau înlocuirea cu un steroid mai puțin puternic.
Recuperarea funcției axei HPA este, în general, promptă și completă la întreruperea medicamentului. Rareori, pot apărea semne și simptome de retragere a steroizilor, necesitând suplimentarea corticosteroizilor sistemici.
Copiii pot absorbi cantități proporțional mai mari de corticosteroizi topici și, prin urmare, pot fi mai susceptibili la toxicitate sistemică (vezi pct. PRECAUȚII – Uz pediatric). În cazul apariției iritației, corticosteroizii topici trebuie întrerupți și trebuie instituit un tratament adecvat.
Ca și în cazul oricărui produs corticosteroidic topic, utilizarea prelungită poate produce atrofierea pielii și a țesuturilor subcutanate. Atunci când se utilizează pe zonele intertriginoase sau flexoare, sau pe față, acest lucru poate apărea chiar și în cazul utilizării pe termen scurt.
În prezența infecțiilor dermatologice, trebuie instituită utilizarea unui agent antifungic sau antibacterian adecvat. Dacă nu apare prompt un răspuns favorabil, corticosteroidul trebuie întrerupt până când infecția a fost controlată în mod adecvat.
Informații pentru pacient
Pacienții care utilizează corticosteroizi topici trebuie să primească următoarele informații și instrucțiuni:
- Acest medicament trebuie utilizat conform indicațiilor medicului. Este numai pentru uz extern. Evitați contactul cu ochii.
- Pacienții trebuie sfătuiți să nu utilizeze acest medicament pentru orice altă afecțiune decât cea pentru care a fost prescris.
- Zona de piele tratată nu trebuie bandajată sau acoperită sau înfășurată în alt mod, astfel încât să fie ocluzivă, decât la indicația medicului.
- Pacienții trebuie să raporteze orice semne de reacții adverse locale, în special sub pansament ocluziv.
- Părinții pacienților pediatrici trebuie sfătuiți să nu folosească scutece strânse sau pantaloni de plastic la un copil tratat în zona de scutec, deoarece aceste articole de îmbrăcăminte pot constitui pansamente ocluzive.
Teste de laborator
Următoarele teste pot fi utile în evaluarea suprimării axei HPA:
Testul de cortizol liber urinar
Testul de stimulare a ACTH
Carcinogeneză, mutageneză și afectarea fertilității
Nu au fost efectuate studii pe termen lung pe animale pentru a evalua potențialul carcinogen sau efectul asupra fertilității al corticosteroizilor topici.
Studiile pentru determinarea mutagenității cu prednisolon și hidrocortizon au dat rezultate negative.
Categoria de fertilitate C
Corticosteroizii sunt în general teratogeni la animalele de laborator atunci când sunt administrați pe cale sistemică la doze relativ mici. Corticosteroizii mai puternici s-au dovedit a fi teratogeni după aplicarea cutanată la animalele de laborator. Nu există studii adecvate și bine controlate la femeile gravide privind efectele teratogene ale corticosteroizilor aplicați local. Prin urmare, corticosteroizii topici trebuie utilizați în timpul sarcinii numai dacă beneficiul potențial justifică riscul potențial pentru făt. Medicamentele din această clasă nu trebuie utilizate în mod extensiv la pacientele gravide, în cantități mari sau pentru perioade prelungite de timp.
Mamele care alăptează
Nu se știe dacă administrarea topică de corticosteroizi ar putea avea ca rezultat o absorbție sistemică suficientă pentru a produce cantități detectabile în laptele matern. Corticosteroizii administrați pe cale sistemică sunt secretați în laptele matern în cantități care nu sunt susceptibile de a avea un efect nociv asupra sugarului. Cu toate acestea, trebuie să se manifeste prudență atunci când corticosteroizii topici sunt administrați unei femei care alăptează.
Utilizare pediatrică
Pacienții pediatrici pot prezenta o susceptibilitate mai mare la supresia axei HPA indusă de corticosteroizi topici și la sindromul Cushing indusă de corticosteroizi decât pacienții maturi, din cauza unui raport mai mare între suprafața cutanată și greutatea corporală.
Supresia axei hipotalamo-hipofizo-suprarenale (HPA), sindromul Cushing și hipertensiunea intracraniană au fost raportate la copiii care primesc corticosteroizi topici. Manifestările supresiei suprarenale la copii includ întârzierea creșterii liniare, creșterea în greutate întârziată, niveluri plasmatice scăzute de cortizol și absența răspunsului la stimularea cu ACTH. Manifestările de hipertensiune intracraniană includ fontanele bombate, cefalee și papilism bilateral.
Administrarea de corticosteroizi topici la copii trebuie limitată la cea mai mică cantitate compatibilă cu un regim terapeutic eficient. Terapia cronică cu corticosteroizi poate interfera cu creșterea și dezvoltarea copiilor.
Reacții adverse
Celelalte reacții adverse locale sunt raportate rar cu corticosteroizii topici, dar pot apărea mai frecvent la utilizarea pansamentelor ocluzive. Aceste reacții sunt enumerate într-o ordine aproximativ descrescătoare de apariție:
| Mâncărime | Dermatită parietală |
| Mâncărime | Dermatită alergică de contact |
| Irritare | Macerația pielii |
| Secarea | Infecție secundară |
| Foliculită | Atrofia pielii |
| Hipertricoză | Striații |
| Erupții acneiforme | Miliară |
| Hipopigmentare |
Supradozaj
Corticosteroizii aplicați topic pot fi absorbiți în cantități suficiente pentru a produce efecte sistemice (vezi pct. PRECAUȚII).
Dosare și mod de administrare a Lidex
Lidex Gel se aplică în general pe zona afectată sub formă de peliculă subțire de două până la patru ori pe zi, în funcție de severitatea afecțiunii.
Pansamentul ocluziv poate fi utilizat pentru tratamentul psoriazisului sau al afecțiunilor recalcitrante.
În cazul apariției unei infecții, trebuie întreruptă utilizarea pansamentelor ocluzive și trebuie instituit un tratament antimicrobian adecvat.
Cum se administrează Lidex
Lidex® (fluocinonidă) Gel 0.05% este furnizat în
Tub de 15 g – NDC 99207-507-13
Tub de 30 g – NDC 99207-507-14
Tub de 60 g – NDC 99207-507-17
Conservați la temperatura camerei 15°-30°C (59°-86°F).
Fabricat pentru:
MEDICIS, The Dermatology Company®
Scottsdale, AZ 85258
Aprilie 2001
În-5071/S
| Lidex fluocinonidă gel |
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
Etichetă – MEDICIS
Întrebări frecvente
- Se folosește pentru căderea părului?
- Care este un substitut pentru crema de fluocinonidă?
- Fluocinonida este o cremă antifungică?
- Cât timp trebuie să utilizați fluocinonida?
- La ce este bună crema de fluocinonidă?
- Se poate folosi fluocinonida pentru a trata o erupție de iederă otrăvitoare?
- Este un steroid?
- Este un antibiotic?
Mai multe informații despre Lidex (fluocinonidă topică)
- Efecte secundare
- În timpul sarcinii sau alăptării
- Informații privind dozajul
- Interacțiuni medicamentoase
- 8 Recenzii
- Disponibilitate generică
- Clasa de medicament: steroizi topici
Resurse pentru consumatori
- Lectură avansată
- Lidex Mild (lectură avansată)
- Lidex Regular (lectură avansată)
- Lidex Regular (lectură avansată)
.
Resurse profesionale
- Informații pentru prescriere
- Lidex Topical Solution (FDA)
- Lidex Unguent (FDA)
Alte mărci Vanos, Lidex-E
Ghiduri de tratament conexe
- Dermatită atopică
- Eczema
- Dermatită
- Psoriazis
Denunțare medicală
.