În această serie, Colin Baker de la Bedford School oferă demonstrații spectaculoase, concepute pentru a capta imaginația elevilor. Demonstrațiile sunt ușor de pregătit, sigure și funcționează.
Nimic nu tinde să imprime faptele chimice în minte atât de mult ca expunerea unor experimente interesante – Samuel Parkes, 1816
În septembrie 1931, chimistul american Wallace Carothers, care lucra în laboratoarele DuPont, a raportat cercetări asupra unor molecule „gigantice” numite polimeri, bazate pe o înțelegere a structurii chimice a lânii. Munca sa s-a concentrat pe o fibră denumită simplu „66”, un număr derivat din structura sa moleculară. În 1935, s-a născut nailonul, „fibra miraculoasă”, care a avut un succes uriaș pe piața sa inițială, cea a ciorapilor pentru femei. Când Statele Unite au intrat în cel de-al Doilea Război Mondial, în decembrie 1941, Consiliul pentru Producția de Război a alocat întreaga producție de nailon pentru uz militar, inclusiv pentru parașute și anvelope pentru bombardierele B29.

Sursa: Colin Baker
Reacția dintre diclorura de decanedioil și 1,6-diaminohexan
O clorură de diacid într-un solvent organic formează un strat imiscibil cu o diamină alifatică în apă. La interfață, unde cele două soluții incolore se întâlnesc, se formează un polimer alb, cu lanț lung. Această peliculă de polimer poate fi trasă de la interfață și este imediat înlocuită pe măsură ce este îndepărtată. Dacă nu mai trageți, nu pare să se întâmple nimic – reacția se oprește, dar este reluată imediat când începeți să trageți din nou. Reacția poate avea loc timp de mai multe ore.

Sursa: Colin Baker
Kit
- Ciclohexan, 100cm3 (iritant, foarte inflamabil);
- Diclorură de decanedioil, 5.0cm3;
- Apă distilată, 100cm3;
- Carbonat de sodiu anhidru, 10g;
- 1,6-diaminohexan, 5,0g;
- Două pahare, 250cm3;
- Beaker, 5cm3;
- Tweezers;
- Bățulețe de sticlă.
Siguranță
Decanedioil diclorura și 1,6-diaminohexanul sunt corozive. Sunt nocive dacă sunt înghițite sau inhalate, iar în contact cu pielea provoacă arsuri. Sunt iritanți severi. Ciclohexanul este foarte inflamabil și iritant.
Procedură
Pregătiți următoarele două soluții:
Soluția A: diclorură de decanedioil în ciclohexan. Se pun 100cm3 ciclohexan într-un pahar de 250cm3, se adaugă 5,0cm3 diclorură de decanedioil și se amestecă pentru dizolvare. Această soluție se păstrează timp de aproximativ patru săptămâni.
Soluția B: 1,6-diaminohexan în carbonat de sodiu apos. Se pun 100cm3 de apă distilată într-un pahar de 250cm3, se adaugă 10g de carbonat de sodiu anhidru și se amestecă până la dizolvare. Se adaugă 5,0 g de 1,6-diaminohexan solid și se amestecă până la dizolvare.
Se toarnă 2cm3 de soluție A într-un pahar de 5 cm3. Adăugați cu grijă un volum egal de soluție B. Soluția A conține solventul organic, este mai densă decât stratul apos și, prin urmare, este stratul inferior. Prindeți cu o pensetă pelicula de poliamidă (un solid alb) care începe să se formeze la interfața dintre aceste două soluții și scoateți-o încet din pahar. Înfășurați fibra în jurul unei tije de sticlă și continuați să trageți. Opriți procesul atunci când unul dintre reactanți este epuizat.
Sugestii speciale
Atenție la adăugarea celei de-a doua soluții pentru a evita amestecul. Demonstrați cum poate fi trasă fibra într-un fir continuu și apoi organizați un concurs pentru a vedea care pereche de elevi poate produce cea mai lungă fibră. Aceștia ar trebui să fie capabili să producă până la 5 m înainte ca fibra să se rupă. Își vor da seama rapid că au nevoie de ajutor pentru a susține fibra – am împărțit clasa în două grupuri mari, fiecare înarmat cu tije de sticlă. Elevii mei au produs fibre de peste 30 m, încercând chiar să ocolească colțuri. Va trebui să limitați volumul maxim al fiecărei soluții la 10cm3. Elevii trebuie să poarte mănuși și să evite contactul cu fibrele. Dacă fibra se rupe, atunci trebuie înfășurată în hârtie absorbantă. Orice scurgere trebuie curățată cu hârtie absorbantă și aruncată la gunoi.
Obiective didactice
Poliamidele sunt polimeri în care unitățile repetitive sunt ținute împreună prin legături amidice, -CO-NH-.
Nylon-6,10
Nylon-6,10 este fabricat din doi monomeri, unul conține șase atomi de carbon, iar celălalt 10 – de unde și numele său. Monomerul cu 10 atomi de carbon este diclorura de decanedioil (ClOC(CH2)8 COCl), o clorură acidă cu o grupare -COCl la fiecare capăt. Celălalt monomer este un lanț cu șase atomi de carbon cu o grupare amino, -NH2, la fiecare capăt. Acesta este 1,6-diaminohexanul (H2 N(CH2)6 NH2, cunoscut și sub numele de hexan-1,6-diamină).
Când acești doi compuși se polimerizează, grupările amină și acidă se combină, de fiecare dată cu pierderea unei molecule de clorură de hidrogen:
n ClOC-(CH2)8-COCl + n H2N-(CH2)6-NH2 → -(CO-(CH2)8-CONH-(CH2)6-NH)n – + n HCl
Acest proces de formare a polimerilor care implică pierderea unei molecule mici este cunoscut sub numele de polimerizare prin condensare.
Nylon-6,6
Acest polimer se obține prin condensarea a două molecule cu șase atomi de carbon, acidul hexanedioic și 1,6-diaminohexanul. În industrie, ciclohexanul este utilizat pentru a obține ambii monomeri. Dacă ciclohexanul este oxidat, inelul se deschide și ambele capete ale lanțului au o grupare acidă – se formează acidul hexanedioic. Dacă acest acid este neutralizat cu amoniac, se produce sarea de diamoniu (NH4 OOCCH2 CH2 CH2 CH2 CH2 COONH4), care poate fi deshidratată (prin încălzire la 350°C) și redusă (folosind H2/Ni) la 1,6-diaminohexan. Are loc polimerizarea prin condensare a diacidului și a diaminei, cu pierderea de apă:
n HOOC-(CH2)4 -COOH + n H2 N-(CH2)6 -NH2 → -(CO-(CH2)4 -CONH-(CH2)6 -NH)n – + n H2 O
Nylon-6
Este posibil să se obțină nailon din caprolactamul monomer unic (hexahidro-2H-azepin-2-one, 1).
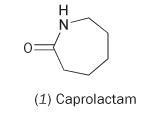
Caprolactama conține o legătură amidă internă. Polimerizarea acestei molecule are ca rezultat deschiderea inelului și alăturarea pentru a forma un lanț continuu:
-(NH-(CH2)5 -CONH-(CH2)5 -CONH-(CH2)5 -CO)n –
Nylon a revoluționat industria textilă și a fost precursorul multor fibre sintetice moderne de astăzi. Acesta rămâne un material important și utilizat pe scară largă în producție.