US Pharm. 2018;43(9):21-26.
ABSTRACT: Hormoonvervangingstherapie (HRT) is de meest effectieve behandeling voor de vasomotorische en genitourinaire symptomen die gepaard gaan met de menopauze. Bijwerkingen van HRT zijn afhankelijk van verschillende factoren, waaronder dosering, route, duur van het gebruik, tijdstip van starten, en keuze van het middel. De beslissing om met HRT te beginnen moet een risicobeoordeling omvatten, en HRT moet op de patiënt worden afgestemd. De vele bestaande HRT-opties komen in een breed scala van doseringen en doseringsvormen. Apothekers moeten patiënten kunnen adviseren over HRT en de bijwerkingen ervan.
De gemiddelde vrouw leeft een derde van haar leven in of na de menopauze.1 Behandeling van menopauzale symptomen is steeds belangrijker geworden vanwege de morbiditeiten die gepaard gaan met het ouder worden van vrouwen.2 Hormoonvervangingstherapie (HRT), een term die wordt gebruikt om oestrogeentherapie, oestrogeen-progesteron-combinatietherapie of oestrogeenreceptoragonist- of antagonisttherapie aan te duiden, speelt nog steeds een belangrijke rol bij de vermindering van perimenopauzale en postmenopauzale symptomen.3 Hoewel de ervaring van elke vrouw anders is, zijn vasomotorische symptomen (VMS) en vulvovaginale symptomen twee van de meest voorkomende klachten die gepaard gaan met de hormonale veranderingen in de menopauze.4
Menopauzale symptomen
VMS behoren tot de meest voorkomende en meest lastige menopauzale symptomen. Opvliegers, gekenmerkt door een plotseling gevoel van warmte in de borst en het gezicht dat 2 tot 4 minuten aanhoudt, komen bij ongeveer 75% van de vrouwen in de menopauze voor.1 Andere mogelijke VMS zijn transpiratie, hartkloppingen en angst.1 VMS zijn in verband gebracht met verminderde slaapkwaliteit, prikkelbaarheid, concentratieproblemen en verminderde levenskwaliteit.3 Bovendien zijn deze symptomen in verband gebracht met cardiovasculaire, bot- en cognitieve risico’s.5-9 HRT wordt al lang erkend als de meest effectieve behandeling voor VMS.4,10
Naast hinderlijke VMS hebben veel vrouwen last van vulvovaginale symptomen. Geschat wordt dat 10% tot 40% van de vrouwen last heeft van vaginale atrofie.3 Vaginale atrofie kan leiden tot vulvaire pijn, branderigheid en jeuk; vaginale droogheid; vaginale afscheiding; dyspareunie (moeilijke of pijnlijke geslachtsgemeenschap); en spotting of bloeding na geslachtsgemeenschap.1 Deze symptomen treden meestal op in de late postmenopauzale fase en kunnen leiden tot ongemak bij strakzittende kleding, tijdens zitten of sporten, of bij seksuele activiteit.1 Topische HRT wordt meestal aanbevolen voor de behandeling van vulvovaginale symptomen.1
Naast het verlichten van de eerder genoemde symptomen zijn er aanwijzingen dat standaard HRT in lage doses ook postmenopauzale heup-, ruggengraat- en niet-ruggengraatfracturen kan voorkomen.10 Voordelen van HRT voor VMS en urogenitale symptomen zijn onder andere verbetering van de overactieve blaas, minder slaapstoornissen, minder risico op diabetes type 2, mogelijke bescherming tegen coronaire hartziekte (CAD) en myocardinfarct, minder risico op osteoporose of fracturen, en een mogelijke vermindering van de mortaliteit als gevolg van alle oorzaken.1,10 De voordelen van HRT voor de botdichtheid nemen echter snel af na het staken van de behandeling. Bovendien, hoewel sommige producten door de FDA zijn goedgekeurd voor de preventie van osteoporose, is geen van hen momenteel goedgekeurd voor de behandeling van osteoporose. Belangrijke risico’s verbonden aan het gebruik van deze middelen zijn veneuze trombo-embolie (VTE), ischemische beroerte, verhoogde incidentie van endometriumkanker (als een onopgelegd oestrogeen wordt gebruikt bij een vrouw met een baarmoeder), en verhoogd risico op borstkanker als HRT langer dan 3 tot 5 jaar wordt gebruikt.4,10
Beschikbare HRT-producten
Er is een breed scala van HRT-producten beschikbaar in verschillende doseringsvormen.4 Tot de orale preparaten behoren geconjugeerde paardenoestrogenen (CEE), gemicroniseerd 17-bèta-oestradiol (gemicroniseerd om de absorptie te verbeteren), veresterde oestrogenen, ethinyl-oestradiol (een zeer krachtig oestrogeenpreparaat dat in veel lagere doseringen wordt gebruikt voor HRT dan voor orale anticonceptie), oestrogeen-progestine-combinatietabletten, en een CEE/bazedoxifeen-combinatietablet.4
De CEE/bazedoxifeen-tablet, een combinatie van oestrogeen en een selectieve oestrogeenreceptormodulator, is in de Verenigde Staten verkrijgbaar voor de behandeling van menopauzale VMS en de preventie van osteoporose. In deze combinatie voorkomt bazedoxifeen oestrogeen-geïnduceerde endometriumhyperplasie, waardoor de toediening van een progestageen overbodig wordt. Bazedoxifeen wordt echter in verband gebracht met een verhoogd risico op VTE.4 Het gebruik van bazedoxifeen is veilig bevonden wanneer het gedurende maximaal 7 jaar werd onderzocht voor de behandeling van osteoporose, maar de combinatie is alleen voor kortere perioden onderzocht.11,12 Onderzoeken naar VMS met een duur tot 2 jaar hebben geen toename aangetoond van de incidentie van borsttederheid of van het risico op borstkanker.3 De huidige richtlijnen bevelen het gebruik van CEE/bazedoxifeen aan bij postmenopauzale vrouwen met een baarmoeder en zonder contra-indicaties om VMS te behandelen en botverlies te helpen voorkomen, maar specificeren niet de duur van de therapie.1 Op basis van het beschikbare bewijsmateriaal lijkt behandeling van VMS met CEE/bazedoxifeen gedurende maximaal 2 jaar veilig; de veiligheid van gebruik na 2 jaar blijft onduidelijk.
HRT is ook beschikbaar in verschillende topische toepassingen. Transdermale patchpreparaten van 17-bèta-oestradiol of oestrogeen-progestinecombinaties zijn beschikbaar. Andere topische preparaten zijn gelpakketjes of doseerpompen, sprays en emulsies.4 Depotinjecties kunnen ook worden overwogen, maar deze producten worden zelden gebruikt in het kader van HRT.4 Een overzicht van beschikbare systemische HRT-formuleringen wordt gegeven in TABEL 1.13-15
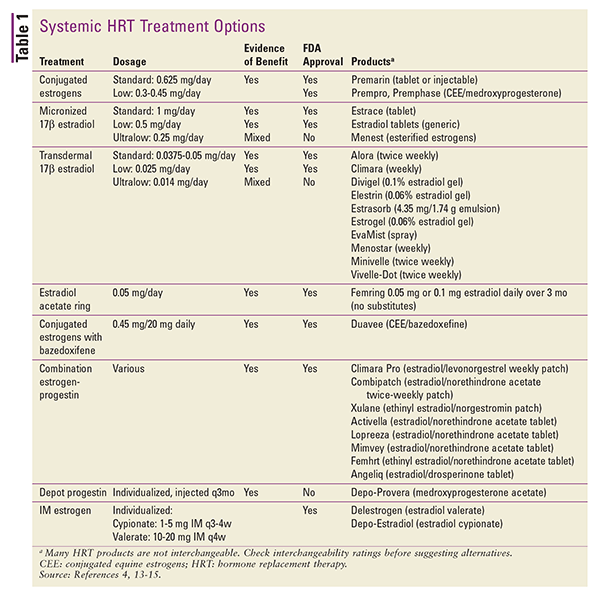
Bij de omzetting van de ene doseringsvorm naar de andere kan rekening worden gehouden met verschillen in toedieningsweg en werkzaamheid van het product door gebruik te maken van geschatte dosisequivalenten.4 Dosisequivalenten voor orale preparaten zijn als volgt: 1 mg gemicroniseerd 17-bèta-oestradiol is gelijk aan 1,25 mg piperazine-oestronensulfaat. Bij omrekening tussen orale en transdermale oestrogeenpreparaten is 0,05 mg/24 uur transdermaal gelijk aan ongeveer 0,625 mg per dag via de mond.4
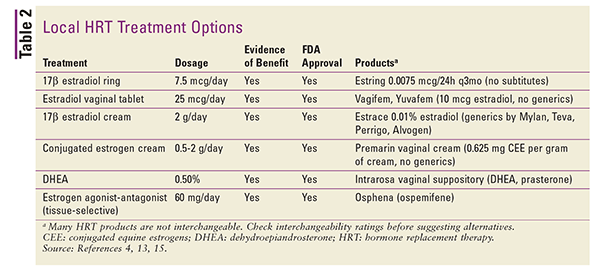
Lokale preparaten zijn over het algemeen laaggedoseerd en worden specifiek gebruikt voor de behandeling van symptomen van vulvovaginale atrofie.4 Hogere doses kunnen worden gebruikt voor de behandeling van systemische VMS, maar dit wordt over het algemeen niet aanbevolen.4 Lokale preparaten omvatten vaginale ringen, tabletten en crèmes. Zie TABEL 2 voor een overzicht van de beschikbare lokale HRT-formuleringen.4,13,15
Current Guideline Recommendations
Drie organisaties – het American College of Obstetricians and Gynecologists (Amerikaans College van Verloskundigen en Gynaecologen), de North American Menopause Society (NAMS) en de Endocrine Society (Endocrine Society) – hebben richtlijnen opgesteld voor het gebruik van HRT in de menopauze. Zoals in deze richtlijnen wordt vermeld, zijn de indicaties voor HRT onder meer de behandeling van VMS in verband met de menopauze en de behandeling van vulvovaginale effecten als er geen hinderlijke systemische symptomen zijn.1,3,4 Oestrogeen alleen of in combinatie met een progestageen bleek de wekelijkse VMS met 75% te verminderen en de ernst van de symptomen aanzienlijk te verminderen in vergelijking met placebo.4
Bij vrouwen jonger dan 60 jaar die minder dan 10 jaar na de menopauze zijn, hinderlijke VMS hebben, en geen contra-indicaties hebben voor HRT of een te hoog risico hebben op hart- en vaatziekten of borstkanker, wordt het gebruik van uitsluitend oestrogeentherapie aanbevolen voor degenen zonder baarmoeder. Bij patiënten met een baarmoeder wordt toevoeging van een progestageen aanbevolen om endometriumhyperplasie en mogelijk endometriumkanker te voorkomen.1,3,4 Momenteel is de vereiste progestageenblootstelling onduidelijk, maar veel aanbieders geven progestageen in een cyclus van 14 dagen per maand.4 Voor vrouwen ouder dan 60 jaar of die meer dan 10 jaar na de menopauze zijn, wordt de overweging van andere (niet-hormonale) therapieën aanbevolen in plaats van HRT.3
Bij vrouwen met een verhoogd risico op hart- en vaatziekten (CVD; gedefinieerd als >10% 10-jaars risico op CVD volgens de American College of Cardiology/American Heart Association cardiovascular risk estimator tool) hebben niet-hormonale therapieën de voorkeur.3 Bij vrouwen met een matig risico op CVD wordt de voorkeur gegeven aan transdermaal oestrogeen met of zonder progestageen boven orale therapie, omdat deze preparaten minder effect hebben op de bloeddruk, de lipiden en het koolhydraatmetabolisme.1 Bij patiënten met een verhoogd risico op VTE wordt de voorkeur gegeven aan het gebruik van niet-orale middelen in de laagste effectieve dosis. Tenslotte wordt bij patiënten met een hoog of gemiddeld borstkankerrisico de voorkeur gegeven aan niet-hormonale therapieën.4
Indien voor HRT wordt gekozen, wordt in alle richtlijnen het gebruik van de laagste effectieve dosis aanbevolen.1,4,10 Een voordeel van lagere doses HRT is het betere bijwerkingenprofiel in vergelijking met hoge-doseringsschema’s.4 Er is momenteel geen voorkeursbehandelroute voor de behandeling van VMS; daarom moet de toedieningsroute worden bepaald door de voorkeur van de patiënt. Opgemerkt moet worden dat transdermale producten geassocieerd kunnen zijn met een lagere incidentie van bijwerkingen, zoals VTE, maar studies worden nog uitgevoerd.10
Voor de behandeling van urogenitale symptomen bij vrouwen zonder een voorgeschiedenis van hormoonafhankelijke kankers, kan laaggedoseerd vaginaal oestrogeen worden gebruikt.1 Voor alleen vaginale symptomen wordt in de richtlijnen de toevoeging van progestine afgeraden, ongeacht of de baarmoeder aanwezig is. Deze therapie kan ook geschikt zijn bij patiënten met een voorgeschiedenis van hormoonafhankelijke vormen van kanker, maar in die gevallen moet de keuze van de therapie gebaseerd zijn op een gezamenlijk besluitvormingsproces, waarbij de risico’s en voordelen worden besproken. Mogelijke voordelen van vaginaal oestrogeen zijn een snelle verbetering van vaginale en urinaire symptomen en mogelijke preventie van terugkerende urineweginfecties. Niet-oestrogene FDA-goedgekeurde en richtlijnconforme therapieën die worden gebruikt om dyspareunie te verlichten zijn ospemifeen en intravaginaal dehydropiandrosteron.16,17
Progestine-only therapie, testosteron, plantaardige alternatieve niet-hormonale therapieën, en samengestelde bio-identieke hormonen hebben geen gegevens en worden over het algemeen niet aanbevolen.1,4 De NAMS stelt dat voorschrijvers samengestelde HRT kunnen overwegen in situaties waarin een patiënt geen FDA-goedgekeurde therapieën kan verdragen.3 Niet-hormonale behandelingsopties voor vasomotorische symptomen zijn onder meer selectieve serotonineheropnameremmers en selectieve serotonine-noradrenalineheropnameremmers, clonidine en gabapentine, en niet-hormonale behandeling voor vaginale symptomen zijn onder meer glijmiddelen, oestrogeenagonisten en kruidenremedies.4 Het bewijs voor het gebruik van niet-hormonale therapieën varieert, en niet alle opties hebben bewezen bewijs of een door de FDA goedgekeurde indicatie.4
Monitoring van HRT moet regelmatige borstkankerscreenings omvatten tijdens en na voltooiing van de therapie. Terugkerende ongeplande bloedingen moeten snel worden beoordeeld.1 De duur van de therapie moet ten minste jaarlijks opnieuw worden bekeken, en de kortste behandelingsduur verdient de voorkeur.1 Wanneer patiënten en zorgverleners besluiten om te stoppen met HRT, kan ofwel een taps toelopende of een abrupte stopzettingsstrategie worden gebruikt. Er is onvoldoende bewijs voor methoden van staken; daarom wordt gezamenlijke besluitvorming aanbevolen voor het proces van staken.1,4
Drug-Drug Interactions
De meeste in de handel verkrijgbare HRT-producten (TABEL 1) ondergaan levermetabolisme dat wordt bemiddeld door het CYP450-systeem.15 Met name oestrogeenproducten worden gedeeltelijk gemetaboliseerd door CYP3A4; daarom kunnen sterke inducers van CYP3A4 de werkzaamheid van oestrogeen-HST verminderen en kunnen sterke remmers de serumconcentraties van oestrogeen verhogen. Bovendien kunnen andere drugsubstraten voor deze enzymen het metabolisme van HRT verstoren.15
Severe en veel voorkomende bijwerkingen
De belangrijkste bijwerkingen van HRT zijn CVD, borstkanker, endometrium- of eierstokkanker, beroerte en VTE.1 Gebruik zonder oestrogeen verhoogt het risico op endometriumhyperplasie en -kanker, vandaar de aanbeveling om progestine toe te voegen bij vrouwen met een baarmoeder. Wat betreft het risico op borstkanker, lijkt er een klein risico te bestaan op het ontwikkelen van borstkanker wanneer een vrouw 5 jaar lang oestrogeen gebruikt.3 De huidige literatuur is inconsistent wat betreft het bepalen van het risico op het ontwikkelen van eierstokkanker door HRT.3 Er zijn meer gerandomiseerde, gecontroleerde onderzoeken nodig om het werkelijke risico op het ontwikkelen van eierstokkanker door HRT-gebruik vast te stellen.1 De effecten van HRT op coronaire hartziekten (CAD), beroertes en VTE variëren afhankelijk van de leeftijd van een vrouw op het moment van starten of de tijd sinds het begin van de menopauze. Het blijkt dat vrouwen die meer dan 10 jaar na het begin van de menopauze HRT gebruiken, een verhoogd risico lopen op het ontwikkelen van CAD.3 In het algemeen suggereren studies dat orale en transdermale formuleringen met lagere doseringen een lager risico op beroerte en VTE geven in vergelijking met HRT met standaarddosering.3 Patiënten die ouder dan 60 jaar zijn wanneer zij met HRT beginnen of die meer dan 10 jaar na het begin van de menopauze zijn, lopen een verhoogd risico op deze bijwerkingen. Bovendien lopen vrouwen die HRT met oestrogeen alleen of in combinatie gebruiken een verhoogd risico op galstenen, cholecystitis en cholecystectomie.3 Het risico op galblaasaandoeningen is in verband gebracht met het gebruik van orale HRT en bestaat mogelijk niet bij topische of transdermale formuleringen.1,3
Contra-indicaties
Richtlijnen van beroepsverenigingen hebben geen lijst van absolute of relatieve contra-indicaties voor HRT gespecificeerd.2 Daarom is, zoals bij de meeste klinische besluitvorming, een geïndividualiseerde afweging van risico’s en voordelen belangrijk. In het algemeen moet HRT worden vermeden bij patiënten met onverklaarbare vaginale bloedingen; een voorgeschiedenis van beroerte of een transient ischemic attack; myocardinfarct; longembolie of VTE; borst- of endometriumkanker; actieve leverziekte; bekend proteïne C-, proteïne S-, of antitrombinetekort of andere trombofiele aandoeningen; en bekende of vermoede zwangerschap.1 Bovendien is voorzichtigheid geboden bij patiënten met diabetes, galblaasaandoeningen, hypertriglyceridemie (>400 mg/dag), hypoparathyreoïdie, benigne meningioom, intermediair of hoog risico op borstkanker, hoog risico op hartaandoeningen, of migraine met aura.2
Consultatiepunten
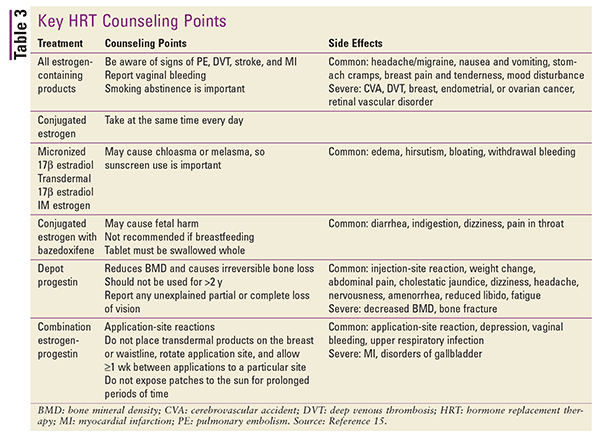
Refereer naar TABEL 3 voor een samenvatting van de belangrijkste adviespunten en bijwerkingen voor de verschillende soorten HRT.15
Conclusie
HRT, dat verkrijgbaar is in een breed scala van preparaten, is de meest effectieve behandeling voor zowel VMS als genitourinaire symptomen. Omdat de risico’s van HRT voor elke vrouw anders zijn, moet de behandeling op de persoon worden afgestemd en gericht zijn op maximale werkzaamheid, minimale therapieduur en vermindering van het risico van bijwerkingen. In scenario’s waarin HRT geen optie is, zijn er niet-hormonale behandelingsopties voor zowel VMS als genitourinaire symptomen beschikbaar, maar de werkzaamheid en goedkeuring van deze producten door de FDA variëren; daarom moeten de werkzaamheidsgegevens voor deze producten worden beoordeeld.
1. Stuenkel CA, Davis SR, Gompel A, et al. Behandeling van symptomen van de menopauze: een richtlijn voor de klinische praktijk van de Endocrine Society. J Clin Endocrinol Metab. 2015;100(11):3975-4011.
2. Shifren JL, Schiff I. Rol van hormoontherapie in het beheer van de menopauze. Obstet Gynecol. 2010;115(4):839-855.
3. The NAMS 2017 Hormone Therapy Position Statement Advisory Panel. De 2017 hormoontherapie position statement van de North American Menopause Society. Menopauze. 2017;24(7):728-753.
4. ACOG Practice Bulletin No. 141: management of menopausal symptoms. Obstet Gynecol. 2014;123(1):202-216.
5. Thurston RC, Sutton-Tyrrell K, Everson-Rose SA, et al. Opvliegers en subklinische cardiovasculaire aandoeningen: bevindingen van de Study of Women’s Health Across the Nation Heart Study. Circulation. 2008;118(12):1234-1240.
6. Thurston RC, Kuller LH, Edmundowicz D, Matthews KA. History of hot flashes and aortic calcification among postmenopausal women. Menopauze. 2010;17(2):256-261.
7. Thurston RC, Sutton-Tyrrell K, Everson-Rose SA, et al. Opvliegers en carotis intima media thickness among midlife women. Menopauze. 2011;18(4):352-358.
8. Crandall CJ, Aragaki A, Cauley JA, et al. Associations of menopausal vasomotor symptoms with fracture incidence. J Clin Endocrinol Metab. 2015;100(2):524-534.
9. Maki PM. Verbaal geheugen en de menopauze. Maturitas. 2015;82(3):288-290.
10. North American Menopause Society. De 2012 hormoontherapie position statement van: The North American Menopause Society. Menopauze. 2012;19(3):257-271.
11. Palacios S, Silverman SL, de Villiers TJ, et al. A 7-year randomized, placebo-controlled trial assessing the long-term efficacy and safety of bazedoxifene in postmenopausal women with osteoporosis: effects on bone density and fracture. Menopause. 2015;22(8):806-813.
12. Archer DF, Freeman EW, Komm BS, et al. Pooled analysis of the effects of conjugated oestrogens/bazedoxifene on vasomotor symptoms in the selective oestrogens, menopause, and response to therapy trials. J Womens Health (Larchmt). 2016;25(11):1102-1111.
13. FDA. Orange book: goedgekeurde geneesmiddelen met evaluaties van therapeutische gelijkwaardigheid. Productgegevens voor ANDA 204726. www.accessdata.fda.gov/scripts/cder/ob/results_product.cfm?Appl_Type=A&Appl_No=204726. Accessed March 18, 2018.
14. FDA. Drugs@FDA: FDA approved drug products. www.accessdata.fda.gov/scripts/cder/daf/index.cfm. Accessed June 17, 2018.
15. DrugDex . Greenwood Village, CO: Truven Health Analytics, Inc. www.micromedexsolutions.com. Accessed June 15, 2018.
16. Constantine G, Graham S, Portman DJ, et al. Vrouwelijke seksuele functie verbeterd met ospemifeen bij postmenopauzale vrouwen met vulvar- en vaginale atrofie: resultaten van een gerandomiseerde, placebogecontroleerde trial. Climacteric. 2015;18(2):226-232.
17. Labrie F, Archer DF, Koltun W, et al. Werkzaamheid van intravaginale dehydroepiandrosteron (DHEA) op matige tot ernstige dyspareunie en vaginale droogheid, symptomen van vulvovaginale atrofie, en van het genitourinaire syndroom van de menopauze. Menopause. 2016;23(3):243-256.