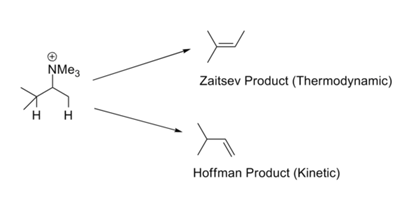
In reacties zoals Hofmann’s Exhaustieve Methylerings – Eliminatie reacties wordt in het algemeen de minst gesubstitueerde olefine als hoofdproduct gevormd. Dit wordt de Hofmann-regel genoemd. Al deze reacties hebben geladen verlaten groepen zoals -NR3+ of -SR2+ en impliceren sterke basen. De regel van Zaitsev (of Saytzeff-regel) vestigt onze aandacht op de alternatieve mogelijkheid. Bij eliminatie van HX wordt de stabielere olefine verkregen (fig. 2.3.1). De schijnbare tegenspraak in deze reeks regels is gemakkelijk op te lossen door een kritische blik op de mechanismen die bij deze twee reeksen reactieomstandigheden betrokken zijn.
Er kunnen twee redenen zijn voor dergelijke voorkeuren. Ingold (1960) en Bunnett (1969) suggereerden dat een positief geladen vertrekkende groep de zuurgraad van de β-protonen verhoogt. Een substituent op de β-positie zou hyperconjugatief de zuurgraad van het β-proton kunnen verlagen. Bijgevolg is een terminale methylgroep (die geen alkylsubstituent heeft) zuurder dan het interne methine-proton (dat ten minste één alkylsubstituent draagt). Wanneer de vertrekkende groep een halogeen is, verschuift het mechanisme naar E1. Onder deze omstandigheden wordt de stabiliteit van de zich ontwikkelende dubbele binding belangrijk en dit leidt tot het thermodynamisch stabielere product. De school van H.C. Brown had gesuggereerd (1956) dat sterische factoren dergelijke eliminatiereacties bepalen. De geladen verlatende groepen zijn groot vergeleken met neutrale verlatende groepen.
De grotere verlatende groepen zoals -NR3+ en -SR2+ geven meer Hoffmann-product dan kleinere groepen zoals halogenen. De volumineusheid van de base verhoogt ook het Hoffmann-product ten koste van het Zaitsav-product. De situatie blijkt complexer te zijn. Wanneer de sterkte van de base werd verhoogd zonder de bulk op de reactieplaats (X-C6H4-O¯) te vergroten, nam het Hoffmann-product toe ten koste van het Zaitsav-product (Froemsdorf (1966,67)). Dit suggereert een E1cB-mechanisme, waarbij de zuurgraad van het β-proton belangrijk is. Het mechanisme (en dus de samenstelling van de producten) zou dus kunnen worden gewijzigd door factoren zoals de grootte van de vertrekkende groep, de grootte van de base, de aard van de vertrekkende groep en de sterkte van de base.
Bijdragers
- Prof. R Balaji Rao (Departement Chemie, Banaras Hindu Universiteit, Varanasi) als onderdeel van Informatie- en Communicatietechnologie