US Pharm. 2018;43(9):21-26.
ABSTRACT: Die Hormonersatztherapie (HRT) ist die wirksamste Behandlung für vasomotorische und genitourinäre Symptome im Zusammenhang mit der Menopause. Unerwünschte Wirkungen im Zusammenhang mit der HRT hängen von verschiedenen Faktoren ab, darunter die Dosierung, die Art und Weise, die Dauer der Anwendung, der Zeitpunkt des Beginns und die Wahl des Mittels. Die Entscheidung, eine HRT zu beginnen, sollte eine Risikobewertung beinhalten, und die HRT sollte individuell auf die Patientin abgestimmt werden. Die vielen bestehenden HRT-Optionen werden in einer Vielzahl von Dosierungen und Darreichungsformen angeboten. Apotheker sollten in der Lage sein, Patienten über die HRT und ihre Nebenwirkungen zu beraten.
Die durchschnittliche Frau wird ein Drittel ihres Lebens in oder nach der Menopause leben.1 Die Behandlung von Wechseljahrsbeschwerden hat aufgrund der mit dem Altern der Frau verbundenen Morbiditäten zunehmend an Bedeutung gewonnen.2 Die Hormonersatztherapie (HRT), ein Begriff, der die Östrogentherapie, die Östrogen-Progesteron-Kombinationstherapie oder die Therapie mit Östrogenrezeptor-Agonisten oder -Antagonisten bezeichnet, spielt nach wie vor eine wichtige Rolle bei der Linderung der perimenopausalen und postmenopausalen Symptome.3 Obwohl jede Frau andere Erfahrungen macht, sind vasomotorische Symptome (VMS) und vulvovaginale Symptome zwei der häufigsten Beschwerden, die mit den hormonellen Veränderungen in den Wechseljahren einhergehen.4
Menopausale Symptome
VMS gehören zu den häufigsten und lästigsten Wechseljahrsbeschwerden. Hitzewallungen, die durch ein plötzliches Hitzegefühl in der oberen Brust und im Gesicht gekennzeichnet sind und 2 bis 4 Minuten andauern, treten bei etwa 75 % der Frauen in den Wechseljahren auf.1 Weitere mögliche VMS sind Schwitzen, Herzklopfen und Angstzustände.1 VMS wurden mit verminderter Schlafqualität, Reizbarkeit, Konzentrationsschwierigkeiten und verminderter Lebensqualität in Verbindung gebracht.3 Darüber hinaus wurden diese Symptome mit kardiovaskulären, knöchernen und kognitiven Risiken in Verbindung gebracht.5-9 Die Hormonersatztherapie ist seit langem als die wirksamste Behandlung für VMS anerkannt.4,10
Zusätzlich zum lästigen VMS leiden viele Frauen unter vulvovaginalen Symptomen. Man schätzt, dass 10 bis 40 % der Frauen an einer vaginalen Atrophie leiden.3 Eine vaginale Atrophie kann Schmerzen, Brennen und Juckreiz in der Vulva, vaginale Trockenheit, vaginalen Ausfluss, Dyspareunie (schwieriger oder schmerzhafter Geschlechtsverkehr) und Schmier- oder Blutungen nach dem Geschlechtsverkehr verursachen.1 Diese Symptome treten in der Regel in der späten postmenopausalen Phase auf und können zu Beschwerden bei eng anliegender Kleidung, beim Sitzen oder Sport oder bei sexueller Aktivität führen.1 Zur Behandlung vulvovaginaler Symptome wird in der Regel eine topische HRT empfohlen.1
Neben der Linderung der oben genannten Symptome gibt es Hinweise darauf, dass eine niedrig dosierte Standard-HRT auch postmenopausalen Hüft-, Wirbelsäulen- und anderen Frakturen vorbeugen kann.10 Zu den Vorteilen der HRT bei VMS und urogenitalen Symptomen gehören Verbesserungen bei überaktiver Blase, weniger Schlafstörungen, ein geringeres Risiko für Typ-2-Diabetes, ein potenzieller Schutz vor koronarer Herzkrankheit (KHK) und Myokardinfarkt, ein geringeres Osteoporose- oder Frakturrisiko und eine potenzielle Verringerung der Gesamtmortalität.1,10 Die Vorteile der HRT für die Knochendichte nehmen jedoch nach dem Absetzen rasch ab. Darüber hinaus sind zwar einige Präparate von der FDA zur Vorbeugung von Osteoporose zugelassen, aber keines von ihnen ist derzeit für die Behandlung von Osteoporose zugelassen. Zu den Hauptrisiken, die mit der Anwendung dieser Mittel verbunden sind, gehören venöse Thromboembolien (VTE), ischämische Schlaganfälle, ein erhöhtes Auftreten von Endometriumkrebs (wenn ein nicht entgegengesetztes Östrogen bei einer Frau mit Gebärmutter verwendet wird) und ein erhöhtes Brustkrebsrisiko, wenn die HRT länger als 3 bis 5 Jahre angewendet wird.4,10
Verfügbare HRT-Produkte
Eine breite Palette von HRT-Produkten ist in verschiedenen Darreichungsformen erhältlich.4 Zu den oralen Präparaten gehören konjugierte equine Östrogene (CEE), mikronisiertes 17-Beta-Östradiol (mikronisiert, um die Absorption zu verbessern), veresterte Östrogene, Ethinylöstradiol (ein hochwirksames Östrogenpräparat, das bei der HRT in viel niedrigeren Dosierungen als bei der oralen Kontrazeption eingesetzt wird), Östrogen-Gestagen-Kombinationstabletten und eine CEE/Bazedoxifen-Kombinationstablette.4
Die CEE/Bazedoxifen-Kombinationstablette, eine Kombination aus Östrogen und einem selektiven Östrogenrezeptormodulator, ist in den Vereinigten Staaten zur Behandlung von VMS in den Wechseljahren und zur Osteoporoseprävention erhältlich. In dieser Kombination verhindert Bazedoxifen die östrogenbedingte Endometriumhyperplasie und macht die Verabreichung eines Gestagens überflüssig. Allerdings wird Bazedoxifen mit einem erhöhten VTE-Risiko in Verbindung gebracht.4 Die Verwendung von Bazedoxifen hat sich bei einer Studiendauer von bis zu 7 Jahren bei der Behandlung von Osteoporose als sicher erwiesen, die Kombination wurde jedoch nur über kürzere Zeiträume untersucht.11,12 VMS-Studien mit einer Dauer von bis zu 2 Jahren haben keinen Anstieg der Häufigkeit von Brustspannen oder des Brustkrebsrisikos gezeigt.3 In den aktuellen Leitlinien wird die Anwendung von CEE/Bazedoxifen bei postmenopausalen Frauen mit Gebärmutter und ohne Kontraindikationen zur Behandlung von VMS und zur Vorbeugung von Knochenschwund empfohlen, wobei jedoch keine Angaben zur Dauer der Therapie gemacht werden.1 Auf der Grundlage der verfügbaren Daten scheint die Behandlung von VMS mit CEE/Bazedoxifen über einen Zeitraum von bis zu 2 Jahren sicher zu sein; die Sicherheit einer Anwendung über 2 Jahre hinaus ist nach wie vor unklar.
HRT ist auch in verschiedenen topischen Anwendungen erhältlich. Es gibt transdermale Pflasterpräparate mit 17-Beta-Östradiol oder Östrogen-Gestagen-Kombinationen. Andere topische Zubereitungen sind Gelpackungen oder Dosierpumpen, Sprays und Emulsionen.4 Auch Depotinjektionen können in Betracht gezogen werden, doch werden diese Produkte im Rahmen einer HRT nur selten verwendet.4 Eine Zusammenfassung der verfügbaren systemischen HRT-Formulierungen ist in TABELLE 1 enthalten.13-15
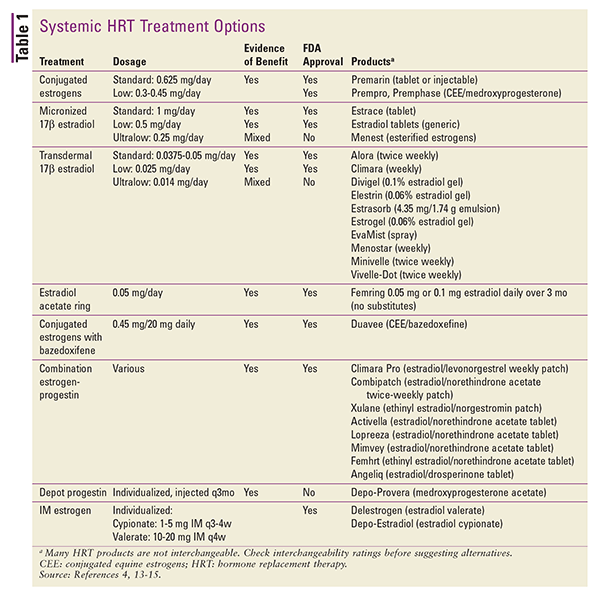
Bei der Umrechnung von einer Darreichungsform in eine andere können Unterschiede in der Art der Verabreichung und der Wirksamkeit des Produkts berücksichtigt werden, indem geschätzte Dosisäquivalente verwendet werden.4 Dosisäquivalente für orale Zubereitungen sind wie folgt: 1 mg mikronisiertes 17-beta-Estradiol entspricht 1,25 mg Piperazin-Estron-Sulfat. Bei der Umrechnung zwischen oralen und transdermalen Östrogenpräparaten entsprechen 0,05 mg/24 Stunden transdermal etwa 0,625 mg täglich durch den Mund.4
Lokale Präparate sind in der Regel niedrig dosiert und werden speziell zur Behandlung der Symptome der vulvovaginalen Atrophie eingesetzt.4 Höhere Dosen können zur Behandlung des systemischen VMS verwendet werden, dies wird jedoch im Allgemeinen nicht empfohlen.4 Zu den lokalen Präparaten gehören Vaginalringe, Tabletten und Cremes. Eine Zusammenfassung der verfügbaren lokalen HRT-Formulierungen finden Sie in TABELLE 2.4,13,15
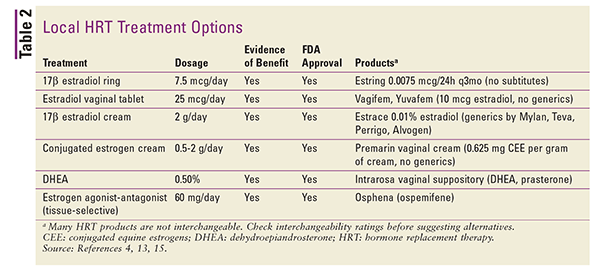
Aktuelle Leitlinienempfehlungen
Drei Organisationen – das American College of Obstetricians and Gynecologists (Amerikanisches Kollegium der Geburtshelfer und Gynäkologen), die North American Menopause Society (NAMS) und die Endocrine Society (Endokrine Gesellschaft) – haben Leitlinien zum Einsatz von HRT in der Menopause erstellt. Wie in diesen Leitlinien vermerkt, umfassen die Indikationen für eine HRT die Behandlung von VMS im Zusammenhang mit der Menopause und die Behandlung von vulvovaginalen Effekten bei Fehlen störender systemischer Symptome.1,3,4 Es wurde festgestellt, dass Östrogen allein oder in Kombination mit einem Gestagen das wöchentliche VMS um 75 % reduziert und den Schweregrad der Symptome im Vergleich zu Placebo deutlich verringert.4
Bei Frauen unter 60 Jahren, die weniger als 10 Jahre nach der Menopause an einem störenden VMS leiden und bei denen keine Kontraindikationen für eine HRT oder ein erhöhtes kardiovaskuläres oder Brustkrebsrisiko vorliegen, wird eine reine Östrogentherapie für Frauen ohne Gebärmutter empfohlen. Bei Patientinnen mit Gebärmutter wird die zusätzliche Gabe eines Gestagens empfohlen, um Endometriumhyperplasie und potenziellem Endometriumkrebs vorzubeugen.1,3,4 Gegenwärtig ist die erforderliche Gestagenexposition unklar, aber viele Anbieter verabreichen Gestagene in einem 14-tägigen Zyklus pro Monat.4 Für Frauen, die älter als 60 Jahre sind oder mehr als 10 Jahre nach der Menopause, wird empfohlen, anstelle einer HRT andere (nicht-hormonelle) Therapien in Betracht zu ziehen.3
Bei Frauen mit einem erhöhten Risiko für kardiovaskuläre Erkrankungen (definiert als >10% 10-Jahres-Risiko für kardiovaskuläre Erkrankungen gemäß dem American College of Cardiology/American Heart Association cardiovascular risk estimator tool) werden nichthormonelle Therapien bevorzugt.3 Bei Frauen mit mäßigem CVD-Risiko ist transdermales Östrogen mit oder ohne Gestagen einer oralen Therapie vorzuziehen, da diese Präparate weniger Auswirkungen auf den Blutdruck, die Lipide und den Kohlenhydratstoffwechsel haben.1 Bei Patientinnen mit erhöhtem VTE-Risiko sind nicht-orale Therapien in der niedrigsten wirksamen Dosis vorzuziehen. Schließlich werden bei Patientinnen mit hohem oder mittlerem Brustkrebsrisiko nicht-hormonelle Therapien bevorzugt.4
Wenn eine HRT gewählt wird, empfehlen alle Leitlinien die Verwendung der niedrigsten wirksamen Dosis.1,4,10 Ein Vorteil niedrigerer HRT-Dosen ist das bessere Nebenwirkungsprofil im Vergleich zu hochdosierten Schemata.4 Es gibt derzeit keinen bevorzugten Therapieweg für die Behandlung von VMS; daher sollte der Verabreichungsweg von der Präferenz der Patientin geleitet werden. Es sollte beachtet werden, dass transdermale Produkte möglicherweise mit einer geringeren Inzidenz von unerwünschten Wirkungen, wie z. B. VTE, in Verbindung gebracht werden, aber Studien werden noch durchgeführt.10
Für die Behandlung von Urogenitalsymptomen bei Frauen ohne eine Vorgeschichte von hormonabhängigen Krebserkrankungen kann niedrig dosiertes vaginales Östrogen verwendet werden.1 Bei reinen Vaginalsymptomen wird in den Leitlinien von der Zugabe eines Gestagens abgeraten, unabhängig davon, ob eine Gebärmutter vorhanden ist. Diese Therapie kann auch bei Patientinnen mit hormonabhängigen Krebserkrankungen in der Anamnese sinnvoll sein, aber in diesen Fällen sollte die Wahl der Therapie auf einem gemeinsamen Entscheidungsprozess beruhen, der eine Diskussion der Risiken und Vorteile beinhaltet. Zu den potenziellen Vorteilen von vaginalem Östrogen gehören eine rasche Verbesserung der vaginalen und harnableitenden Symptome und eine mögliche Vorbeugung von wiederkehrenden Harnwegsinfektionen. Zu den nicht-östrogenen, von der FDA zugelassenen und mit den Leitlinien übereinstimmenden Therapien zur Linderung von Dyspareunie gehören Ospemifen und intravaginales Dehydropiandrosteron.16,17
Reine Gestagen-Therapien, Testosteron, alternative nicht-hormonelle Therapien auf pflanzlicher Basis und zusammengesetzte bioidentische Hormone haben keine ausreichenden Daten und werden im Allgemeinen nicht empfohlen.1,4 Die NAMS erklärt, dass Verordner zusammengesetzte HRT in Situationen in Betracht ziehen können, in denen eine Patientin nicht in der Lage ist, von der FDA zugelassene Therapien zu vertragen.3 Zu den nicht-hormonellen Behandlungsoptionen für vasomotorische Symptome gehören selektive Serotonin-Wiederaufnahmehemmer und selektive Serotonin-Norepinephrin-Wiederaufnahmehemmer, Clonidin und Gabapentin, und zu den nicht-hormonellen Behandlungsoptionen für vaginale Symptome gehören Gleitmittel, Östrogen-Agonisten-Antagonisten und pflanzliche Heilmittel.4 Die Belege für den Einsatz nichthormoneller Therapien sind unterschiedlich, und nicht für alle Optionen gibt es gesicherte Erkenntnisse oder eine von der FDA zugelassene Indikation.4
Die Überwachung der HRT sollte regelmäßige Brustkrebsvorsorgeuntersuchungen während und nach Abschluss der Therapie umfassen. Wiederkehrende ungeplante Blutungen sollten rasch untersucht werden.1 Die Dauer der Therapie sollte mindestens einmal jährlich überprüft werden, wobei die kürzeste Behandlungsdauer zu bevorzugen ist.1 Wenn Patientinnen und Ärzte beschließen, die HRT abzusetzen, kann entweder eine Auslauf- oder eine abrupte Absetzstrategie angewendet werden. Über die Methoden des Absetzens gibt es keine gesicherten Erkenntnisse; daher wird für den Prozess des Absetzens eine gemeinsame Entscheidungsfindung empfohlen.1,4
Wechselwirkungen zwischen Arzneimitteln
Die meisten im Handel erhältlichen HRT-Produkte (TABELLE 1) werden über das CYP450-System in der Leber metabolisiert.15 Insbesondere Östrogenprodukte werden teilweise durch CYP3A4 verstoffwechselt; daher können starke Induktoren von CYP3A4 die Wirksamkeit von Östrogen-HRT verringern und starke Inhibitoren können die Serumkonzentrationen von Östrogen erhöhen. Darüber hinaus können andere Arzneimittelsubstrate für diese Enzyme den Metabolismus der HRT beeinträchtigen.15
Schwere und häufige Nebenwirkungen
Zu den wichtigsten Nebenwirkungen im Zusammenhang mit der HRT gehören Herz-Kreislauf-Erkrankungen, Brustkrebs, Endometrium- oder Eierstockkrebs, Schlaganfall und VTE.1 Die Anwendung von Östrogen ohne Gegenwirkung erhöht das Risiko von Endometriumhyperplasie und -krebs, weshalb bei Frauen mit Gebärmutter die zusätzliche Einnahme von Gestagen empfohlen wird. Was das Brustkrebsrisiko betrifft, so scheint es ein geringes Risiko zu geben, an Brustkrebs zu erkranken, wenn eine Frau 5 Jahre lang Östrogen einnimmt.3 Die derzeitige Literatur ist widersprüchlich, wenn es darum geht, das Risiko der Entwicklung von Eierstockkrebs durch eine HRT zu bestimmen.3 Es werden mehr randomisierte, kontrollierte Studien benötigt, um das tatsächliche Risiko der Entwicklung von Eierstockkrebs bei einer HRT-Anwendung zu ermitteln.1 Die Auswirkungen einer HRT auf die koronare Herzkrankheit (KHK), Schlaganfall und VTE variieren je nach dem Alter der Frau zum Zeitpunkt des Beginns der HRT oder der Zeit seit Beginn der Menopause. Es hat den Anschein, dass Frauen, die mehr als 10 Jahre nach Beginn der Menopause eine HRT einnehmen, ein erhöhtes Risiko für die Entwicklung einer KHK haben.3 Insgesamt deuten Studien darauf hin, dass orale und transdermale Formulierungen mit niedrigerer Dosierung ein geringeres Schlaganfall- und VTE-Risiko mit sich bringen als eine HRT mit Standarddosierung.3 Patientinnen, die bei Beginn der HRT älter als 60 Jahre sind oder bei denen der Beginn der Menopause mehr als 10 Jahre zurückliegt, haben ein erhöhtes Risiko für diese unerwünschten Wirkungen. Darüber hinaus besteht bei Frauen, die eine HRT mit Östrogenen entweder allein oder in Kombination einnehmen, ein erhöhtes Risiko für Gallensteine, Cholezystitis und Cholezystektomie.3 Das Risiko einer Gallenblasenerkrankung wurde mit der Anwendung oraler HRT in Verbindung gebracht und besteht möglicherweise nicht bei topischen oder transdermalen Formulierungen.1,3
Kontraindikationen
Die Leitlinien der Fachgesellschaften enthalten keine Liste absoluter oder relativer Kontraindikationen für die HRT.2 Daher ist, wie bei den meisten klinischen Entscheidungen, eine individuelle Risiko-Nutzen-Abwägung wichtig. Im Allgemeinen sollte eine HRT bei Patientinnen mit ungeklärten vaginalen Blutungen, Schlaganfall oder transitorischer ischämischer Attacke in der Vorgeschichte, Myokardinfarkt, Lungenembolie oder VTE, Brust- oder Endometriumkrebs, aktiver Lebererkrankung, bekanntem Protein-C-, Protein-S- oder Antithrombinmangel oder anderen thrombophilen Störungen sowie bekannter oder vermuteter Schwangerschaft vermieden werden.1 Darüber hinaus ist Vorsicht geboten bei Patienten mit Diabetes, Gallenblasenerkrankung, Hypertriglyceridämie (>400 mg/Tag), Hypoparathyreoidismus, gutartigem Meningeom, mittlerem oder hohem Risiko für Brustkrebs, hohem Risiko für Herzerkrankungen oder Migräne mit Aura.2
Beratungspunkte
Eine Zusammenfassung der wichtigsten Beratungspunkte für Patientinnen und Nebenwirkungen der verschiedenen HRT-Typen finden Sie in TABELLE 3.15
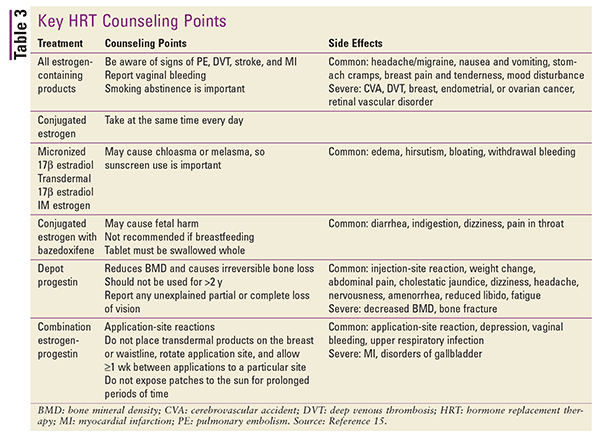
Schlussfolgerung
Die HRT, die in einer breiten Palette von Präparaten erhältlich ist, ist die wirksamste Behandlung sowohl für VMS als auch für urogenitale Symptome. Da die mit der HRT verbundenen Risiken bei jeder Frau anders sind, sollte die Behandlung individuell angepasst werden und darauf abzielen, die Wirksamkeit zu maximieren, die Therapiedauer zu minimieren und das Risiko unerwünschter Wirkungen zu verringern. In Fällen, in denen eine HRT nicht in Frage kommt, stehen nicht-hormonelle Behandlungsmöglichkeiten sowohl für VMS als auch für Symptome des Urogenitaltrakts zur Verfügung, aber die Wirksamkeit und die FDA-Zulassung dieser Produkte sind unterschiedlich; daher sollten die Wirksamkeitsdaten für diese Produkte überprüft werden.
1. Stuenkel CA, Davis SR, Gompel A, et al. Behandlung von Wechseljahrsbeschwerden: eine klinische Praxisleitlinie der Endocrine Society. J Clin Endocrinol Metab. 2015;100(11):3975-4011.
2. Shifren JL, Schiff I. Role of hormone therapy in the management of menopause. Obstet Gynecol. 2010;115(4):839-855.
3. The NAMS 2017 Hormone Therapy Position Statement Advisory Panel. Die Hormontherapie-Positionserklärung 2017 der North American Menopause Society. Menopause. 2017;24(7):728-753.
4. ACOG Practice Bulletin No. 141: management of menopausal symptoms. Obstet Gynecol. 2014;123(1):202-216.
5. Thurston RC, Sutton-Tyrrell K, Everson-Rose SA, et al. Hitzewallungen und subklinische Herz-Kreislauf-Erkrankungen: Ergebnisse der Study of Women’s Health Across the Nation Heart Study. Circulation. 2008;118(12):1234-1240.
6. Thurston RC, Kuller LH, Edmundowicz D, Matthews KA. Vorgeschichte von Hitzewallungen und Aortenverkalkung bei postmenopausalen Frauen. Menopause. 2010;17(2):256-261.
7. Thurston RC, Sutton-Tyrrell K, Everson-Rose SA, et al. Hot flashes and carotid intima media thickness among midlife women. Menopause. 2011;18(4):352-358.
8. Crandall CJ, Aragaki A, Cauley JA, et al. Associations of menopausal vasomotor symptoms with fracture incidence. J Clin Endocrinol Metab. 2015;100(2):524-534.
9. Maki PM. Verbales Gedächtnis und Menopause. Maturitas. 2015;82(3):288-290.
10. North American Menopause Society. The 2012 hormone therapy position statement of: The North American Menopause Society. Menopause. 2012;19(3):257-271.
11. Palacios S, Silverman SL, de Villiers TJ, et al. A 7-year randomized, placebo-controlled trial assessing the long-term efficacy and safety of bazedoxifene in postmenopausal women with osteoporosis: effects on bone density and fracture. Menopause. 2015;22(8):806-813.
12. Archer DF, Freeman EW, Komm BS, et al. Pooled analysis of the effects of conjugated estrogens/bazedoxifene on vasomotor symptoms in the selective estrogens, menopause, and response to therapy trials. J Womens Health (Larchmt). 2016;25(11):1102-1111.
13. FDA. Orange Book: Zugelassene Arzneimittel mit Bewertungen der therapeutischen Äquivalenz. Product details for ANDA 204726. www.accessdata.fda.gov/scripts/cder/ob/results_product.cfm?Appl_Type=A&Appl_No=204726. Accessed March 18, 2018.
14. FDA. Drugs@FDA: FDA approved drug products. www.accessdata.fda.gov/scripts/cder/daf/index.cfm. Accessed June 17, 2018.
15. DrugDex . Greenwood Village, CO: Truven Health Analytics, Inc. www.micromedexsolutions.com. Accessed June 15, 2018.
16. Constantine G, Graham S, Portman DJ, et al. Weibliche Sexualfunktion verbessert mit Ospemifen bei postmenopausalen Frauen mit Vulva- und Vaginalatrophie: Ergebnisse einer randomisierten, placebokontrollierten Studie. Climacteric. 2015;18(2):226-232.
17. Labrie F, Archer DF, Koltun W, et al. Efficacy of intravaginal dehydroepiandrosterone (DHEA) on moderate to severe dyspareunia and vaginal dryness, symptoms of vulvovaginal atrophy, and of the genitourinary syndrome of menopause. Menopause. 2016;23(3):243-256.