Generischer Name: Butalbital, Aspirin und Koffein
Dosierung Form: Kapsel
Medically reviewed by Drugs.com. Zuletzt aktualisiert am 22. Juni 2020.
- Übersicht
- Nebenwirkungen
- Dosierung
- Behandlung
- Interaktionen
- Mehr
- Fiorinal Beschreibung
- Fiorinal – Klinische Pharmakologie
- ANWENDUNGEN
- Kontraindikationen
- Warnungen
- Vorsichtsmaßnahmen
- Allgemein
- Informationen für Patienten
- Laboruntersuchungen
- Arzneimittelwechselwirkungen
- Wechselwirkungen zwischen Medikamenten und Labortests
- Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
- Verwendung in der Schwangerschaft
- Labor und Geburt
- Stillende Mütter
- Pädiatrische Anwendung
- Nebenwirkungen
- Drogenmissbrauch und -abhängigkeit
- Überdosierung
- Fiorinale Dosierung und Anwendung
- Wie wird Fiorinal geliefert
- Aufbewahrung und Abgabe
- Hauptanzeigetafel
- Mehr über Fiorinal (Aspirin / Butalbital / Koffein)
- Ressourcen für Verbraucher
- Ressourcen für Fachleute
- Andere Formulierungen
- Verwandte Behandlungsleitfäden
Fiorinal Beschreibung
Fiorinal (Butalbital, Aspirin und Koffein Kapseln, USP) wird in Kapselform zur oralen Einnahme geliefert.
Jede Kapsel enthält die folgenden Wirkstoffe:
| Butalbital, USP . . . . . . . . . | 50 mg |
| Aspirin, USP . . . . . . . . . . . . . . | 325 mg |
| Koffein, USP . | 40 mg |
Butalbital (5-Allyl-5-isobutylbarbitursäure) ist ein kurz- bis mittelwirkendes Barbiturat. Es hat die folgende Strukturformel:
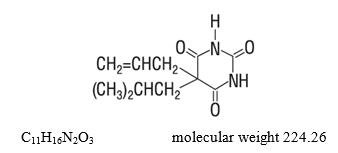
Aspirin (Benzoesäure, 2-(Acetyloxy)-) ist ein Analgetikum, Antipyretikum und Entzündungshemmer. Es hat die folgende Strukturformel:
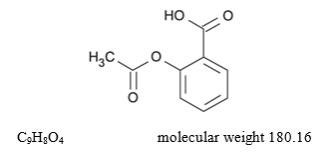
Koffein (1,3,7-Trimethylxanthin) ist ein Stimulans des zentralen Nervensystems. Es hat die folgende Strukturformel:
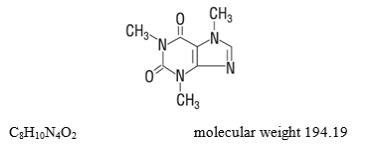
Inaktive Bestandteile: mikrokristalline Cellulose, Quellstärke und Talkum. Gelatinekapseln enthalten D&C Gelb Nr. 10, FD&C Grün Nr. 3, und Gelatine. Die Kapseln sind mit essbarer Tinte bedruckt, die rotes Eisenoxid enthält.
Fiorinal – Klinische Pharmakologie
Pharmakologisch kombiniert Fiorinal die analgetischen Eigenschaften von Aspirin mit den anxiolytischen und muskelentspannenden Eigenschaften von Butalbital.
Die klinische Wirksamkeit von Fiorinal bei Spannungskopfschmerzen wurde in doppelblinden, placebokontrollierten, klinikübergreifenden Studien nachgewiesen. In einer Studie mit faktoriellem Design wurde Fiorinal mit jedem seiner Hauptbestandteile verglichen. Diese Studie zeigte, dass jede Komponente zur Wirksamkeit von Fiorinal bei der Behandlung der Zielsymptome von Spannungskopfschmerzen (Kopfschmerz, psychische Anspannung und Muskelkontraktion im Kopf-, Nacken- und Schulterbereich) beiträgt. Für jedes Symptom und den Symptomkomplex als Ganzes wurde gezeigt, dass Fiorinal eine signifikant bessere klinische Wirkung hat als eine der beiden Komponenten allein.
Pharmakokinetik
Das Verhalten der einzelnen Komponenten wird im Folgenden beschrieben.
Aspirin
Die systemische Verfügbarkeit von Aspirin nach einer oralen Dosis ist in hohem Maße abhängig von der Darreichungsform, dem Vorhandensein von Nahrung, der Magenentleerungszeit, dem pH-Wert des Magens, Antazida, Puffermitteln und der Partikelgröße. Diese Faktoren beeinflussen nicht unbedingt das Ausmaß der Absorption der gesamten Salicylate, sondern vielmehr die Stabilität von Aspirin vor der Absorption.
Während des Absorptionsprozesses und nach der Absorption wird Aspirin hauptsächlich zu Salicylsäure hydrolysiert und in allen Körpergeweben und -flüssigkeiten verteilt, einschließlich fötalen Geweben, Muttermilch und dem zentralen Nervensystem (ZNS). Die höchsten Konzentrationen finden sich in Plasma, Leber, Nierenrinde, Herz und Lunge. Im Plasma sind etwa 50-80 % der Salicylsäure und ihrer Metaboliten lose an Plasmaproteine gebunden.
Die Clearance der gesamten Salicylate unterliegt einer sättigbaren Kinetik; die Eliminationskinetik erster Ordnung ist jedoch für Dosen bis zu 650 mg immer noch ein guter Näherungswert. Die Plasmahalbwertszeit für Aspirin beträgt etwa 12 Minuten und für Salicylsäure und/oder Gesamtsalicylate etwa 3 Stunden.
Die Ausscheidung therapeutischer Dosen erfolgt über die Nieren entweder als Salicylsäure oder andere Biotransformationsprodukte. Die renale Clearance wird durch einen alkalischen Urin, wie er durch gleichzeitige Verabreichung von Natriumbicarbonat oder Kaliumcitrat erzeugt wird, stark erhöht.
Die Biotransformation von Aspirin findet hauptsächlich in den Hepatozyten statt. Die wichtigsten Metaboliten sind Salicylursäure (75 %), die Phenol- und Acylglucuronide von Salicylat (15 %) sowie Gentisinsäure und Gentisursäure (1 %). Die Bioverfügbarkeit der Aspirin-Komponente von Fiorinal entspricht der einer Lösung, mit Ausnahme einer langsameren Absorptionsrate. Eine Spitzenkonzentration von 8,8 mcg/ml wurde 40 Minuten nach einer Dosis von 650 mg erreicht.
Hinweise zur Toxizität siehe ÜBERDOSIERUNG.
Butalbital
Butalbital wird gut aus dem Magen-Darm-Trakt resorbiert und verteilt sich voraussichtlich in den meisten Geweben des Körpers. Barbiturate können im Allgemeinen in die Muttermilch übergehen und die Plazentaschranke leicht überwinden. Sie werden in unterschiedlichem Maße an Plasma- und Gewebeproteine gebunden, wobei die Bindung direkt mit der Lipidlöslichkeit zunimmt.
Butalbital wird in erster Linie über die Niere (59%-88% der Dosis) als unveränderte Droge oder Metaboliten ausgeschieden. Die Plasmahalbwertszeit beträgt etwa 35 Stunden. Zu den mit dem Urin ausgeschiedenen Produkten gehören das Grundarzneimittel (ca. 3,6 % der Dosis), 5-Isobutyl-5-(2,3-dihydroxypropyl)-Barbitursäure (ca. 24 % der Dosis), 5-Allyl-5-(3-hydroxy-2-methyl-1-propyl)-Barbitursäure (ca. 4,8 % der Dosis), Produkte, bei denen der Barbitursäurering mit der Ausscheidung von Harnstoff hydrolysiert wurde (ca. 14 % der Dosis), sowie nicht identifiziertes Material. Von den im Urin ausgeschiedenen Stoffen waren 32 % konjugiert.
Die Bioverfügbarkeit der Butalbitalkomponente von Fiorinal entspricht der einer Lösung, abgesehen von einer Verringerung der Absorptionsrate. Eine Spitzenkonzentration von 2.020 ng/ml wird etwa 1,5 Stunden nach einer Dosis von 100 mg erreicht.
Die In-vitro-Plasmaproteinbindung von Butalbital beträgt 45 % über den Konzentrationsbereich von 0,5-20 mcg/ml. Dies fällt in den Bereich der Plasmaproteinbindung (20%-45%), der für andere Barbiturate wie Phenobarbital, Pentobarbital und Secobarbital-Natrium berichtet wurde. Das Verhältnis von Plasma- zu Blutkonzentration war fast gleich, was darauf hindeutet, dass es keine bevorzugte Verteilung von Butalbital im Plasma oder in den Blutzellen gibt.
Hinweise zur Toxizität siehe ÜBERDOSIERUNG.
Koffein
Wie die meisten Xanthine wird Koffein schnell absorbiert und in allen Körpergeweben und -flüssigkeiten verteilt, einschließlich des ZNS, des fötalen Gewebes und der Muttermilch.
Koffein wird schnell durch Metabolismus und Ausscheidung im Urin abgebaut. Die Plasmahalbwertszeit beträgt etwa 3 Stunden. Die hepatische Biotransformation vor der Ausscheidung führt zu etwa gleichen Mengen an 1-Methylxanthin und 1-Methyluronsäure. Von den 70 % der Dosis, die im Urin wiedergefunden wurden, waren nur 3 % unveränderter Wirkstoff.
Die Bioverfügbarkeit der Koffeinkomponente von Fiorinal entspricht der einer Lösung, mit Ausnahme einer etwas längeren Zeit bis zum Erreichen des Spitzenwertes. Eine Spitzenkonzentration von 1.660 ng/ml wurde bei einer Dosis von 80 mg in weniger als einer Stunde erreicht.
Hinweise zur Toxizität siehe ÜBERDOSIERUNG.
ANWENDUNGEN
Fiorinal ist indiziert zur Linderung des Symptomenkomplexes von Spannungskopfschmerz (oder Muskelkontraktionskopfschmerz). Belege für die Wirksamkeit und Sicherheit von Fiorinal bei der Behandlung von mehrfach wiederkehrenden Kopfschmerzen liegen nicht vor. Diesbezüglich ist Vorsicht geboten, da Butalbital gewohnheitsbildend und potenziell missbräuchlich ist.
Kontraindikationen
Fiorinal ist unter den folgenden Bedingungen kontraindiziert:
- Überempfindlichkeit oder Unverträglichkeit gegenüber Aspirin, Koffein oder Butalbital.
- Patienten mit einer hämorrhagischen Diathese (z.B., Hämophilie, Hypoprothrombinämie, von-Willebrand-Krankheit, Thrombozytopenien, Thrombasthenie und andere nicht definierte hereditäre Thrombozytenfunktionsstörungen, schwerer Vitamin-K-Mangel und schwere Leberschäden).
- Patienten mit dem Syndrom der Nasenpolypen, Angioödemen und bronchospastischer Reaktivität auf Aspirin oder andere nichtsteroidale entzündungshemmende Arzneimittel. Bei solchen Patienten sind anaphylaktoide Reaktionen aufgetreten.
- Peptisches Ulkus oder andere schwere gastrointestinale Läsionen.
- Patienten mit Porphyrie.
Warnungen
Therapeutische Dosen von Aspirin können einen anaphylaktischen Schock und andere schwere allergische Reaktionen hervorrufen. Es sollte festgestellt werden, ob der Patient allergisch auf Aspirin reagiert, auch wenn keine spezifische Allergieanamnese vorliegt.
Bei Patienten mit Magengeschwüren oder anderen gastrointestinalen Läsionen sowie bei Patienten mit Blutungsstörungen kann eine Aspirintherapie zu erheblichen Blutungen führen. Aspirin, das präoperativ verabreicht wird, kann die Blutungszeit verlängern. Butalbital ist gewohnheitsbildend und potenziell missbrauchbar. Daher wird die längere Anwendung von Fiorinal nicht empfohlen. Ergebnisse epidemiologischer Studien deuten auf einen Zusammenhang zwischen Aspirin und dem Reye-Syndrom hin. Vorsicht ist geboten bei der Verabreichung dieses Produkts an Kinder, einschließlich Jugendlicher, mit Windpocken oder Grippe.
Vorsichtsmaßnahmen
Allgemein
Fiorinal sollte mit Vorsicht bei bestimmten Risikopatienten wie älteren oder geschwächten Menschen und solchen mit schwerer Beeinträchtigung der Nieren- oder Leberfunktion, Gerinnungsstörungen, Kopfverletzungen, erhöhtem Hirndruck, akuten abdominalen Zuständen, Hypothyreose, Harnröhrenstriktur, Morbus Addison oder Prostatahypertrophie verschrieben werden.
Aspirin sollte mit Vorsicht bei Patienten unter gerinnungshemmender Therapie und bei Patienten mit zugrundeliegenden hämostatischen Defekten sowie mit äußerster Vorsicht bei Vorliegen eines Magengeschwürs angewendet werden.
Bei der Verabreichung von Salicylaten an Personen mit bekannten Allergien sind Vorsichtsmaßnahmen zu treffen. Eine Überempfindlichkeit gegen Aspirin ist besonders wahrscheinlich bei Patienten mit Nasenpolypen und relativ häufig bei Patienten mit Asthma.
Informationen für Patienten
Die Patienten sollten darüber informiert werden, dass Fiorinal Aspirin enthält und nicht von Patienten mit einer Aspirinallergie eingenommen werden sollte.
Fiorinal kann die geistigen und/oder körperlichen Fähigkeiten beeinträchtigen, die für die Ausführung potenziell gefährlicher Aufgaben wie das Führen eines Fahrzeugs oder das Bedienen von Maschinen erforderlich sind. Solche Aufgaben sollten während der Einnahme von Fiorinal vermieden werden.
Alkohol und andere ZNS-Depressiva können bei gleichzeitiger Einnahme von Fiorinal eine additive ZNS-Depression hervorrufen und sollten vermieden werden.
Butalbital kann gewohnheitsbildend sein. Die Patienten sollten das Arzneimittel nur so lange wie vorgeschrieben, in der vorgeschriebenen Menge und nicht häufiger als vorgeschrieben einnehmen.
Laboruntersuchungen
Bei Patienten mit schweren Leber- oder Nierenerkrankungen sollten die Auswirkungen der Therapie mit seriellen Leber- und/oder Nierenfunktionstests überwacht werden.
Arzneimittelwechselwirkungen
Die ZNS-Wirkungen von Butalbital können durch Monoaminoxidase-Hemmer (MAO) verstärkt werden.
Bei Patienten, die gleichzeitig Kortikosteroide und Aspirin einnehmen, kann das Absetzen der Kortikosteroide zu Salicylismus führen, da Kortikosteroide die renale Clearance von Salicylaten erhöhen und nach dem Absetzen der Kortikosteroide die renale Clearance wieder normalisiert wird.
Fiorinal kann die Wirkung von:
- Oralen Antikoagulantien verstärken, indem es die Prothrombinbildung in der Leber hemmt und Antikoagulantien von Plasmaprotein-Bindungsstellen verdrängt.
- Orale Antidiabetika und Insulin, verursachen Hypoglykämie durch einen additiven Effekt, wenn die Dosierung von Fiorinal die empfohlene Tageshöchstdosis überschreitet.
- 6-Mercaptopurin und Methotrexat, verursachen Knochenmarkstoxizität und Blutdyskrasien durch Verdrängung dieser Arzneimittel von sekundären Bindungsstellen und, im Falle von Methotrexat, auch durch Verringerung seiner Ausscheidung.
- Nicht-steroidale entzündungshemmende Mittel, die das Risiko von Magengeschwüren und Blutungen durch additive Wirkungen erhöhen.
- Andere narkotische Analgetika, Alkohol, Allgemeinanästhetika, Beruhigungsmittel wie Chlordiazepoxid, Sedativa-Hypnotika oder andere ZNS-Depressiva, die eine erhöhte ZNS-Depression verursachen.
Fiorinal kann die Wirkung von:
Uricosurika wie Probenecid und Sulfinpyrazon abschwächen, was ihre Wirksamkeit bei der Behandlung von Gicht verringert. Aspirin konkurriert mit diesen Mitteln um Proteinbindungsstellen.
Wechselwirkungen zwischen Medikamenten und Labortests
Aspirin: Aspirin kann die folgenden Laborbestimmungen im Blut beeinträchtigen: Serumamylase, Nüchternblutzucker, Cholesterin, Eiweiß, Serum-Glutamat-Oxalessig-Transaminase (SGOT), Harnsäure, Prothrombinzeit und Blutungszeit. Aspirin kann die folgenden Laborbestimmungen im Urin stören: Glucose, 5-Hydroxyindolessigsäure, Gerhardt-Keton, Vanillylmandelsäure (VMA), Harnsäure, Diessigsäure und den spektrophotometrischen Nachweis von Barbituraten.
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Angemessene Langzeitstudien mit Aspirin, allein oder in Kombination mit anderen Arzneimitteln, wurden an Mäusen und Ratten durchgeführt, in denen keine Anzeichen von Karzinogenese festgestellt wurden. Es wurden keine angemessenen Studien an Tieren durchgeführt, um festzustellen, ob Aspirin ein Potenzial zur Mutagenese oder zur Beeinträchtigung der Fruchtbarkeit hat. Es wurden keine angemessenen Studien an Tieren durchgeführt, um festzustellen, ob Butalbital ein Potenzial zur Karzinogenese, Mutagenese oder Beeinträchtigung der Fruchtbarkeit hat.
Verwendung in der Schwangerschaft
Teratogene Wirkungen:
Fiorinal wurde nicht in Reproduktionsstudien an Tieren untersucht. Es ist auch nicht bekannt, ob Fiorinal den Fötus schädigen kann, wenn es einer schwangeren Frau verabreicht wird, oder ob es die Fortpflanzungsfähigkeit beeinträchtigt. Fiorinal sollte einer schwangeren Frau nur bei eindeutiger Notwendigkeit verabreicht werden.
Nicht-teratogene Wirkungen:
Bei einem zwei Tage alten männlichen Säugling, dessen Mutter in den letzten 2 Monaten der Schwangerschaft ein Butalbital-haltiges Arzneimittel eingenommen hatte, wurden Entzugskrämpfe beobachtet. Butalbital wurde im Serum des Säuglings nachgewiesen. Der Säugling erhielt Phenobarbital 5 mg/kg, das ohne weitere Krampfanfälle oder andere Entzugssymptome abgesetzt werden konnte.
Studien über die Verwendung von Aspirin bei schwangeren Frauen haben nicht gezeigt, dass Aspirin das Risiko von Missbildungen erhöht, wenn es während des ersten Trimesters der Schwangerschaft verabreicht wird. In kontrollierten Studien, an denen 41 337 schwangere Frauen und ihre Kinder teilnahmen, gab es keine Hinweise darauf, dass die Einnahme von Aspirin während der Schwangerschaft zu Totgeburten, Todesfällen bei Neugeborenen oder einem geringeren Geburtsgewicht führt. In kontrollierten Studien mit 50.282 schwangeren Frauen und ihren Nachkommen zeigte die Verabreichung von Aspirin in mäßigen und hohen Dosen während der ersten vier Mondmonate der Schwangerschaft keine teratogene Wirkung.
Therapeutische Dosen von Aspirin bei schwangeren Frauen kurz vor der Geburt können Blutungen bei Mutter, Fötus oder Neugeborenem verursachen. In den letzten 6 Monaten der Schwangerschaft kann die regelmäßige Einnahme von Aspirin in hohen Dosen die Schwangerschaft und Geburt verlängern.
Labor und Geburt
Die Einnahme von Aspirin vor der Geburt kann die Geburt verlängern oder zu Blutungen bei der Mutter oder dem Neugeborenen führen.
Stillende Mütter
Aspirin, Koffein und Barbiturate werden in geringen Mengen in die Muttermilch ausgeschieden, aber die Bedeutung ihrer Auswirkungen auf den stillenden Säugling ist nicht bekannt. Wegen des Potenzials für schwerwiegende Nebenwirkungen von Fiorinal bei stillenden Säuglingen sollte unter Berücksichtigung der Bedeutung des Arzneimittels für die Mutter entschieden werden, ob das Stillen unterbrochen oder das Arzneimittel abgesetzt werden soll.
Pädiatrische Anwendung
Sicherheit und Wirksamkeit bei pädiatrischen Patienten wurden nicht nachgewiesen.
Nebenwirkungen
Die häufigsten Nebenwirkungen sind Schläfrigkeit und Schwindel. Weniger häufige Nebenwirkungen sind Benommenheit und gastrointestinale Störungen einschließlich Übelkeit, Erbrechen und Blähungen. Im Zusammenhang mit der Anwendung von Fiorinal wurde ein einziger Fall von Knochenmarksuppression gemeldet. Es wurden mehrere Fälle von dermatologischen Reaktionen, einschließlich toxischer epidermaler Nekrolyse und Erythema multiforme, berichtet.
Drogenmissbrauch und -abhängigkeit
Kontrollierte Substanz
Fiorinal wird von der Drug Enforcement Administration kontrolliert und ist unter Schedule III eingestuft.
Missbrauch und Abhängigkeit
Butalbital
Barbiturate können gewohnheitsbildend sein: Toleranz, psychische Abhängigkeit und körperliche Abhängigkeit können vor allem nach längerem Gebrauch hoher Dosen von Barbituraten auftreten. Die durchschnittliche Tagesdosis für einen Barbituratabhängigen beträgt in der Regel etwa 1.500 mg. Wenn sich eine Toleranz gegenüber Barbituraten entwickelt, steigt die Menge, die benötigt wird, um den gleichen Grad der Intoxikation aufrechtzuerhalten; die Toleranz gegenüber einer tödlichen Dosis steigt jedoch nicht mehr als um das Zweifache. In diesem Fall wird die Spanne zwischen einer Rauschdosis und einer tödlichen Dosis kleiner. Die tödliche Dosis eines Barbiturats ist weitaus geringer, wenn gleichzeitig Alkohol eingenommen wird. Schwere Entzugserscheinungen (Krämpfe und Delirium) können innerhalb von 16 Stunden auftreten und bis zu 5 Tage nach abruptem Absetzen dieser Drogen anhalten. Die Intensität der Entzugssymptome nimmt über einen Zeitraum von etwa 15 Tagen allmählich ab. Die Behandlung der Barbiturat-Abhängigkeit besteht in einem vorsichtigen und schrittweisen Entzug der Droge. Für die Entwöhnung von Barbiturat abhängigen Patienten gibt es eine Reihe von verschiedenen Entwöhnungsmethoden. Eine Methode besteht darin, die Behandlung mit der regulären Dosierung des Patienten zu beginnen und die Tagesdosis allmählich zu verringern, wie es vom Patienten toleriert wird.
Überdosierung
Die toxischen Wirkungen einer akuten Überdosierung von Fiorinal sind hauptsächlich auf seine Barbiturat-Komponente und in geringerem Maße auf Aspirin zurückzuführen. Da toxische Wirkungen von Koffein nur in sehr hohen Dosierungen auftreten, ist die Möglichkeit einer signifikanten Koffeintoxizität bei einer Überdosierung von Fiorinal unwahrscheinlich.
Anzeichen und Symptome
Symptome, die auf eine akute Barbituratvergiftung zurückzuführen sind, sind Schläfrigkeit, Verwirrung und Koma, Atemdepression, Hypotonie und hypovolämischer Schock. Zu den Symptomen einer akuten Aspirinvergiftung gehören Hyperpnoe, Säure-Basen-Störungen mit Entwicklung einer metabolischen Azidose, Erbrechen und Bauchschmerzen, Tinnitus, Hyperthermie, Hypoprothrombinämie, Unruhe, Delirium, Krämpfe. Eine akute Koffeinvergiftung kann Schlaflosigkeit, Unruhe, Zittern und Delirium, Tachykardie und Extrasystolen verursachen.
Behandlung
Die Behandlung besteht in erster Linie aus der Behandlung der Barbiturat-Intoxikation und der Korrektur des Säure-Basen-Ungleichgewichts aufgrund des Salicylismus. Bei bewussten Patienten sollte das Erbrechen mechanisch oder mit Brechmitteln herbeigeführt werden. Eine Magenspülung kann durchgeführt werden, wenn die Rachen- und Kehlkopfreflexe vorhanden sind und weniger als 4 Stunden seit der Einnahme vergangen sind. Bei bewusstlosen Patienten sollte vor der Magenspülung ein Endotrachealtubus mit Manschette eingelegt werden, wenn dies zur Unterstützung der Beatmung erforderlich ist. Die Diurese, die Alkalisierung des Urins und die Korrektur von Elektrolytstörungen sollten durch die Verabreichung intravenöser Flüssigkeiten wie z. B. 1 % Natriumbicarbonat in 5 % Dextrose in Wasser erreicht werden. Auf die Aufrechterhaltung einer angemessenen Lungenventilation sollte sorgfältig geachtet werden. Der Nutzen von Vasopressoren wie Noradrenalin oder Phenylephrinhydrochlorid bei der Behandlung von Hypotonie ist fraglich, da sie die Gefäßverengung verstärken und den Blutfluss verringern. Wenn jedoch eine längere Unterstützung des Blutdrucks erforderlich ist, kann Norepinephrin Bitartrat (Levophed®) intravenös verabreicht werden, wobei die üblichen Vorsichtsmaßnahmen zu beachten sind und der Blutdruck in regelmäßigen Abständen überwacht werden muss. In schweren Vergiftungsfällen kann eine Peritonealdialyse, Hämodialyse oder eine Austauschtransfusion lebensrettend sein. Hypoprothrombinämie sollte mit Vitamin K, intravenös, behandelt werden.
Aktuelle Informationen über die Behandlung von Überdosierungen können oft von einem zertifizierten regionalen Giftinformationszentrum erhalten werden. Die Telefonnummern der zertifizierten regionalen Giftnotrufzentralen sind in der Physicians‘ Desk Reference® aufgeführt.
Toxische und tödliche Dosen (für Erwachsene)
Butalbital: toxische Dosis 1 g (20 Kapseln)
Aspirin: toxischer Blutspiegel größer als 30 mg/100 mL; tödliche Dosis 10-30 g
Koffein: toxische Dosis 1 g (25 Kapseln)
Fiorinale Dosierung und Anwendung
Eine oder 2 Kapseln alle 4 Stunden. Die tägliche Gesamtdosis sollte 6 Kapseln nicht überschreiten. Eine längere und wiederholte Einnahme dieses Produktes wird wegen der Gefahr einer körperlichen Abhängigkeit nicht empfohlen.
Wie wird Fiorinal geliefert
Fiorinal® (Butalbital-, Aspirin- und Koffein-Kapseln, USP)
Helle, kellygrüne Kappe mit hellgrünem Körper. Auf jeder Kapselhälfte ist in roter Farbe „Fiorinal 955“ aufgedruckt.
Die 100er-Flaschen werden mit kindergesicherten Verschlüssen geliefert. (NDC 0023-6146-01)
Aufbewahrung und Abgabe
Unter 25°C (77°F); dicht verschlossen. Vor Feuchtigkeit schützen.
Nur Rx
Für alle medizinischen Anfragen wenden Sie sich an:
Allergan
Medizinische Kommunikation
Vertrieben durch:
Allergan USA, Inc.
Madison, NJ 07940
© 2018 Allergan. Alle Rechte vorbehalten.
Fiorinal® ist eine eingetragene Marke von Allergan Sales, LLC.
Allergan® und sein Design sind Marken von Allergan, Inc.
Alle Marken sind Eigentum ihrer jeweiligen Inhaber.
Inhalt aktualisiert: Juni 2018
v1.0USPI6146
Hauptanzeigetafel
NDC 0023-6146-01
Fiorinal®
(Butalbital, Aspirin und
Koffein Kapseln, USP)
100 Kapseln
Rx only

| Fiorinal Butalbital, Aspirin und Koffein Kapsel |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Labeler – Allergan, Inc. (144796497)
Mehr über Fiorinal (Aspirin / Butalbital / Koffein)
- Nebenwirkungen
- Während der Schwangerschaft
- Dosierungshinweise
- Drogen Bilder
- Wechselwirkungen
- Preisangaben &Gutscheine
- En Español
- 72 Bewertungen
- Verfügbarkeit von Generika
- Medikamentenklasse: Analgetika-Kombinationen
Ressourcen für Verbraucher
- Patienteninformationen
Ressourcen für Fachleute
- Verschreibungsinformationen
Andere Formulierungen
- Fiorinal mit Codein
Verwandte Behandlungsleitfäden
- Schmerz
- Migräne
- Kopfschmerzen
Medizinischer Haftungsausschluss